Jak se tvoří hydroxidy? (s příklady)
Různé / / July 04, 2021
The hydroxidy výsledek kombinace a oxid kovu (také zvaný bazické oxidy) A voda. Tímto způsobem je složení hydroxidů dáno třemi elementy: kyslík, vodík a dotyčný kov. V kombinaci se kov vždy se chovej jako kation a hydroxidová skupina (OH–) působí jako anion. Například:
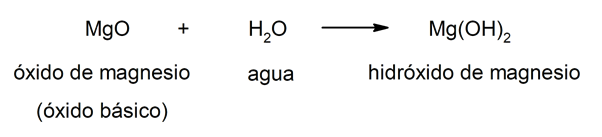
Hydroxidy obecně sdílejí řadu charakteristik, jako je hořká chuť a žíravost. Kromě toho jsou obvykle kluzké na dotek a korozivní. Na druhou stranu mají některé vlastnosti detergentů a mýdel. Většina z nich je rozpustná ve vodě a reaguje s kyseliny k výrobě jdete ven.
Některé vlastnosti jsou naproti tomu specifické pro každý typ hydroxidu, jako například sodík (NaOH), který absorbuje vodu a ve směsi s páleným vápnem (CaO) rychle absorbuje oxid uhličitý (CO2). Z jeho strany hydroxid vápenatý (Ca (OH)2) získává se reakcí oxidu vápenatého s vodou a také absorbuje CO2. Dalším příkladem je hydroxid železitý (Fe (OH)2), což je želatinová sloučenina a je prakticky nerozpustný ve vodě.
Hydroxidy se také nazývají zásady nebo zásady, ačkoli tyto termíny byly rozšířeny i pro další látky zásaditého charakteru, které nejsou hydroxidy.
Na co se hydroxidy používají?
Aplikace hydroxidů se také liší v různých případech:
Názvosloví
Stejně jako pojmenovat další typy chemické sloučeniny, existují různé nomenklatury pro hydroxidy:
Příklady hydroxidů
- Hydroxid olovnatý, Pb (OH)2dihydroxid olovnatý.
- Hydroxid platnatý, Pt (OH)4, tetrahydroxid platiny.
- Vanadic hydroxid, V (OH)4, tetrahydroxid vanadu.
- Hydroxid železitý, Fe (OH)2dihydroxid železa.
- Hydroxid olovnatý, Pb (OH)4tetrahydroxid olovnatý.
- Hydroxid stříbrný, AgOH, hydroxid stříbrný.
- Hydroxid kobaltu, Co (OH)2, dihydroxid kobaltu.
- Hydroxid manganatý, Mn (OH)3, trihydroxid manganatý.
- Hydroxid železitý, Fe (OH)3, trihydroxid železitý.
- Hydroxid měďnatý, Cu (OH)2dihydroxid měďnatý.
- Hydroxid hlinitý, Al (OH)3, trihydroxid hlinitý.
- Hydroxid sodný, NaOH, hydroxid sodný.
- Hydroxid strontnatý, Sr (OH)2dihydroxid strontnatý.
- Hydroxid hořečnatý, Mg (OH)2dihydroxid hořečnatý.
- Hydroxid amonný, NH4OH, hydroxid amonný.
- Hydroxid kademnatý, Cd (OH)2, dihydroxid kademnatý.
- Hydroxid vanadičitý, V (OH)3, trihydrát vanadu.
- Hydroxid rtuťnatý, Hg (OH)2, dihydroxid rtuťnatý.
- Hydroxid měďný, CuOH, hydroxid měďnatý.
- Hydroxid lithný, LiOH, hydroxid lithný.
Hydroxidy někdy mají běžné názvy dáno jeho konvenčnějšími způsoby použití: hydroxid sodný se také nazývá louh sodný, hydroxid draselný žíravý potaš, hydroxid vápenatý nazývaný vápenná voda nebo hašené vápno a hydroxid hořečnatý nazývaný mléko magnézie.
Postupujte podle:



