20 Beispiele für Alkene
Verschiedenes / / July 04, 2021
Das Alkene Sie sind Verbindungen Kohlenstoff-Kohlenstoff-Doppelbindungen enthalten. Wenn diese Verbindungen offenkettige Strukturen aufweisen, reagieren sie auf die Summenformel CneinH2n (wo nein ist die Anzahl der Kohlenstoffatome). Alkene werden auch Olefine genannt und entsprechen der Gruppe der Kohlenwasserstoffe ungesättigt. Sie werden hauptsächlich im Rahmen des Ölcrackenprozesses und durch Dehydrierung von Alkanen gewonnen. Beispielsweise: Ethen, Propen, Cyclohexen.
Sie sind organische Verbindungen, die sein können kurze, mittlere oder lange Kette; es gibt auch cyclische Alkene oder Cycloalkene. Durch die Kohlenstoff-Kohlenstoff-Doppelbindung haben Alkene weniger Wasserstoff als alkane entsprechend mit gleicher Anzahl von Atome Kohlenstoff.
Wie werden Alkene benannt?
Um die Alkene zu benennen, Kohlenstoffkette die die meisten Kohlenstoffatome enthält und die auch die Doppelbindung enthält. Wenn diese Kette mehrere Doppelbindungen hat, werden sie nach der kleinstmöglichen Kombination der Positionen dieser Doppelbindungen benannt.
Die Position des Doppelbindung Es wird angezeigt, indem vor dem Suffix -no das lateinische Präfix eingefügt wird, das die Nummer des Kohlenstoffs angibt, an dem die Doppelbindung beginnt (di (2), tri (3), tetra (4), penta (5), octa (8), usw.). Substituenten (meist Chlor, Brom, Ethyl, Methyl usw.) werden als Präfixe (am Anfang des Namens) genannt, detailliert und in alphabetischer Reihenfolge werden sie auch nach der kleinstmöglichen Kombination ihrer Positionen in der benannt Kette. Beispielsweise: 1-Buten / 1,2-Butadien / 5-Chlor-1-penten / 4-Pentenylchlorid
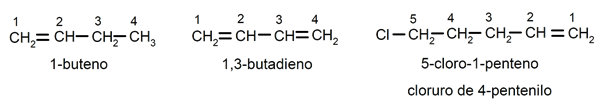
Angesichts der Komplexität des chemischen Namens, der gemäß der IUPAC-KriterienViele natürlich vorkommende organische Alkene haben ausgefallene Namen, die oft mit ihrer natürlichen Quelle zusammenhängen. Beispielsweise: Limonen / 1-Methyl-4-(1-methylethenyl)-cyclohexen / Geraniol / 3,7-Dimethyl-2,6-octadien-1-oldien
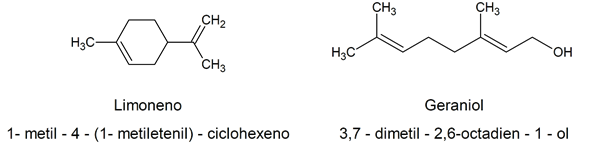
Alkene mit bis zu vier Kohlenstoffatomen sind Gase bei Raumtemperatur, solche mit 4 bis 18 Kohlenstoffe Sie sind Flüssigkeiten und die längsten sind solide. Sie lösen sich auf in Lösungsmittel organisch wie Ether oder Alkohol und sind etwas dichter als die entsprechenden Alkane (d. h. mit der gleichen Anzahl von Kohlenstoffatomen).
Der Punkt von Verschmelzung Ja Sieden von Alkenen, wie bei Alkanen, nimmt zu, je länger die Kohlenstoffkette ist.
Auf der anderen Seite aufgrund der von der Doppelbindung erzeugte Spannung, beträgt der Abstand zwischen den an der Doppelbindung beteiligten Kohlenstoffatomen im Alken 1.34 pm (Pikometer), während der Abstand der Einfachbindung im entsprechenden Alkan 1.54. beträgt Uhr
Sie präsentieren a chemische Reaktivität viel höher als Alkane, gerade weil sie diese Doppelbindungen haben, die eine Dichte haben Elektronik, die hoch ist und zusammenbrechen und die Anlagerung anderer Atome, oft Wasserstoff oder. zulassen kann Halogene. Sie können auch erleben Oxidation und Polymerisation.
Alkene sind normalerweise vorhanden cis-trans-Isomerie oder Stereoisomerie, da die durch die Doppelbindung verbundenen Kohlenstoffatome nicht rotieren können und sich die Substituenten dadurch auf der gleichen Seite der Doppelbindung oder auf gegenüberliegenden Seiten befinden. Beispielsweise: trans-2-Buten / cis-2-Buten
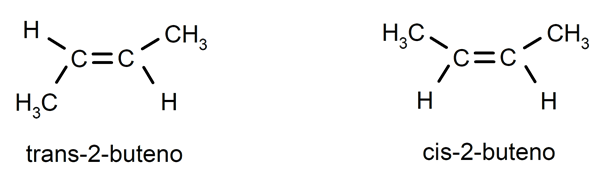
Alkene mit zwei Doppelbindungen werden Diene genannt, und solche mit mehr als zwei Doppelbindungen werden allgemein als Polyene bezeichnet.
In der Pflanzenwelt sind Alkene ziemlich reichlich vorhanden und haben physiologische Rollen von großer Bedeutung, wie die Regulierung des Fruchtreifeprozesses oder die Filterung bestimmter Sonneneinstrahlung.
Die chemische Struktur organischer Alkene ist normalerweise recht komplex und umfasst Kohlenstoffketten und -ringe. Einige Früchte (wie Karotten oder Tomaten) und einige Krebstiere (wie Krabben) produzieren erhebliche Mengen an Beta-Carotin, einem wichtigen Alken, das eine Vorstufe von Vitamin A ist.
Beispiele für Alkene
- Ethen
- 2-Methylpropen
- Propen
- 2,3-Butadien
- Myrcen
- Limonen
- Geraniol
- Lycopin
- Lanosterol
- mentofuran
- Tetrafluorethylen
- 1,3,5,7-Cyclooctatetraen
- 5-Brom-3-methyl-3-hexen
- 3,5-Diethyl-4-propyl-2,5-dimethyl-2-hepten
- 7,7,8-Trimethyl-3,5-nonadien
- 3,3-Diethyl-1,4-hexadien
- Cyclohexen
- 1-Chlor-2-methylprop-1-en
- 3-Brom-5-methyl-cyclopenten
- 1-Methyl-cyclohexen
Diagramme der chemischen Verbindungen dieser Alkene: