Lanthanoid-Eigenschaften
Chemie / / July 04, 2021
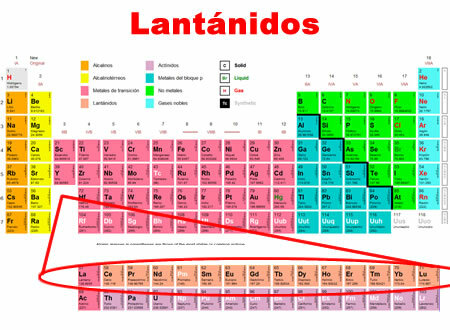
Lanthanide sind die chemischen Elemente, die von Lanthan bis Lutetium reichen. Sie haben gemeinsame Merkmale, für die sie am Ende des Periodensystems in eine spezielle Kategorie eingeordnet werden.
Hauptmerkmale von Lanthaniden:
- Sie liegen in der 6. Periode des Periodensystems.
- Sie decken 15 Elemente von 57 bis 71 ab.
- Sie teilen die Struktur von Lanthan, zu dem ein chemisch weniger reaktives Energieniveau f hinzugefügt wird.
- Sie wurden seltene Erden genannt, weil sie im natürlichen Zustand immer zu Oxiden verbunden sind.
- Einige sind relativ reichlich vorhanden.
- Obwohl sie variable Valenzen haben, haben die meisten Valenzen +3.
- Mit zunehmender Ordnungszahl nimmt sein Radius ab.
- Sie alle haben einen glänzenden Metallic-Look.
Individuelle Eigenschaften von Lanthaniden:
Lanthan (La).
- Ordnungszahl 57
- Atomgewicht: 139
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 920 °C
- Siedepunkt: 3457 ° C
Es wurde 1839 entdeckt. In der Industrie wird es in Legierungen mit anderen Lanthaniden zur Herstellung leichterer Steine verwendet; in der Optik wird es für optische Gläser verwendet. Es wird auch für Wasserstoffschwämme verwendet, die Gase enthalten. In der Medizin wird es in Form von Lanthancarbonat zur Behandlung von Nierenversagen verwendet, da es eine Affinität hat, sich mit Phosphaten zu vermischen und Hyperphosphämie zu reduzieren.
Cer (Ce)
- Ordnungszahl 58
- Atomgewicht: 140
- Zustand: Weicher Feststoff
- Aussehen: Metallisch, silbergrau, eisenähnlich
- Valencia: +3, +4
- Schmelzpunkt: 798 ° C
- Siedepunkt: 3426 ° C
Es wurde 1803 entdeckt. Es ist das am häufigsten vorkommende Lanthanoid. Es wird zur Herstellung von Katalysatoren, hauptsächlich für Automobile (Katalysatoren) und zum Ölcracken verwendet. In Oxidform wird es zum Polieren von Gläsern und Linsen verwendet. Obwohl keine biologischen Funktionen bekannt sind, wird es in der Medizin in Brandsalben verwendet.
Praseodym (Pr)
- Ordnungszahl 59
- Atomgewicht: 144
- Zustand: Weicher Feststoff
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 931 ° C
- Siedepunkt: 3520°C
Es wurde 1841 entdeckt und 1885 isoliert. In der Industrie wird es in Legierungen mit Magnesium zur Herstellung von Flugzeugtriebwerken verwendet; Es wird verwendet, um Glas und Emaille eine gelbe Farbe zu verleihen. Nickellegierungen haben magnetische Eigenschaften. Reagiert mit Halogenen unter Bildung von Fluoriden, Chloriden, Bromiden und Jodiden.
Neodym (Nd)
- Ordnungszahl 60
- Atomgewicht: 139
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1024 ° C
- Siedepunkt: 3100 ° C
Es wurde 1885 entdeckt, als Praseodym isoliert wurde; Neodym wurde bis 1925 isoliert. Es ist eines der reaktivsten Lanthanoide. In der Industrie wird es zum Einfärben von Glas und Emaille verwendet. Aufgrund seiner Fähigkeit, Licht zu absorbieren, wird es in der Astronomie zur Herstellung von Kristallen verwendet, mit denen Infrarotspektrometer und -filter kalibriert werden. Eine seiner Hauptanwendungen ist die Herstellung von Magneten mit hoher magnetischer Intensität. Diese Magnete werden für Präzisionsinstrumente, wie sie in Computerfestplatten verwendet werden, sowie für einige dünnformatige Lautsprecher verwendet.
Promethium (PM)
- Ordnungszahl 61
- Atomgewicht: 145
- Fester Zustand
- Aussehen: ?
- Valencia: +3
- Schmelzpunkt: 1100 ° C
- Siedepunkt: 3000 ° C
Seine Existenz wurde 1902 vorhergesagt, konnte aber erst 1944 nachgewiesen werden. Dieses Lanthanoid kommt in der Natur nicht vor, die Quelle seiner Gewinnung und Erforschung ist die Spaltung von Uran. Bei der Uranspaltung in einem Kernreaktor ist eines der Atome, die bei dieser Atomtrennung entstehen, das Promethium. Es hat radioaktive Eigenschaften, die ihm Phosphoreszenz verleihen, und wird für Kalibratoren und Nuklearbatterien in Raumfahrzeugen verwendet.
Samarium (Sm)
- Ordnungszahl 62
- Atomgewicht: 150
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1072 ° C
- Siedepunkt: 1803°C
Es wurde 1853 entdeckt und 1879 isoliert. Es hat mehrere Isotope, von denen mindestens zwei radioaktiv sind. In der Industrie wird es in der Optik verwendet, um Kristalle herzustellen, die Infrarotlicht absorbieren. Es wird auch als Katalysator zur Gewinnung von Alkohol und als Element in einigen Leuchtstofflampen und Fernsehern verwendet. Was die Gesundheit betrifft, kann es beim Einatmen (wie das Oxid zum Polieren von Kristallen) Lungenembolien verursachen oder die Leber beeinträchtigen. Radioaktive Isotope werden in der Strahlentherapie unheilbar kranker Patienten verwendet.
Europium (EU)
- Ordnungszahl 63
- Atomgewicht: 152
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +2, +3
- Schmelzpunkt: 826 ° C
- Siedepunkt: 1527 ° C
Es wurde 1890 entdeckt. Es ist das reaktivste der Lanthanoide. Es wurde in Leuchtstofflampen und Fernsehern verwendet, kann jedoch Lungenembolien verursachen, wenn es eingeatmet oder die Leber geschädigt, wenn es sich im menschlichen Körper anreichert, hat es fast keine industrielle Verwendung. In der Atomforschung wird es verwendet, da es Neutronen absorbiert.
Gadolinium (Gd)
- Ordnungszahl 64
- Atomgewicht: 157
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1312 ° C
- Siedepunkt: 3250 ° C
Gadolinium hat nur wenige Anwendungen, die wichtigste ist die magnetische industrielle Kühlung, da es seine magnetischen Eigenschaften bei niedrigen Temperaturen erhöht; Da diese Art von Kühlern jedoch die Verwendung von Arsen erfordert, werden sie nicht in der Haushaltskühlung verwendet. In der Medizin wird es als Kontrastmittel für die Kernspinresonanz verwendet.
Terbium (Tb)
- Ordnungszahl 65
- Atomgewicht: 159
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +4
- Schmelzpunkt: 1356 ° C
- Siedepunkt: 3230 ° C
Es wurde 1843 entdeckt und 1905 isoliert. Es ist sehr wichtig in der Elektronikindustrie, da es eines der Elemente ist, die zur Herstellung von Halbleitern verwendet werden. Andere Verwendungen sind die Herstellung von Leuchtstoffröhren und Bildröhren. Es wird auch als Katalysator in Brennstoffzellen verwendet. Obwohl es keine biologischen Funktionen hat, hat seine Inhalation oder das Eindringen in den menschlichen Körper toxische Wirkungen, die hauptsächlich die Leber betreffen.
Dysprosium (Dy)
- Ordnungszahl 66
- Atomgewicht: 162,5
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +2, +3
- Schmelzpunkt: 1407 ° C
- Siedepunkt: 2567 ° C
Es wurde 1843 entdeckt und 1905 isoliert. Es ist sehr wichtig in der Elektronikindustrie, da es eines der Elemente ist, die zur Herstellung von Halbleitern verwendet werden. Andere Verwendungen sind die Herstellung von Leuchtstoffröhren und Bildröhren. Es wird auch als Katalysator in Brennstoffzellen verwendet. Obwohl es keine biologischen Funktionen hat, hat seine Inhalation oder das Eindringen in den menschlichen Körper toxische Wirkungen, die hauptsächlich die Leber betreffen.
Holmium (Ho)
- Ordnungszahl 67
- Atomgewicht: 166
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1474 ° C
- Siedepunkt: 2700 ° C
Sie wurde 1878 entdeckt und ihr Name leitet sich von ihrer Entdeckungsstadt Stockholm ab, auf Latein Holmia. Es hat fast keinen praktischen Nutzen; es wird jedoch in einigen Industrien als Katalysator für chemische Reaktionen sowie für einige elektronische Komponenten verwendet. Es wird auch verwendet, um die Frequenz und Intensität des Laserstrahls zu ändern.
Erbium (Er)
- Ordnungszahl 68
- Atomgewicht: 167
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1795 ° C
- Siedepunkt: 2863 ° C
Es wurde 1843 entdeckt. Es wird in der Nuklearindustrie als Neutronenpuffer verwendet. In Oxidform ist es ein Farbstoff für Kristalle, der ihnen einen rosa Farbton verleiht; Diese Kristalle werden in Optik und Schmuck verwendet. Es wird auch zur Herstellung von Glasfasern verwendet.
Thulium (Tm)
- Ordnungszahl 69
- Atomgewicht: 167
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1545 ° C
- Siedepunkt: 1947 ° C
Es wurde 1879 entdeckt. Trotz seiner geringen Verfügbarkeit aufgrund seiner radioaktiven Eigenschaften wird es hauptsächlich als Röntgenquelle in tragbaren Geräten und für Festkörperlaser verwendet.
Ytterbium (Yb)
- Ordnungszahl 70
- Atomgewicht: 173
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 824 ° C
- Siedepunkt: 1194 ° C
Es wurde 1878 entdeckt und 1907 isoliert. Radioaktive Isotope werden für tragbare Röntgengeräte verwendet, die ohne Strom auskommen. Es wird auch verwendet, um Stahllegierungen zu verbessern und ihre Widerstandsfähigkeit zu erhöhen, eine Eigenschaft, die in der Zahnheilkunde aufgrund der Verbesserung der mechanischen Eigenschaften von Stahl verwendet wird. Es muss mit Vorsicht behandelt werden, da es Reizungen und Verbrennungen verursachen kann. Darüber hinaus kann es bei Reaktion mit Luft eine Explosion oder einen Brand verursachen.
Lutetium (Lu)
- Ordnungszahl 71
- Atomgewicht: 175
- Fester Zustand
- Aussehen: Metallic, silberweiß
- Valencia: +3
- Schmelzpunkt: 1652 ° C
- Siedepunkt: 3402 ° C
Es wurde 1907 entdeckt. Es ist das am seltensten vorkommende chemische Element in der Erdkruste. Trotz seiner geringen Verfügbarkeit wird es zur Ölraffination und als Katalysator für Reaktionen in der organischen Chemie verwendet. Einige radioaktive Isotope wurden auch für Strahlentherapiebehandlungen getestet.
