Beispiel für organische und anorganische Moleküle
Chemie / / July 04, 2021
Das Allgemeine Chemie Es ist die Wissenschaft, die studiert alle Arten von Materie, die es gibt, und ihre interne Änderungen Kontakt zwischen verschiedenen Arten davon haben.
Das Organische Chemie Es ist der Teil der Allgemeinen Chemie, der dazu bestimmt ist, die Materie zu untersuchen, deren Hauptbestandteil die Kohlenstoffelement, Na und es ist Teil lebender Organismen.
Das Anorganische Chemie Es ist der Teil der Allgemeinen Chemie, der für das Studium der sog "mineralische Materie", die Teil der Ich lebe nicht Umwelt.
Das Molekül ist die Vereinigung von verschiedene Atome verschiedener Elemente Chemikalien zu neuen Stoffen mit ihren besonderen Eigenschaften.
In der Allgemeinen Chemie, Elemente Sind die reine Stoffe die gebildet werden durch Atome eines einzigen Typs. Die Elemente werden in das Periodensystem der chemischen Elemente eingeordnet.
Genau wie er Atom ist die Grundeinheit der Elemente, das Molekül ist die Haupteinheit von Verbindungen, das sind Stoffe, die ein charakteristisches chemisches Verhalten haben.
Das Verbindungen kann als Folge von. gebildet werden Naturphänomen, oder in Laboren erstellt werden oder in Industrieanlagen, Moleküle sind also überall vorhanden. Die Moleküle befinden sich in Mineralien, in Baumblättern, in Lebensmitteln, in Medikamenten, im Wasser, das wir trinken, in der Luft, die wir atmen, und sogar in der Umweltverschmutzung.
Allgemeine Chemie ist hauptsächlich unterteilt in Anorganische Chemie Ja Chemischzu OrganisationneinicaDaher können Moleküle auch als Anorganisch und Organisch klassifiziert werden.
Anorganische Moleküle
In der Anorganischen Chemie werden Moleküle hauptsächlich durch die Kombination von Atomen positiver Valenzen mit anderen negativer Valenzen, in ionischen Bindungen. Diese Bindungen werden hauptsächlich durch die elektromagnetischen Kräfte zwischen den Atomen gebildet, die durch die Anwesenheit von Valenzelektronen erzeugt werden.
So entstehen alle ionischen Verbindungen, wie Salze, Oxisalte, Säuren, Oxysäuren, Oxide und Hydroxide.
Anorganische Moleküle als Elektrolyte
Die Haupteigenschaft ionischer Moleküle besteht darin, dass bei Kontakt mit Wasser H2ODER, sie sind in zwei Teile getrennt: positiv und negativ. Diese beiden Teile, elektrisch geladene Atome oder Atomgruppen, sind im Wasser dispergiert. An die anorganische Substanz, die sich so in Wasser trennen kann, es heißt Elektrolyt.
Die von Wasser und positiv und negativ geladenen Teilchen gebildete Lösung heißt "Elektrolytische Lösung". Diese Art von Lösung ist in der Lage, elektrische Ströme zu leiten, weshalb sie in elektrochemischen Zellen wie Autobatterien verwendet wird.
Anorganische Säure und alkalische Moleküle
Bei anorganischen Molekülen wie Säuren, das Oxysäuren und der Hydroxide, während sie sich gleichzeitig in einen positiven und einen negativen Teil trennen, tragen sie zur Lösung bei, eine Eigenschaft namens Wasserstoffpotential, gemessen als negativer Logarithmus der Wasserstoffionenkonzentration.
Das Wasserstoffpotential (pH) bestimmt, wie stark die Lösung sauer ist. Auf der pH-Skala, die von einem Wert von 1 für maximale Säure bis 14 reicht, was für vollständige Alkalität oder Basizität steht, reicht der Säurecharakter von Werten von 1 bis 6 und der alkalische Wert liegt zwischen 8 und 14. 7 stellt einen neutralen pH dar; weder sauer noch basisch. Das Ergebnis des negativen Logarithmus der H + -Konzentration wird uns sagen, wo wir auf der Skala stehen.
Beispiele für Säuren:
Salzsäure: HCl: H+ + Cl-
Bromwasserstoffsäure: HBr: H+ + Br-
Schwefelsäure: H2S: 2H+ + S-2
Cyanwasserstoffsäure: HCN: H+ + CN-
Salzsäure: HI: H+ + ich-
Beispiele für Oxysäuren:
Schwefelsäure: H2SW4: 2H+ + SO4-2
Kohlensäure: H2CO3: 2H+ + CO3-2
Salpetersäure: HNO3: H+ + NEIN3-
Phosphorsäure: H3Bestellung4: 3H+ + PO4-3
Perchlorsäure: HClO4: H+ + ClO4-
Beispiele für Hydroxide:
Natriumhydroxid: NaOH: Na+ + OH-
Calciumhydroxid: Ca (OH)2: Ca+ + 2OH-
Ammoniumhydroxid: NH4OH: NH4+ + OH-
Kaliumhydroxid: KOH: K+ + OH-
Magnesiumhydroxid: Mg (OH)2: Mg+ + 2OH-
Anorganische Moleküle in chemischen Reaktionen
Wenn anorganische Moleküle an einer chemischen Reaktion teilnehmen, kann es vier grundlegende und einfache Reaktionsmechanismen geben: Synthese, Zersetzung, einfache Substitution und Doppelsubstitution. Hier ist jeweils ein Beispiel:
Synthese
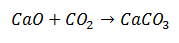
Eine Synthesereaktion ist eine Reaktion, bei der zwei Moleküle kommen zu einem Endprodukt zusammen, das aus einem einzigen Molekül besteht. Im Beispiel ist es der Fall, dass sich Calciumoxid mit Kohlendioxid verbindet, um ein Calciumcarbonat-Molekül zu bilden.
Zersetzung:

Eine Zersetzungsreaktion ist eine, bei der ein anfängliches Molekül trennt sich in zwei neue stabile Moleküle. Dies ist der Fall von Calciumhydroxid, das sich in ein Molekül Calciumoxid und ein weiteres Wassermolekül aufspaltet.
Einfache Ersetzung:

In einer einfachen Substitutionsreaktion ein Atom eines Elements wird mit einem der Atome eines Moleküls ausgetauscht. Dies ist der Fall von metallischem Zink, das sich an die Stelle von Wasserstoff in Chlorwasserstoff stellt, es freisetzt und Zinkchloridmoleküle bildet.
Doppelsubstitution:
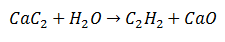
Bei einer Doppelsubstitutionsreaktion bestimmte Atome zweier Ausgangsmoleküle werden ausgetauscht, um zwei verschiedene Moleküle als Produkte zu erzeugen. Dies ist der Fall von Calciumcarbid, bei dem Kohlenstoff freigesetzt wird, der sich mit Wasserstoff aus Wasser zu Acetylen verbindet. Calcium bindet sich an Sauerstoff, um als zweites Produkt Calciumoxid zu bilden.
Organische Moleküle
Organische Chemie ist Kohlenstoffchemie, was bedeutet, dass alle organischen Moleküle dieses Element in unterschiedlichen strukturellen Anordnungen aufweisen.
Organische Moleküle sind gekennzeichnet durch ständige Präsenz kovalenter Bindungen. Kovalente Bindungen mit denen, in denen zwei Atome schließen sich zusammen, um ihre Valenzelektronen zu teilen und so ihre Oktette gegenseitig zu vervollständigen.
Dies ist bei Kohlenstoff der Fall, der an andere Atome desselben Elements bindet. Es entstehen Ketten unterschiedlichster Länge, von zwei bis sechzig Kohlenstoffatomen, und selbst diese Ketten sie verzweigen sich mit anderen Ketten gleicher Länge, wodurch eine immense Vielfalt an Molekülen erreicht wird organisch.
Auch ionische Bindungen sind vorhanden, diese treten jedoch in Zwischenschritten langer Reaktionsmechanismen auf, in denen ein gewünschtes Molekül gebildet wird.
Zu den einfachsten organischen Molekülen gehören Kohlenstoff und Wasserstoff. Letzteres vervollständigt die Kohlenstoffvalenz, die es erfordert.
In der organischen Chemie können Moleküle linear oder aliphatisch, verzweigt, cyclisch und aromatisch sein.
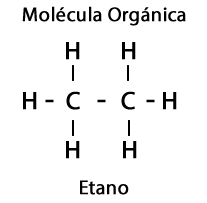
Darüber hinaus sind in den organischen Molekülen die Elemente Sauerstoff, Stickstoff, Schwefel und Phosphor beteiligt, wodurch eine beeindruckende Vielfalt an funktionellen Gruppen für die Moleküle entsteht.
Funktionelle Gruppen in organischen Molekülen
Das Funktionelle Gruppen sind Gruppen aus zwei oder mehr Atomen, die beim Verbinden einer Kohlenstoff-Wasserstoff-Kette unterschiedliche chemische Spezies mit einem bestimmten Verhalten bilden. Als nächstes werden die sieben Haupttypen organischer Moleküle mit ihren jeweiligen funktionellen Gruppen aufgelistet. Der Buchstabe "R" wird verwendet, um die Kohlenstoff-Wasserstoff-Kette zu bezeichnen.
Alkylhalogenide - Form: R-X / Funktionelle Gruppe: A Halogenelement (Chlor, Brom, Jod)

Alkohole - Form: R-OH / Funktionelle Gruppe: -OH oder Hydroxyl.
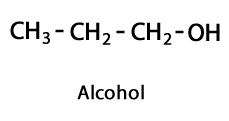
Aldehyde - Form: R-CHO / Funktionsgruppe: -CHO, die immer bis zum Ende der Kette geht.
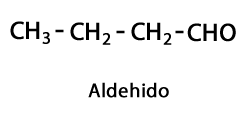
Ketone - Form: R-CO-R / Funktionelle Gruppe: -CO- oder Carboxy, immer im mittleren Kohlenstoff der Kette.
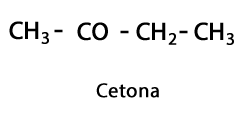
Organische Säuren - Form: R-COOH / Funktionelle Gruppe: -COOH oder Carboxyl, immer am Ende der Kette.
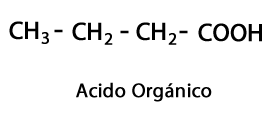
Säureester - Form: R-COO-R / Funktionelle Gruppe: -COO-, ist das Ergebnis der Verbindung einer Säurekette mit einer anderen Kohlenstoff-Wasserstoff-Kette.
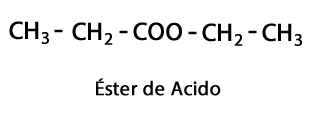
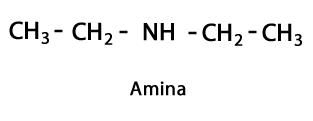
Amine - Form: R-NH2, R-NH-R, R-N-2R / Funktionelle Gruppe: -NH2, -NH-, -N = oder Amino, das ist ein mit Wasserstoff ergänzter Stickstoff an den Stellen, an denen keine Kohlenstoff-Wasserstoff-Kette vorhanden ist. Wie gesagt, kann es am Ende der Kette oder in der Mitte gehen. Das Stickstoffatom kann von einer, zwei oder drei organischen Ketten begleitet werden, um ein endgültiges Molekül zu bilden. Amine können als organische Derivate von Ammoniak NH. angesehen werden3.
Organische Moleküle in chemischen Reaktionen
Organische Moleküle, je länger ihre Kohlenstoff-Wasserstoff-Ketten, desto mehr Stellen oder Atome stehen zur Verfügung, um an einer chemischen Reaktion teilzunehmen.
Meistens werden Elemente oder Ketten an einen der vorhandenen Kohlenstoffe angefügt oder ein Teil der Hauptkette wird abgelöst, um eine andere organische Verbindung zu erzeugen.
Da solche Reaktionen langsam sind, werden Katalysatoren verwendet, die chemische Mittel sind, um die Reaktionen zu beschleunigen. In einigen Fällen ist der Katalysator ein feines Netz aus Platinmetall.
Beispiele für anorganische Moleküle
Natriumchlorid NaCl
Kaliumchlorid KCl
Ammoniumchlorid NH4Cl
Natriumnitrat NaNO3
Kaliumnitrat KNO3
Ammoniumnitrat NH4NICHT3
Schwefelsäure H2SW4
Phosphorsäure H3Bestellung4
Phosphorsäure H3Bestellung3
Salzsäure HCl
Jodsäure HI
Natriumhydroxid NaOH
Kaliumhydroxid KOH
Ammoniumhydroxid NH4Oh
Calciumhydroxid Ca (OH)2
Magnesiumhydroxid Mg (OH)2
Eisenhydroxid Fe (OH)2
Eisen(III)-hydroxid Fe (OH)3
Eisensulfid FeS
Eisensulfat FeSO4
Eisensulfat Fe2(SW4)3
Beispiele für organische Moleküle
Glukose C6H12ODER6
Methan CH4
Ethan C2H6
Acetylen C2H2
Propan C3H8
Butan C4H10
Ethanol C2H6ODER
Saccharose C12H22ODER11
Methanol CH4ODER
Glycerin C3H8ODER3



