20 Παραδείγματα χημικών βάσεων
Miscellanea / / July 04, 2021
Ονομάζεται χημική βάση σε όλες τις ουσίες που, όταν διαλύονται σε νερό, απελευθερώνουν ιόντα υδροξυλίου (ΟΗ–). Για παράδειγμα: υδροξείδιο του ασβεστίου, υδροξείδιο του χαλκού, υδροξείδιο του ψευδαργύρου.
Οι χημικές βάσεις είναι επίσης γνωστές ως αλκαλίο, διότι διαχωρίζοντας και απελευθερώνοντας τις ομάδες υδροξυλίου (ΟΗ–), ο pH των διαλυμάτων αυξάνεται, δηλαδή, το διάλυμα γίνεται αλκαλικό. Αυτό είναι αντίθετο με αυτό που συμβαίνει όταν οξύ, επειδή σε αυτή την περίπτωση το pH μειώνεται και το διάλυμα γίνεται όξινο.
Οι βάσεις έχουν ένα πικρή γέυση χαρακτηριστικό γνώρισμα. Μετά το δικό του διάλυση, οι προκύπτουσες λύσεις μεταφέρουν το ηλεκτρικό ρεύμα (λόγω της παρουσίας ιόντων) και συνήθως είναι καυστικά και ερεθιστικά για το δέρμα και άλλους ανθρώπινους και ζωικούς ιστούς.
Οι βάσεις εξουδετερώνει τα οξέα, συχνά σχηματίζονται βγες έξω. Τα αλκαλικά διαλύματα τείνουν να αισθάνονται ολισθηρά ή σαπούνια. Αυτό συμβαίνει επειδή παράγουν αμέσως τη σαπωνοποίηση του λίπη παρόν στην επιφάνεια του δέρματος.
Στην περίπτωση των υδροξειδίων τους διαλυτότητα εξαρτάται από μέταλλο: αυτά της ομάδας (Ι) είναι τα πιο διαλυτά στο νερό, από την άλλη πλευρά, τα υδροξείδια των στοιχείων με Ο βαθμός οξείδωσης (II) είναι λιγότερο διαλυτός και ο βαθμός οξείδωσης (III) ή (IV) είναι σχεδόν αδιάλυτος. Αμίνες και βάσεις νουκλεϊκά οξέα είναι οι πιο διαδεδομένες βάσεις μεταξύ των οργανικών.
Θεωρίες που καθορίζουν τις βάσεις
Υπάρχουν διαφορετικές θεωρίες για τον καθορισμό των χημικών βάσεων:
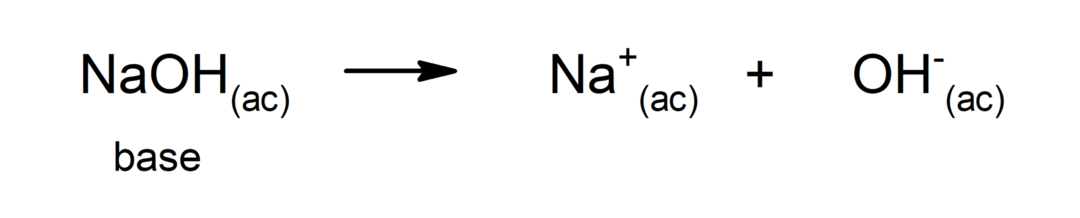
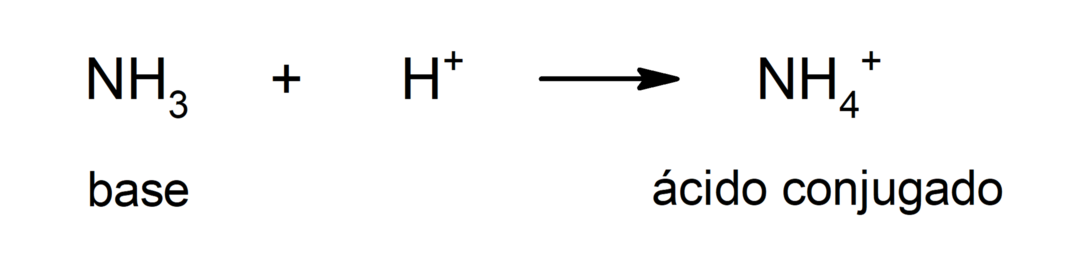

Έτσι, το OH ιόν–δωρίζει το μη συνδεδεμένο ζεύγος ηλεκτρονίων του στο Η+για να σχηματίσετε έναν συντεταγμένο ή έναν εγγενή δεσμό (είναι ένας τύπος ομοιοπολικό δεσμό όπου μόνο ένα από τα άτομα που σχηματίζει τον δεσμό παρέχει το ζεύγος ηλεκτρονίων) μέσω του οποίου σχηματίζεται το μόριο νερού.
Χρήσεις των βάσεων
ο υδροξείδιο του νατρίου Χρησιμοποιείται ευρέως στο βιομηχανία: είναι η λεγόμενη καυστική σόδα. Στην κατασκευή σαπουνιού, λίπη ζώα ή λαχανικά, τα οποία βράζονται με υδροξείδιο σχηματίζεται νάτριο και έτσι στεατικό νάτριο.
Το υδροξείδιο του νατρίου χρησιμοποιείται επίσης στην κατασκευή καθαριστικών φούρνων, στην κατασκευή χαρτοπολτού και σε ορισμένα οικιακά καθαριστικά. Μια άλλη ευρέως χρησιμοποιούμενη βάση είναι το υδροξείδιο του ασβεστίου, το οποίο είναι ο ασβέστης που χρησιμοποιείται στην κατασκευή.
Παραδείγματα χημικών βάσεων
- Υδροξείδιο του ασβεστίου - Ca (OH) ₂
- Υδροξείδιο του καλίου - ΚΟΚ
- Υδροξείδιο του βαρίου - Ba (OH) ₂
- Υδροξείδιο του μαγνησίου - Mg (OH) ₂
- Αμμωνία - NH₃
- Υδροξείδιο χαλκού (II) - Cu (OH) ₂
- Υδροξείδιο του σιδήρου (II) - Fe (OH) ₂
- Υδροξείδιο αλουμινίου - AI (OH) ₃
- Υδροξείδιο του ψευδαργύρου - Zn (OH) ₂
- Υδροξείδιο του νατρίου - NaOH
- Υδροξείδιο του νικελίου (II) - Ni (OH) ₂
- Απορρυπαντικό σαπούνι