Παράδειγμα οργανικής χημείας
Χημεία / / July 04, 2021
ο Οργανική χημεία Είναι το τμήμα της Γενικής Χημείας που είναι υπεύθυνο για τη μελέτη και τη λειτουργική ταξινόμηση των χημικών ενώσεων των οποίων το δομικό στοιχείο είναι Ανθρακας, υπάρχει σε αφθονία στο ζωντανή ύλη; Αυτό δημιουργεί ένα πολύ διαφοροποιημένο σύμπαν Ανόργανης Χημείας, αφιερωμένο σε χημικές ενώσεις που ταξινομούνται ως μέταλλα.
Το άτομο άνθρακα έχει τέσσερα ηλεκτρόνια στο τελευταίο κέλυφος της ηλεκτρονικής του διαμόρφωσης. Αυτό το χαρακτηριστικό, μαζί με αυτό της ατομικής του ακτίνας, του επιτρέπει να συνδέεται με ομοιοπολικούς δεσμούς με άλλους άτομα του ίδιου στοιχείου, σε πολλές αλυσίδες, σχηματίζοντας μεγάλη ποικιλία χημικών ενώσεων σταθερός.
Μπορείς να ελέγξεις Ομοιοπολικούς δεσμούς.
Τέτοιες χημικές ενώσεις, εκτός από τα άτομα άνθρακα που τους δίνουν την αρχέγονη δομή τους, περιέχουν άτομα υδρογόνου ως το κύριο συμπλήρωμα του σθένους άνθρακα. Επιπλέον, σε αυτήν την ποικιλομορφία των ενώσεων, υπάρχουν αυτές με την παρέμβαση ατόμων οξυγόνου, Στοιχεία αζώτου, αλογόνων, θείου και ακόμη και φωσφόρου, αλκαλικών και αλκαλικών γαιών και μετάλλων μετάβαση. Ανάλογα με το ποιος εμπλέκεται στο μόριο, θα είναι οι φυσικές και χημικές ιδιότητες της τελικής ουσίας.
ο ΟΡΓΑΝΙΚΕΣ ΕΝΩΣΕΙΣ είναι παρόντες σε όλη τη διάρκεια ζωντανή ύλη; προωθήστε και διατηρήστε όλους βιολογικές λειτουργίες, σε αντίθεση με τις ανόργανες ή ανόργανες ουσίες, που έχουν χρησιμοποιηθεί από τον άνθρωπο για εμπορικούς σκοπούς, για πειραματισμούς ή για την εκπλήρωση ορισμένων οικιακών εργασιών.
Ιστορία Οργανικής Χημείας
Πριν από το 1828, η διάκριση έγινε ήδη μεταξύ της Οργανικής Χημείας και της Ανόργανης Χημείας. Η οργανική ύλη συσχετίστηκε με μια δημιουργία μέσω ενός "ζωτική δύναμη", και στα ανόργανα με τα μη ζωντανά, με το ορυκτό. Δεδομένων αυτών των αντιλήψεων, δεν θα περίμενε κανείς να λάβει οργανικές ενώσεις από ανόργανα υλικά στο εργαστήριο.
Ωστόσο, το 1828 Friedrich Wöhler (1800-1882) κατάφερε να προετοιμάσει μια οργανική ουσία, Urea CO (ΝΗ2)2, ένα σημαντικό προϊόν του μεταβολισμού των ζώων, από ανόργανες ενώσεις. Θεραπευτική αγωγή Μόλυβδος Cyanate Pb (CNO)2 με Ammonia NH3 να πάρω Ammonium Cyanate NH4CNO; Αυτή η ένωση σχηματίστηκε, όντως, αλλά όταν το διάλυμα έβρασε για κρυστάλλωση του κυανικού αμμωνίου, μετατράπηκε σε ουρία.
Αυτή η χημική αλλαγή είναι ένα παράδειγμα Εσωτερική ομαδοποίηση, στην οποία ο αριθμός ή η κατηγορία ατόμων στο μόριο δεν αλλάζει, αλλά μόνο η σειρά τους μέσα σε αυτό. Αυτοί οι τύποι μετασχηματισμών είναι πολύ συνηθισμένοι στην οργανική χημεία.
Η ανακάλυψη του Wöhler ξεκίνησε την εγκατάλειψη της θεωρίας της ζωτικής δύναμης, αργότερα απορρίφθηκε πλήρως ακολουθούμενο από την παρασκευή πολλών άλλων οργανικών ενώσεων στο εργαστήριο. Παρ 'όλα αυτά, οι προσδιοριστές ανόργανων και οργανικών υφίστανται, καθώς οι ανόργανες ενώσεις σχετίζονται με ορυκτά προϊόντα και οι οργανικές ενώσεις, οι οποίες είναι στην πραγματικότητα ενώσεις άνθρακα και υδρογόνου και τα παράγωγά τους, είναι του τύπου που παράγεται από ζωντανούς οργανισμούς.
Παρόλο που οι νόμοι της γενικής χημείας ισχύουν εξίσου και για τις δύο ενώσεις, διάφορες αιτίες δικαιολογούν και καθιστούν απαραίτητη αυτήν τη διαίρεση. Έτσι, οι οργανικές και ανόργανες ενώσεις διαφέρουν σε διαφορετικές ιδιότητες, όπως: αυτές Διαλυτότητα προτιμάται σε οργανικούς διαλύτες (αιθέρας, αλκοόλη, χλωροφόρμιο, κ.λπ.) και σε νερό, αντίστοιχα, του Σταθερότητα (οργανικές ενώσεις αποσυντίθενται σε σχετικά χαμηλές θερμοκρασίες), και Φύση των αντιδράσεων; για τις ανόργανες ενώσεις είναι ιονικές, απλές και πρακτικά στιγμιαίες, και για τις οργανικές ενώσεις είναι ομοιοπολικές, πολύπλοκες και αργές.
ΟΡΓΑΝΙΚΕΣ ΕΝΩΣΕΙΣ
Είναι γνωστές ενώσεις άνθρακα με αλυσίδες έως ενενήντα ατόμων. ο αλυσίδες Τα άτομα άνθρακα μπορεί να είναι γραμμική και διακλαδισμένη και έχουν απλούς ομοιοπολικούς δεσμούς ή έχουν διπλούς ή τριπλούς δεσμούς. Περισσότερες από 2.500 ενώσεις είναι γνωστό ότι περιέχουν μόνο άνθρακα και υδρογόνο (Υδρογονάνθρακες).
Ισομερισμός οργανικών ενώσεων
Σε ανόργανες ενώσεις, ένας τύπος γενικά αντιπροσωπεύει μία μόνο ένωση. Έτσι, υπάρχει μόνο μία ουσία του τύπου Η2ΝΔ4. Το μόριο θειικού οξέος περιέχει δύο άτομα υδρογόνου, ένα από το θείο και τέσσερα οξυγόνο, σε μια συγκεκριμένη και μοναδική διάταξη. Στις οργανικές ενώσεις είναι σπάνια για να συμβεί αυτό. Έτσι, για παράδειγμα, υπάρχουν δύο ενώσεις που ανταποκρίνονται στον τύπο Γ2Η6Ή, αιθυλική αλκοόλη ή αιθανόλη και διμεθυλαιθέρας.

Όσο πιο περίπλοκο είναι το μόριο, δηλαδή, όσο μεγαλύτερος είναι ο αριθμός των ατόμων άνθρακα, τόσο μεγαλύτερος είναι ο αριθμός των πιθανών ισομερών.
Ανάλυση οργανικής ένωσης
Η ανάλυση μιας οργανικής ένωσης περιλαμβάνει το ποιοτική ανάλυση, ο ποσοτική ανάλυση και το Λειτουργική ανάλυση. Στην περίπτωση που υποθέτουμε ότι η ένωση είναι σε ακάθαρτη κατάσταση, έχει προηγουμένως καθαριστεί από Αποκρυστάλλωση, Απόσταξη, Εξάχνιση, Εξαγωγή, και τα λοιπά. Το κριτήριο καθαρότητας μπορεί να κριθεί με βάση τις φυσικές του σταθερές, όπως σημείο τήξης, σημείο βρασμού, πυκνότητα, διαλυτότητα, κρυσταλλική μορφή, δείκτης διάθλασης κ.λπ.
ο ποιοτική ανάλυση Επαληθεύεται με τη διερεύνηση της παρουσίας των στοιχείων που απαρτίζουν την ένωση, ιδίως άνθρακα, υδρογόνο και άζωτο, και μερικές φορές αλογόνα, θείο και φωσφόρο.
ο ποσοτική ανάλυση Πραγματοποιείται με βάση τις μεθόδους που χρησιμοποιούνται για ποιοτική ανάλυση. Το σημείο εκκίνησης είναι μια ορισμένη ποσότητα ουσίας που υφίσταται καύση και το διοξείδιο του άνθρακα συλλέγεται και ζυγίζεται. άνθρακας και υδρατμοί που σχηματίζονται για τον υπολογισμό του ποσοστού άνθρακα και υδρογόνου στο χημική ένωση. Τα αποτελέσματα της ποσοτικής ανάλυσης διευκολύνουν τον υπολογισμό του συνοπτικός τύπος, αν και ο μοριακός τύπος μπορεί να βρεθεί μόνο μετά τον προσδιορισμό του μοριακού βάρους της ουσίας. Αλλά το πρόβλημα δεν έχει ακόμη λυθεί, επειδή ο ίδιος μοριακός τύπος μπορεί να αντιστοιχεί σε διαφορετικά ισομερή.
Ταξινόμηση οργανικών ενώσεων
Σύμφωνα με τη δομή τους, οι οργανικές ενώσεις χωρίζονται σε ενώσεις αλιφατικός, αρωματικός Γ ετεροκυκλικό. Οι αλειφατικές ενώσεις σχετίζονται με το μεθάνιο CH4, είναι ανοιχτή αλυσίδα, εκτός από τις κυκλοπαραφίνες, και οφείλουν το όνομά τους στο γεγονός ότι τα ζωικά και φυτικά λίπη ανήκουν σε αυτήν την ομάδα.
ο αρωματικές ενώσεις, κλειστή αλυσίδα, που σχετίζεται στενά με το βενζόλιο, C6Η6, και οφείλουν το όνομά τους στο γεγονός ότι πολλά από αυτά έχουν αρωματικές, ευχάριστες μυρωδιές.
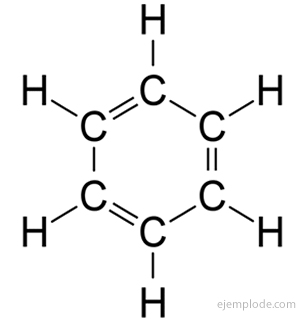
Δαχτυλίδι βενζολίου
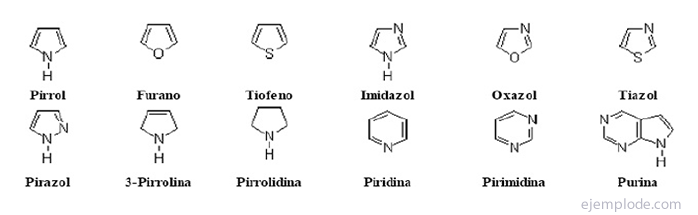
ο ετεροκυκλικές ενώσεις Είναι ενώσεις κλειστής αλυσίδας στις οποίες υπάρχει ένα στοιχείο διαφορετικό από τον άνθρακα στον δακτύλιο.
Από το σύνταγμά τους, είναι:
Υδρογονάνθρακες, το οποίο με τη σειρά του, λόγω του τύπου των συνδέσμων που έχει, ταξινομείται ως Αλκάνια, Αλκένια Γ Αλκίνες. Επιπλέον, τα κυκλοαλκάνια, το βενζόλιο και τα παράγωγά τους που αποτελούνται μόνο από άνθρακα και υδρογόνο βρίσκονται σε αυτήν την κατηγορία.
Ετεροκυκλικές ενώσεις
Αλογονωμένα παράγωγα:R-Χ
Νιτρο ενώσεις:R-ΟΧΙ2
Σουλφονικά οξέα:R-SO3Η
Νιτρίλια (Ή αλκυλοκυανίδια) και Ιονιτρίλια:R-CN και R-NC. Διαφέρουν ως προς το πώς συνδέεται το άτομο αζώτου στο μόριο.
Αλκοόλ:Ρ-ΟΗ
Φαινόλες: Ενώσεις βασισμένες σε ραχοκοκαλιά που αποτελείται από δακτύλιο βενζολίου με προστιθέμενη υδροξυλομάδα.

Αιθέρες:R-O-R
Mercaptans: R-SH
Θειοαιθέρες:R-S-R
Θειοοξέα:R-COSH
Αλδεϋδες:R-CHO
Κετόνες:R-CO-R
Καρβοξυλικά οξέα:R-COOH
Βγες έξω:R-COOM (M για μέταλλο)
Εστέρες: R-COO-R
Ανυδρίτες: R-CO-O-OC-R
Αμίνες:R-ΝΗ2, R-NH-R, 2R-N-R
Υδατάνθρακες τύπου Aldosa:-CHOH-CHOH-CHO
Υδατάνθρακες τύπου κετόζης:-CHOH-CO-CH2Ω
Οργανομεταλλικές ενώσεις:R-M-R
Αλογονίδια μετάλλου-αλκυλίου:R-MX (επίσης γνωστό ως αντιδραστήρια Grignard)


