Heterotsükliliste ühendite näide
Keemia / / July 04, 2021
On tsüklilisi keemilisi ühendeid, mis koosnevad ainult süsinikuaatomitest, nende valentsidega on täiendatud vesiniku aatomid. Selliseid ühendeid nimetatakse homotsükliline. A heterotsükliline ühend See on orgaaniline aine, mis sisaldab rohkem kui ühte tüüpi aatomitest moodustunud ringi; Peale süsiniku on levinumad lämmastik, hapnik ja väävel. Neid erinevaid aatomeid nimetatakse heteroaatomid.
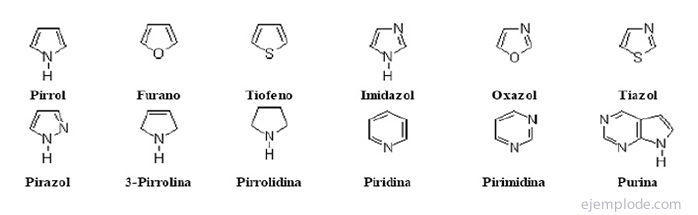
Eespool nimetatud ühendeid nimetatakse triviaalseteks nimedeks, see tähendab kaubanimedeks, mis ei paku molekuli kohta struktuurset teavet, kuid mille IUPAC on aktsepteerinud ja tunnustanud.
Heterotsükliliste ühendite klassifikatsioon
Heterotsüklilised ühendid klassifitseeritakse kahe peamise kriteeriumi järgi: Linkide tüüp mis sisaldab (kui need on ühe- või kahekordsed) ja Sõrmuste arv sellel on.
Tema jaoks Linkide tüüp need sisaldavad, on liigitatud Alitsüklilised ühendid, kui selle sidemed on üksikud või kahekordsed, kuid geomeetrias on kuni 5 aatomit; Y Aromaatsed ühendid, kui neil on rõngas Benseen selle struktuuris või mis on heteroaatomi olemasolu aluseks.
Tema jaoks Sõrmuste arv mida ta omab, saab selle liigitada Monotsükliline, Bitsükliline, Tritsüklilineja vajaduse korral lisatakse järjestikune numbriline eesliide.
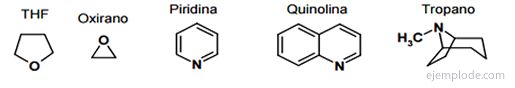
Kolme aatomi heterotsüklilised ühendid
Seal on kolm aatomit sisaldavaid heterotsüklilisi tsükleid, mis on nukleofiilide avamise lihtsuse tõttu väga reaktiivsed, neid nimetatakse epoksiidideks ja asiridiinideks. Need on orgaanilise sünteesi väärtuslikud lähteained.
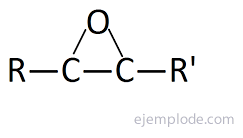
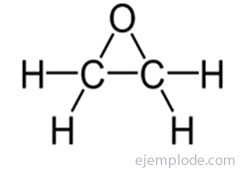
The Epoksiidid, mida nimetatakse ka oksüraanideks, on tsüklilised eetrid, mis koosnevad hapniku aatomi ühendamisest kahel järjestikusel süsinikul, mis omakorda moodustavad osa kovalentsete sidemete ahelast. See on kolmnurkne struktuur, mille alus on süsinik ja tipp hapnik. Need on värvusetud vedelikud, lahustuvad alkoholides, eetrites ja benseenis. Lihtsaim termin on Etüleenoksiid, nimetatud ka Epoksüetaan või Oxirano. Selle süntees toimub sagedamini süsinikuaatomite vahelise kaksiksideme purunemise kaudu hapnikku sisaldavate hapnike vahel. Neid nimetatakse hapniku aatomi kinnituskohtade tähistamiseks, millele järgneb eesliide "Epoksü-" ja seda toetava süsivesiniku nimi.
Polümeerides esinevate materjalidena kasutatakse neid struktuuride, katete ja liimide plastikuna. Lisaks on neil oluline osa abrasiivide, hõõrdematerjalide valmistamisel, tekstiilitööstuses, malmis, filtrites ja lakkides. Samuti mineraalvilla, immutuste, puitmaterjalide, vahtude, vormimispulbrite jaoks. Toiduainetööstuses kasutatakse epoksiide keemiliste sterilantidena madala niiskusesisaldusega toiduainetes ja aseptilistes pakkematerjalides.
The AsiridiinidLisaks epoksiididele on neil kolmnurkne struktuur, ainult et heteroaatom on lämmastik. Need on värvusetud vedelikud, vees lahustuvad, mürgised ja ammoniaagilõhnaga. Neil on eriline füüsiline omadus, mis omistatakse rõnga geomeetriale; lämmastikuaatomil on oluliselt suurem takistus püramiidi inversioonil kui teistel monotsüklilistel ja atsüklilistel amiinidel. Asiridiini sünteesi kasulik meetod on 1,2,3-triasoliinide pürolüüs või fotolüüs. Neid ühendeid saab hõlpsasti valmistada, reageerides atsiidid alkeenidega 1,3-dipolaarse tsüklilahendusreaktsioonina.
Aurustumisel võib asiridiin jõuda 20 ° C juures õhus kahjuliku kontsentratsioonini. Reageerib oksüdeerivate ainetega ja on altid põlemisele, tekitades lämmastikoksiide.

Viie aatomi heterotsüklilised ühendid
Viie aatomiga heterotsüklilised ühendid on kõige lihtsamad: Pürrool, lämmastiku heteroaatomiga, Furan, Heteroatomi hapnik ja Tiofeen, Väävli heteroaatom.
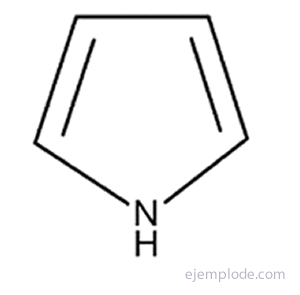
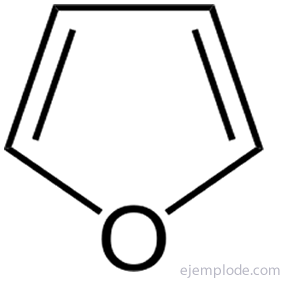
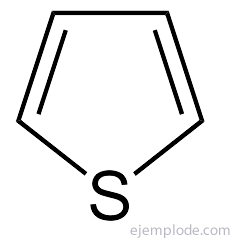
Pürroolitsükkel on porfüriinisüsteemi põhiüksus, mida leidub näiteks klorofüllis ja hemoglobiinis.
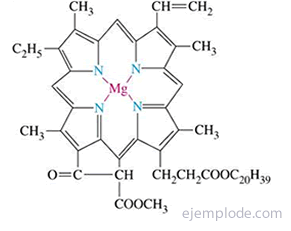
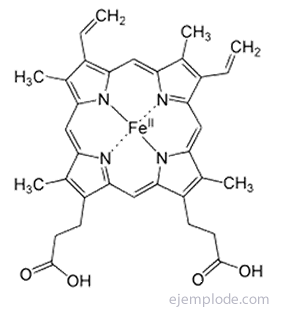
Pürrooli leidub väikestes kogustes kivisöetõrvas, nagu ka tiofeeni. Tõrva fraktsioneeriva destilleerimisega kogutakse tiofeen (keemistemperatuur 84 ° C) koos benseeniga (keemistemperatuur 80 ° C).
Lihtsaim viis furaani saamiseks on furfuraali dekarbonüülimine (süsinikmonooksiidi eemaldamine) (furfuraldehüüd), mis omakorda saadakse kaera- või riisikestade või maisitõlvikute töötlemisel happega keev soolhape.
Kuue aatomi heterotsüklilised ühendid
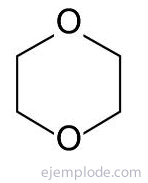
Küllastunud terminitest on üks olulisemaid 1,4-dioksaan või dioksaan, mis on vedelik värvitu, iseloomuliku lõhnaga, mille aur on õhust tihedam ja võib levida piki Ma tavaliselt. Kokkupuutel õhuga võivad moodustada plahvatusohtlikke peroksiide. Reageerib tugevate hapete ja oksüdeerijatega. Reageerib ägedalt mõne katalüsaatoriga.
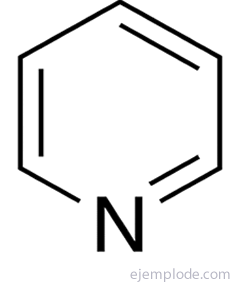
Küllastumata heterotsüklilistest on üks olulisemaid termineid püridiin, mis koosneb lämmastiku heteroaatomiga benseeni tsükli struktuurist. See on paljude elutähtsate molekulide, näiteks deoksüribonukleiinhappe komponentide eelkäija konfiguratsioon.
Heterotsükliliste ühendite süstemaatiline nomenklatuur
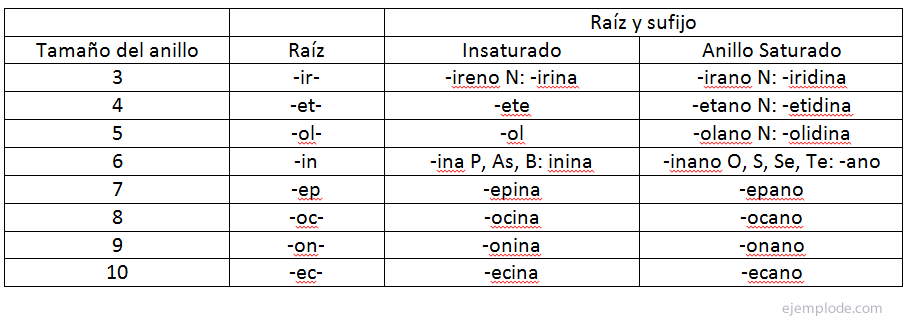
Sõrmuse heterotsükliliste ühendite (monotsüklilised) ühendite puhul tuletatakse sobiv nomenklatuur, ühendades teatud juurele sobivad eesliide ja järelliide järgmiste reeglite kohaselt:
The eesliide tähistab heteroaatomi olemust Juur selgitab sõrmuse suurust ja Liide määrab küllastumatusastme. Nomenklatuuris järgitav järjekord on prefiks-juur-järelliide.
The heteroaatomi olemus tähistatakse eesliidetega nagu okso hapniku jaoks, onu väävli või asa lämmastiku jaoks.
The heteroaatomi paljusus on tähistatud täiendava eesliitega, näiteks di, tri, tetra jne.
Kui on kaks või enam erinevat heteroaatomit, nimetatakse neid järgmise prioriteediga: O> S> N; näiteks Oxazo hapniku ja lämmastiku puhul, Tiazo väävli ja lämmastiku puhul, Oxatio hapniku ja väävli jaoks.
The rõnga suurus seda tähistatakse õige tüvega.
The küllastumatusaste määratakse järelliitega. On mugav märkida, et järelliide on veidi modifitseeritud, kui heterotsüklilises ringis pole lämmastikku.
Sõrmuse nummerdamine algab kõrgeima prioriteediga heteroaatomiga ja jätkub ringi ümber, määrates teistele heteroaatomitele või asendajatele võimalikult madala arvu.
Kui süsteem, millel on maksimaalne kaksiksidemete arv, sisaldab tsüklis endiselt küllastunud aatomit, tähistab see numbrit, mis näitab selle asukohta ja tähte H- suurtäht kursiiv eesliitena.



