Käsite määritelmässä ABC
Sekalaista / / April 22, 2022
käsitteen määritelmä
Atseotroopit ovat kemiallisten yhdisteiden seoksia, joilla on määrätty koostumus ja jotka kiehuvat tietyissä lämpötiloissa. Perusominaisuus on, että seos käyttäytyy ikään kuin se olisi yksi puhdas aine, joka säilyttää ominaisuudet ja helpottaa käsittelyä.

Kemian insinööri
Seos voidaan antaa kahdesta tai useammasta komponentista ja sen sävellys se on sama sekä nestefaasissa että kaasufaasissa, mikä luo yhtäläisyyksiä puhtaiden aineiden kanssa. Tästä on helppo päätellä, että tätä seosta ei voida erottaa komponenteiksi prosesseilla, kuten esim jakotislaus, koska, kuten edellä mainittiin, se säilyttää mittasuhteensa ja käyttäytyy kuin se olisi yksittäinen komponentti.
Toinen ominaisuus on, että tämän seoksen kiehumispiste voi olla korkeampi, matalampi tai jopa yhtä suuri kuin jonkin sen komponentin kiehumispiste. Kun atseotrooppi kiehuu a lämpötila Kiehumispisteen enimmäislämpötilassa sitä kutsutaan maksimiatseotroopiksi ja kun se tekee niin alimmassa mahdollisessa lämpötilassa, sitä kutsutaan minimiatseotroopiksi. Tämä tarkoittaa, että minimiatseotroopilla on alhaisempi kiehumispiste kuin sen puhtailla komponenteilla ja päinvastoin suurimmalla atseotroopilla. Esimerkiksi metanoli-bentseeni-seoksessa atseotrooppi on minimissään (0,61 bentseeni - 0,39 metanolia fraktioissa molaarinen), jonka kiehumispiste on 58 °C, säiliössä, jossa bentseenin kiehumispiste on 80 °C ja metanolin 65 °C
Minimi ja maksimi atseotroopit
Nyt… mistä atseotrooppi tulee? Kun on poikkeama Laki Raoult, eli atseotrooppisen seoksen höyrynpaine ei liity suoraan sen mooliosuuteen, vaan silloin syntyy atseotrooppisen seoksen käsite. Nämä poikkeamat tapahtuvat, kun komponentit vetävät toisiaan merkittävästi puoleensa tai hylkivät toisiaan, eli molekyylien väliset voimat ovat hyvin erilaisia eri yhdisteissä.
Kun poikkeama on positiivinen, meillä on pienin atseotrooppi, kun taas jos poikkeama on negatiivinen, meillä on suurin atseotrooppi. Ymmärtääksemme tätä käsitettä paremmin, katsotaanpa joitain grafiikkaa:
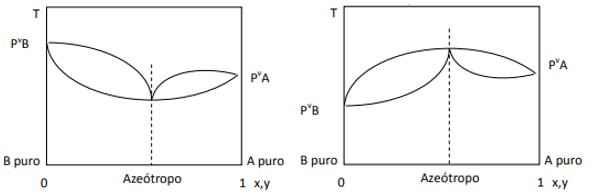
Tässä havaitaan, että jos seos olisi ihanteellinen, Raoultin lain mukaan puhtaiden komponenttien höyrynpaineet tulisi yhdistää suoralla viivalla, koska no, siitä laista on poikkeama, joka aiheuttaa minimi- ja maksimiatseotrooppien muodostumisen riippuen siitä, onko affiniteetti suurempi vai pienempi komponentit. Kun poikkeama Raoultin laista on negatiivinen, kuten vasemmalla olevassa kuvassa, se on minimi kaavio paineen, mutta maksimi lämpötilakaaviossa (siis maksimin atseotrooppi). Toisaalta, jos poikkeama on positiivinen Raoultin lain suhteen, se on maksimi paineessa vs. koostumus, mutta minimi lämpötila vs. koostumus (tässä meillä on vähimmäisatseotrooppi). Älä sekoita kaavioita paine vs. koostumus ja lämpötila vs. sävellys.
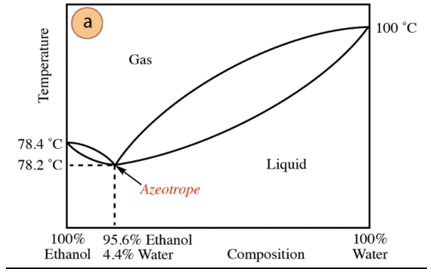
Etanoli-vesi-seoksessa on atseotroopin vähimmäismäärä, jonka koostumus on 95,6 % etanolia ja 4,4 % vettä. Atseotrooppisen seoksen kiehumislämpötila on 78,2 °C alhaisempi kuin puhtaiden komponenttien. Oletetaan siis, että tislataan vesi-etanoli-seosta, jossa on korkea vesipitoisuus (lähes 100 %). Puhdasta alkoholia ei ole mahdollista saada, koska jokaisessa tislausvaiheessa saadaan suurempia fraktioita. etanolia, mutta ei koskaan saavuta 100 %, se lähestyy vähitellen atseotrooppisen seoksen koostumusta (matalin kohta alla). Tästä syystä sillä, kuten vedellä, on taipumus muodostaa minimaalisia atseotrooppeja orgaaniset yhdisteet (ottaen huomioon vuorovaikutuksessa olevien molekyylien välisten voimien tyyppi), vesi on ensin poistettava seoksesta puhtaan yhdisteen saamiseksi. Tai, kun atseotrooppi on saatu, menetelmät uuttaminen ylimääräisestä vedestä.
Edellä olevan perusteella alkoholia ei löydy sattumalta (supermarketista ja apteekki) 95 %:lla on halvin tuote, joka voidaan saada. Puhtaan alkoholin saamiseksi atseotrooppi on "rikottava". tekniikka lisäksi, kuten kuivausaineiden tai atseotrooppisten tislausten käyttö. Atseotrooppinen tislaus koostuu ylimääräisen komponentin lisäämisestä seokseen, joka vaikuttaa kuljettamalla ja vuorovaikutusta minkä tahansa seoksen komponentin kanssa (suurempi affiniteetti) voidaan poistaa seoksesta.
Aiheet Azeotroopeissa