50 Esimerkkejä aldehydeistä ja ketoneista
Esimerkkejä / / November 06, 2023
The aldehydit ovat orgaaniset yhdisteet joiden rakenteessa on funktionaalinen karbonyyliryhmä (= C = O), joka on kytketty hiiliketjuun ja vetyatomiin. Esimerkiksi: metanaali (kutsutaan myös formaldehydiksi), etanoli (kutsutaan myös asetaldehydiksi) ja propanaali (kutsutaan myös propaldehydiksi).
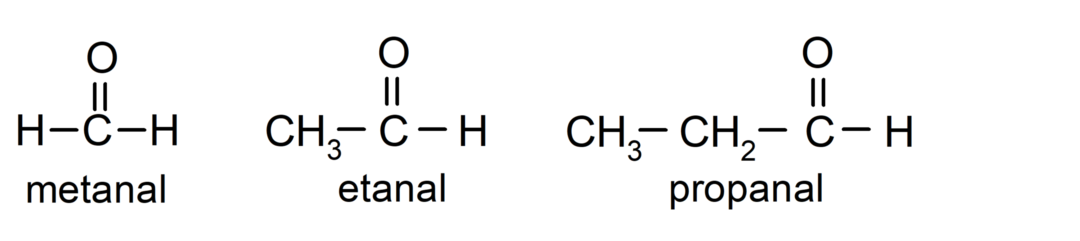
The ketonit Ne ovat orgaanisia yhdisteitä, joiden rakenteessa on karbonyyliryhmä, joka on liittynyt kahteen hiiliatomiin. Esimerkiksi: propanoni (kutsutaan myös asetoniksi), butanoni ja 2-pentanoni.
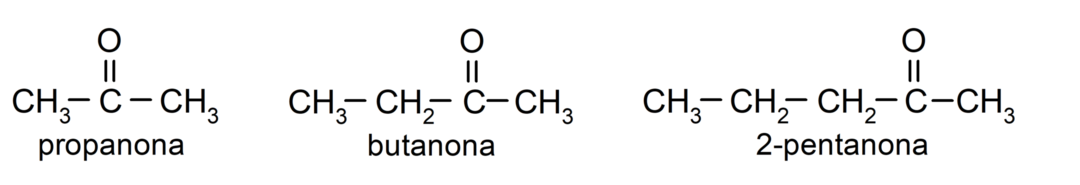
Erot aldehydien ja ketonien välillä
Tärkeimmät erot aldehydien ja ketonien välillä ovat:
- Aldehydien rakenteessa on funktionaalinen karbonyyliryhmä, joka sijaitsee toisessa terminaalisessa päässä, kun taas ketoneilla on karbonyyliryhmä, joka sijaitsee niiden ei-terminaalisissa asemissa rakenne.
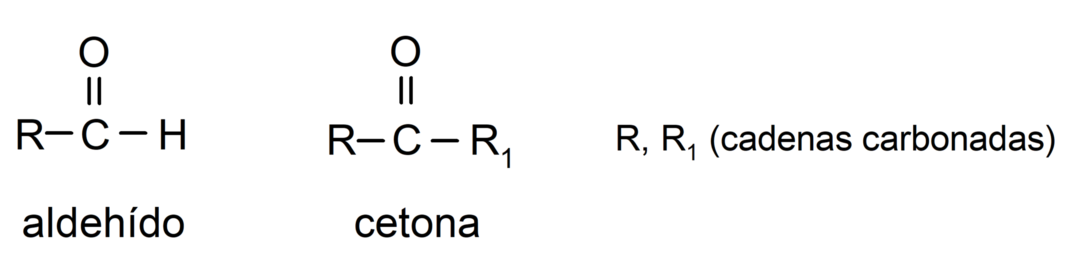
- Aldehydit hapetetaan reaktiossa Tollensin reagenssin kanssa, jolloin muodostuu metallista hopeaa. Ne myös hapettavat Benedictin reagenssia vastaan muodostaen kuparioksidia. Kumpikaan reagenssi ei hapeta ketoneja.
- Aldehydit pelkistetään primäärisiksi alkoholeiksi, kun taas ketonit pelkistetään sekundäärisiksi alkoholeiksi.
Fyysiset ominaisuudet
Aldehydien fysikaaliset ominaisuudet
Aldehydien fysikaaliset ominaisuudet ovat hyvin erilaisia, koska ne riippuvat karbonyyliryhmään kytketyn hiiliketjun kokoonpanosta.
Jotkut ovat:
- Aldehydit, jotka liukenevat parhaiten veteen, ovat kooltaan pienempiä, kuten metanoli ja etanoli.
- Haihtuvilla aldehydeillä on pistävä ja jopa ärsyttävä haju.
- Karbonyyliryhmä antaa niille polaarisuuden.
- Niillä on yleensä korkeammat kiehumispisteet kuin samankokoisilla kemiallisilla yhdisteillä.
Ketonien fysikaaliset ominaisuudet
Ketonien fysikaaliset ominaisuudet riippuvat siitä, kuinka hiiliketju, joka on kytketty karbonyyliryhmään, muodostuu.
- Monilla ketoneilla on miellyttävä tuoksu.
- Sen liukoisuus veteen riippuu karbonyyliryhmään kiinnittyneen hiiliketjun koosta. Mitä pienempi hiiliketju on, sitä liukenevampi ketoni on veteen.
- Karbonyyliryhmä antaa niille huomattavan polaarisuuden.
- Niillä on melko korkeat kiehumispisteet verrattuna molekyylikokoisiin kemiallisiin yhdisteisiin.
Kemialliset ominaisuudet
Aldehydien kemialliset ominaisuudet
Aldehydien kemiallisista ominaisuuksista löytyy:
Ne hapetetaan vastaavan karboksyylihapon muodostamiseksi, eli muodostuneella hapolla on sama määrä hiiliä hiiliketjussa kuin aldehydi joka aiheutti sen. Esimerkiksi:
- Hapetus Tollensin reagenssilla (ammoniakaalinen hopeakompleksi emäksisessä liuoksessa, [Ag (NH)3)2]+) tuottaa etanolista etaanihappoa ja metallihopeaa.
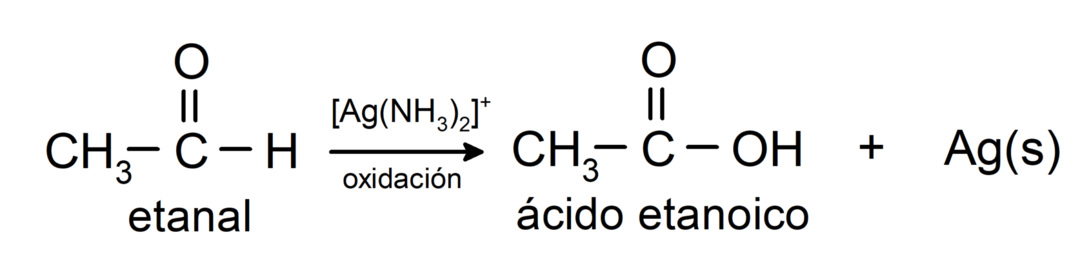
- Etanaalin hapetus Benedictin reagenssilla (kuparisulfaatin alkalinen liuos) tuottaa etaanihappoa ja kuparioksidia.
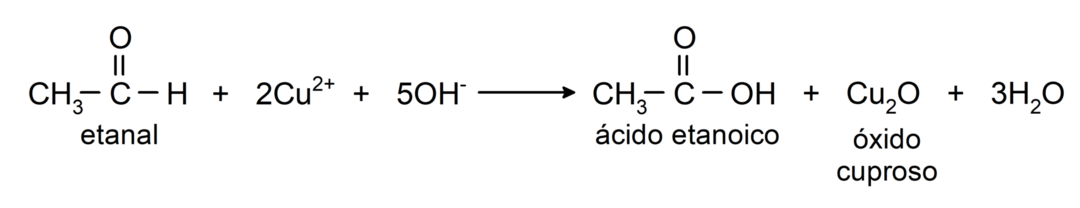
Ne käyvät läpi nukleofiilisiä additioreaktioitaeli nukleofiilin lisääminen karbonyyliryhmään. Esimerkiksi:
- Syaanivetyhapon lisääminen syanohydriinien tai syanohydriinien muodostamiseksi.
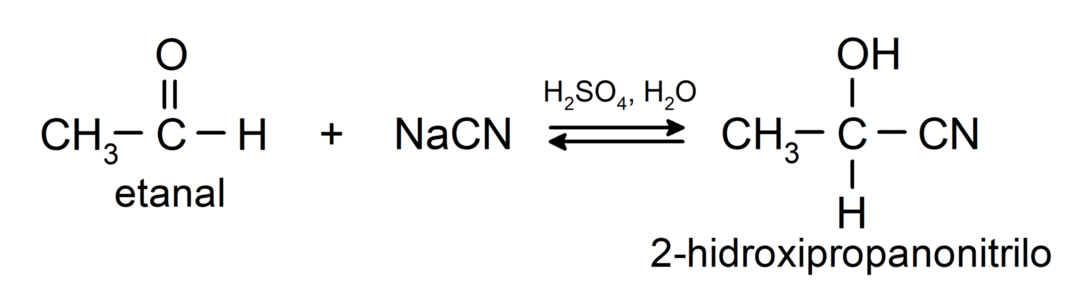
- Vedettömän happojen läsnäollessa aldehydien karbonyyliryhmään lisätään alkoholeja asetaaleiden ja hemiasetaalien muodostamiseksi.
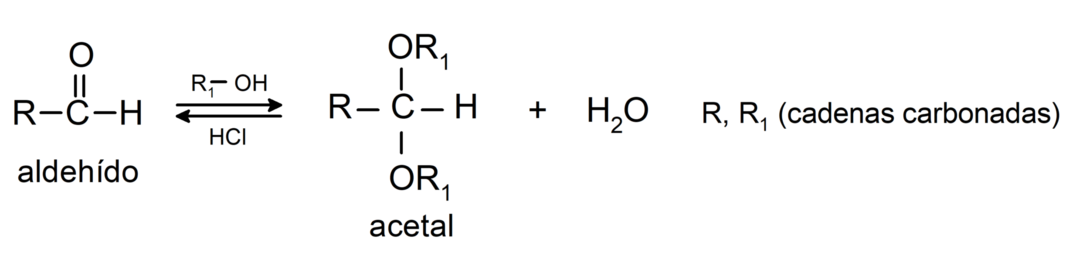
Ne käyvät läpi aldolin kondensaatioreaktioita. Näissä reaktioissa kahden aldehydin yhdistyminen tapahtuu natriumhydroksidin (NaOH) ja kemiallinen yhdiste tuloksena olevaa kutsutaan aldoliksi. Esimerkiksi:
- Etanaalin kondensaatioreaktio laimennetun NaOH: n läsnä ollessa.
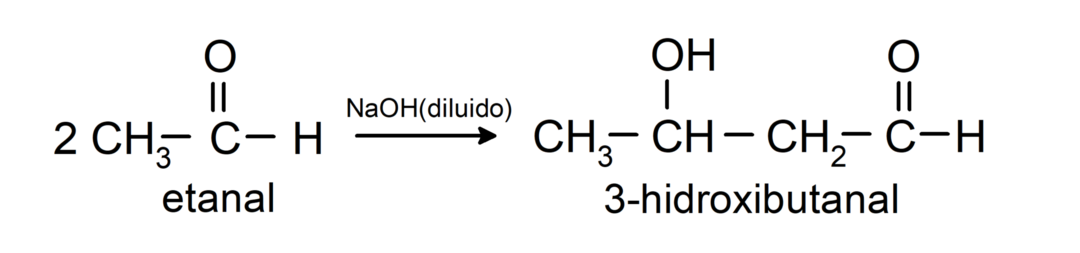
Ne pelkistetään primäärisiksi alkoholeiksi. Aldehydit voidaan pelkistää primäärisiksi alkoholeiksi katalyyttisellä hydrauksella tai pelkistämällä natriumboorihydridillä (NaBH).4) ja litiumalumiinihydridi (LiAlH4).
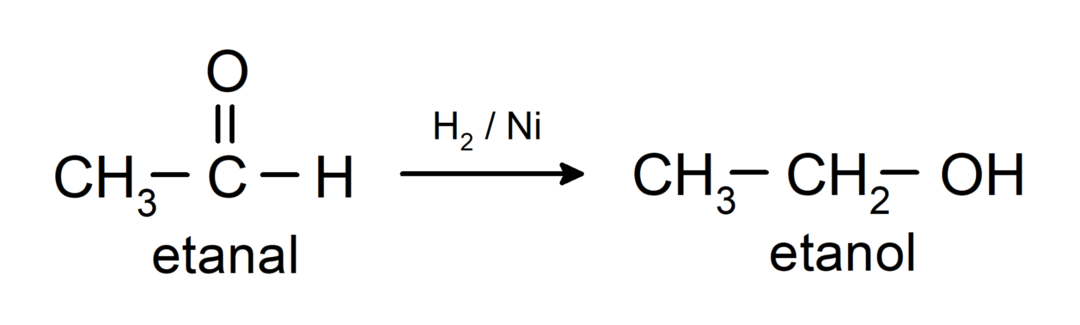
Ketonien kemialliset ominaisuudet
Ketonien kemiallisista ominaisuuksista löytyy:
Ne käyvät läpi nukleofiilisiä additioreaktioita. Esimerkiksi:
- Syaanivetyhapon lisääminen syanohydriinien tai syanohydriinien muodostamiseksi.
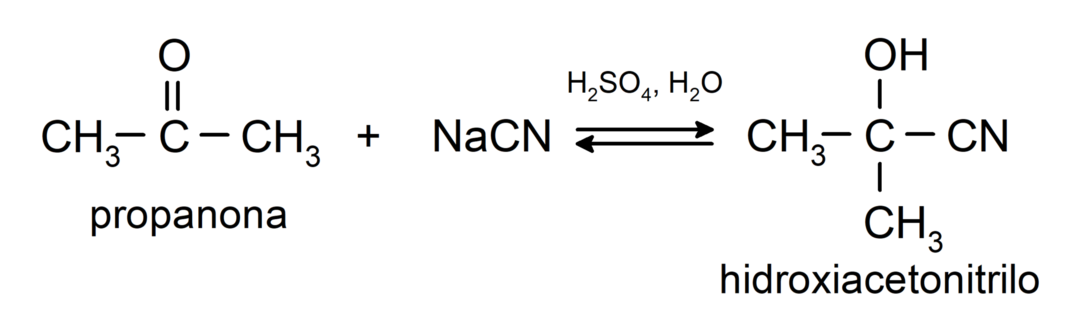
Ne lisäävät alkoholia (vedettömien happojen läsnä ollessa) ketonien karbonyyliryhmään muodostaen ketaaleja ja hemiketaaleja. Esimerkiksi:
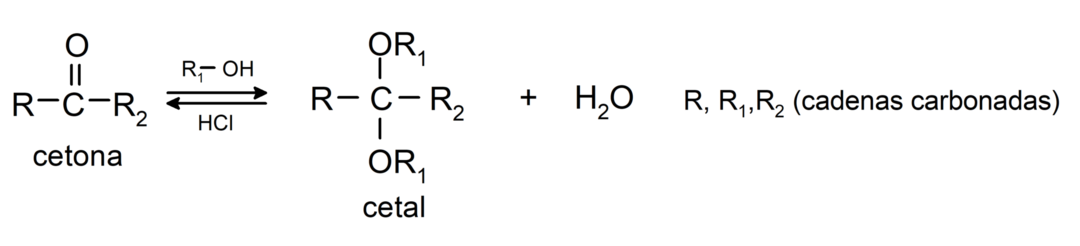
Ne käyvät läpi halogenointireaktioita. Ketonit, joissa on alfavetyä (α) reagoi korvaamalla tämä vety halogeeneilla (kloori (Cl), bromi (Br), jodi (I), fluori (F)) happamien tai emäksisten katalyyttien läsnä ollessa. Korvaus tapahtuu lähes yksinomaan hiilessä αeli hiiltä, joka on sitoutunut vetyyn α. Esimerkiksi:
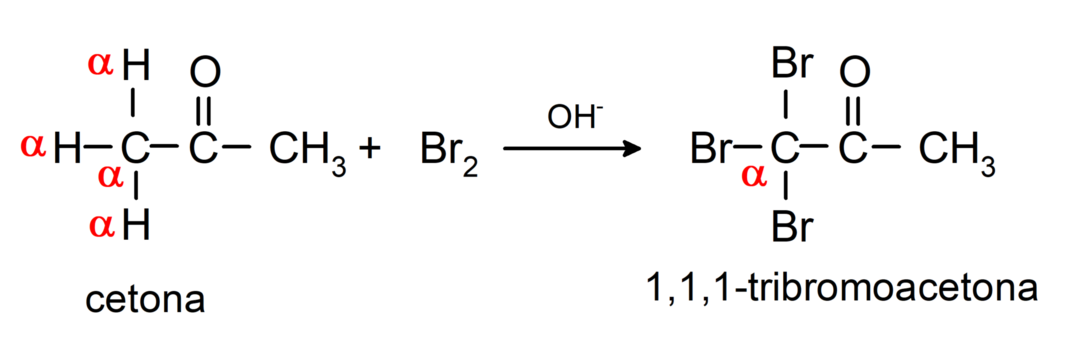
Ne pelkistetään sekundäärisiksi alkoholeiksi katalyyttisellä hydrauksella tai pelkistämällä natriumboorihydridillä (NaBH4) ja litiumalumiinihydridi (LiAlH4). Esimerkiksi:
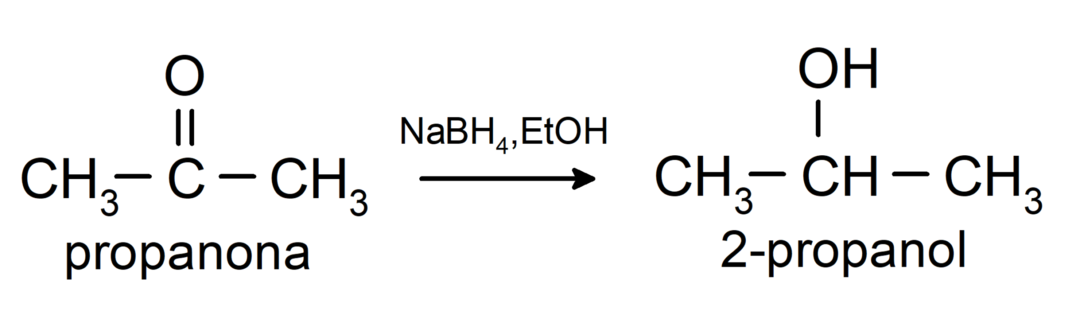
Tollensin ja Benedictin reagenssit eivät hapeta ketoneja.
Aldehydien nimikkeistö
Kansainvälisen puhtaan ja sovelletun kemian liiton (IUPAC) sääntöjen mukaan Aldehydit nimetään etuliitteillä, jotka osoittavat ketjun hiilen määrän. hiilihapotettu. Karbonyyliryhmän paikkaa ei tarvitse määritellä, koska se on aina asemassa yksi, molekyylin toisessa päässä. Lisäksi aldehydinimen loppuun kirjoitetaan jälkiliite -al. Esimerkiksi:
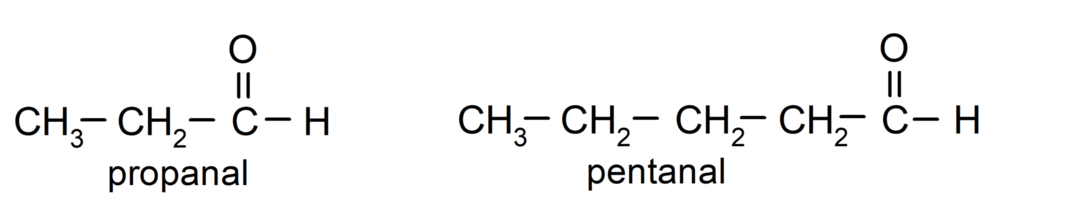
Jos aldehydi koostuu useista hiiliketjuista, eli siinä on haaroja, pääketjuksi valitaan se hiiliketju, jossa on eniten hiiliatomeja. Muut ketjut nimetään substituenttiryhmiksi, ja kunkin substituentin asema valitaan siten, että se vie ketjussa pienimmän mahdollisen määrän. Lisäksi hiiliatomit alkavat laskea siitä päästä, jossa on karbonyyliryhmä. Esimerkiksi:
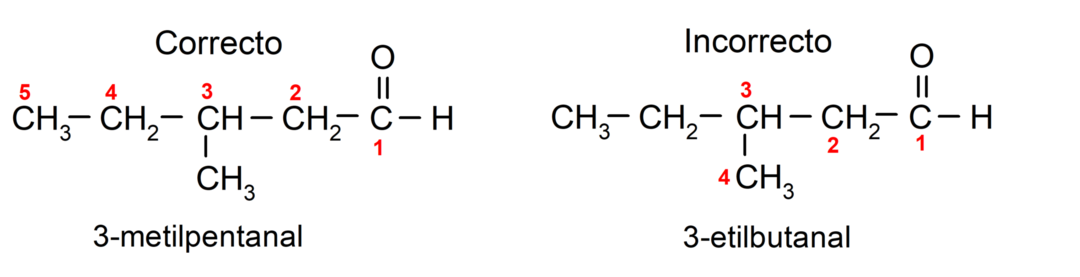
Aldehydit, joissa on kaksi karbonyyliryhmää, nimetään käyttämällä päätettä -dial. Esimerkiksi:
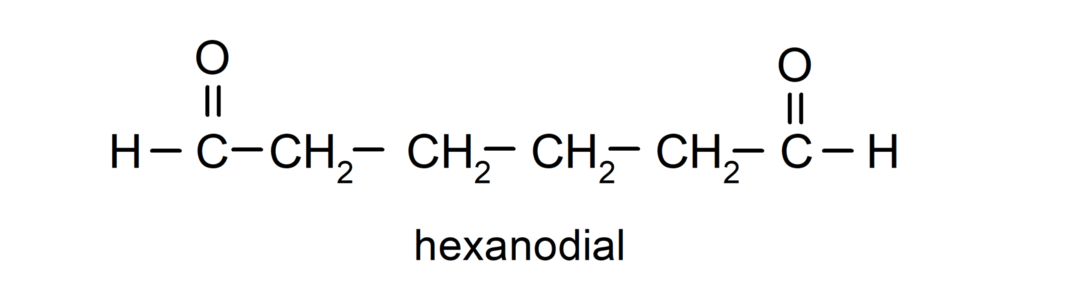
Ketoninimikkeistö
Kansainvälisen puhtaan ja sovelletun kemian liiton (IUPAC) mukaan ketonit nimetään käyttämällä etuliitteitä, jotka osoittavat hiiliketjun hiilen määrän.
Toisaalta asetonin nimi kirjoitetaan käyttämällä päätettä -one, jota edeltää numero, joka osoittaa karbonyyliryhmän aseman hiiliketjussa. Karbonyyliryhmän sijainti tulee valita siten, että se vastaa pienintä mahdollista numerointia. Esimerkiksi:
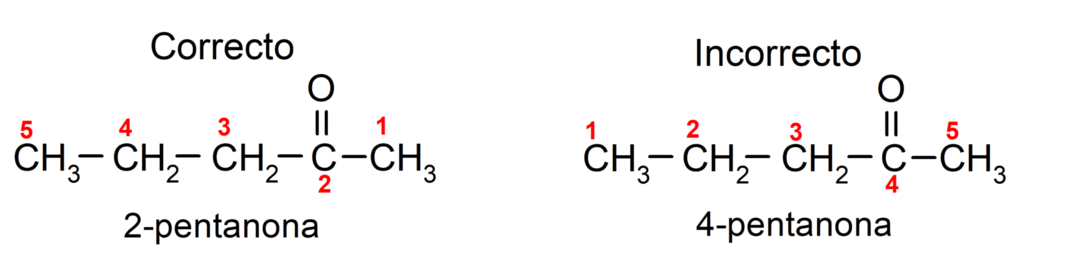
Valitsemme ketonin, joka koostuu useista hiiliketjuista eli haaroista pääketjuna hiiliketju, jossa on eniten hiiliatomeja ja joka sisältää ryhmän karbonyyli. Loput ketjut on nimetty substituenttiryhmiksi. Esimerkiksi:
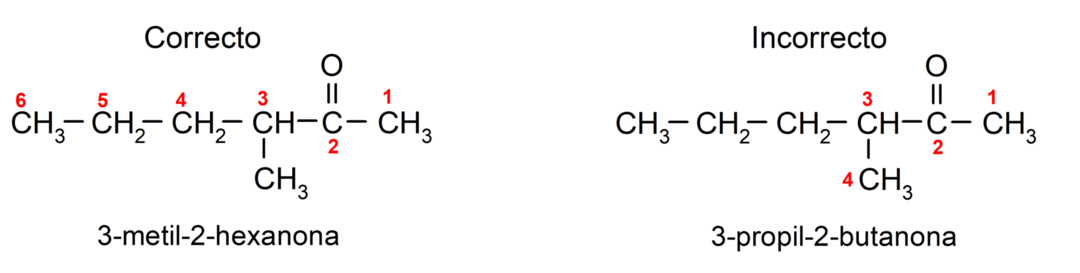
On ketoneja, joissa on kaksi karbonyyliryhmää, niitä kutsutaan dioneiksi. Esimerkiksi:
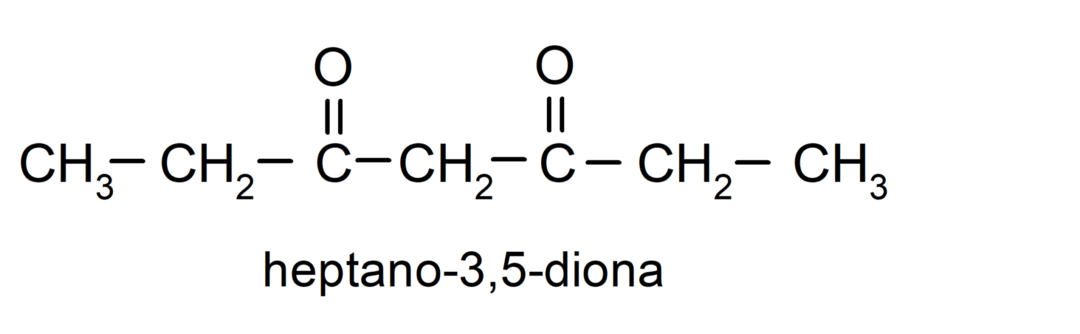
Esimerkkejä aldehydeistä
- metanoli (formaldehydi)
- etanoli (asetaldehydi)
- propanaali (propaldehydi)
- butanaali
- pentanal
- heksanaali
- 3-bromisyklopentaanikarbaldehydi
- sykloheksaanikarbaldehydi
- bentsaldehydi
- 4,4-dimetyylipentanaali
- 2-hydroksibutanaali
- 2-hydroksi-2-metyylibutanaali
- 2,3-dimetyylipentanaali
- pentaanikaali
- 4-hydroksi-3-metoksibentsaldehydi
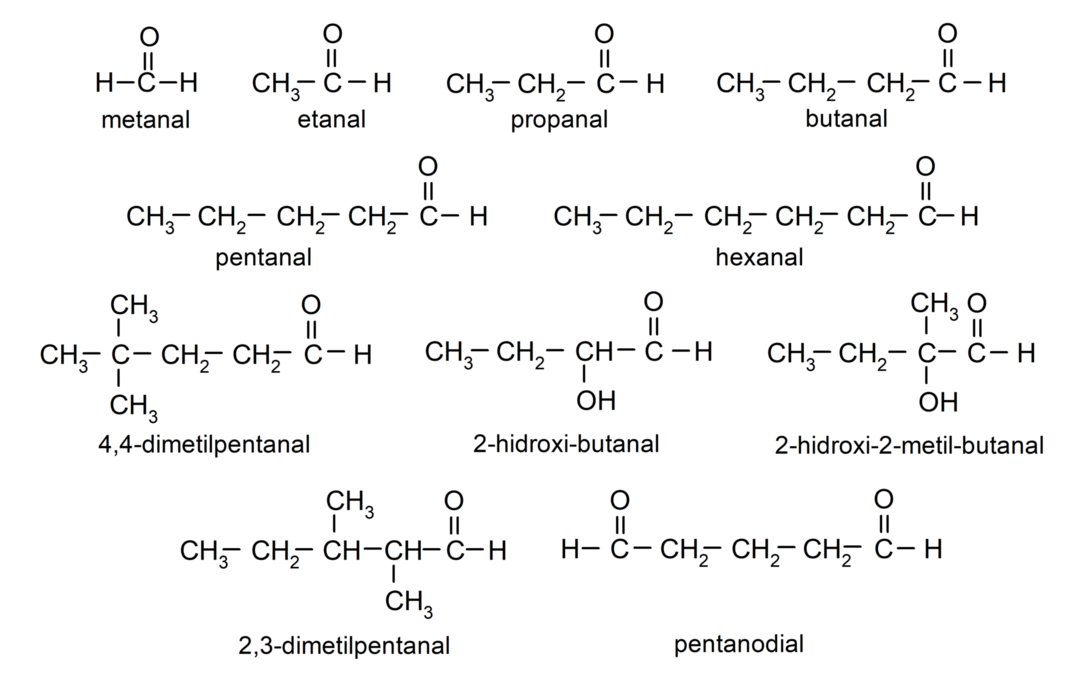
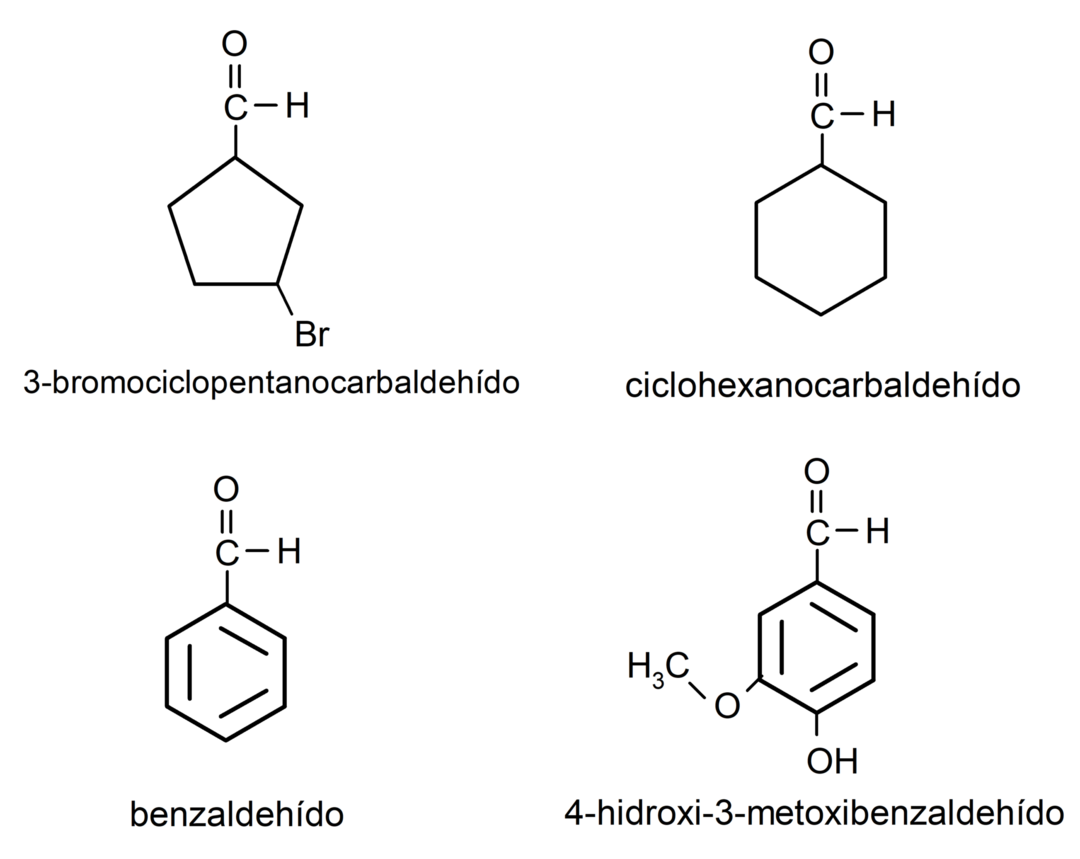
Esimerkkejä ketoneista
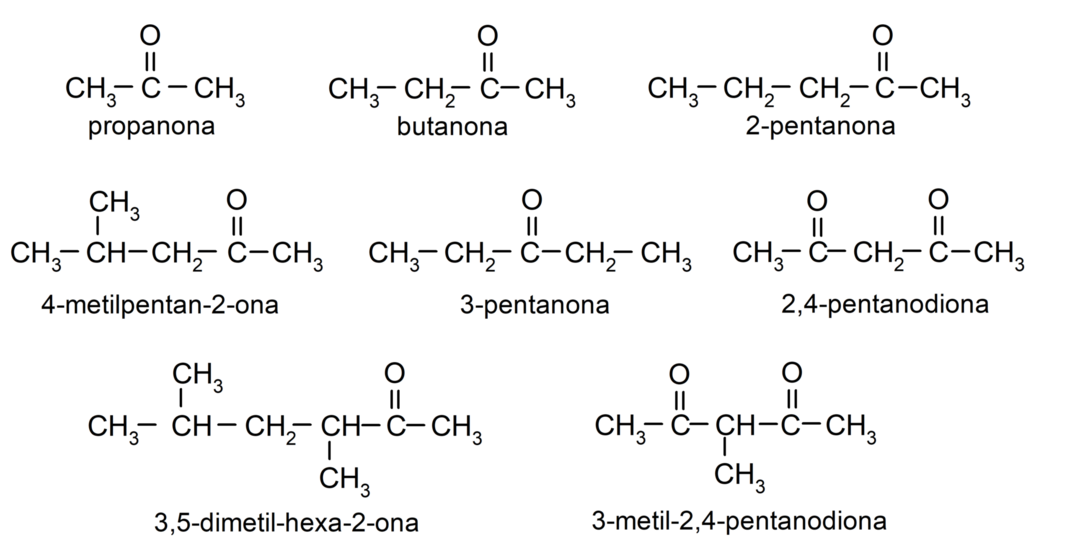
- propanoni (asetoni)
- butanoni
- 2-pentanoni
- 4-metyylipentan-2-oni
- 3-metyylisykloheksanoni
- sykloheksyylimetyyliketoni
- 3,4-dimetyyliheksan-2-oni
- etyylifenyyliketoni
- 2,4-pentaanidioni
- sykloheksanoni
- 3-pentanoni
- 3-metyyli-2,4-pentaanidioni
- 1-fenyylipropanoni
- syklopentanoni
- difenyyliketoni
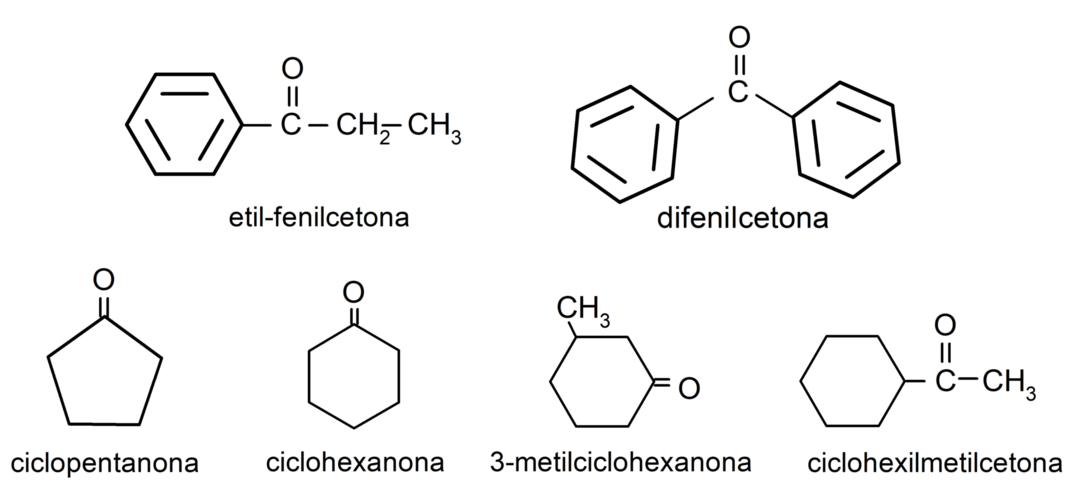
Aldehydien käyttö jokapäiväisessä elämässä
Jotkut aldehydien käyttötavat ovat:
- Niitä käytetään liuottimien, maalien, hajuvesien, hartsien ja esanssien valmistukseen.
- Niitä käytetään säilöntäaineina kosmeettisissa tuotteissa, biologisissa näytteissä ja ruumiissa. Formaldehydiä käytetään eniten näihin tarkoituksiin.
- Niitä käytetään muovien valmistukseen, mikä mahdollistaa metalliosien vaihdon autoteollisuudessa.
- Niitä käytetään joidenkin elintarvikkeiden mausteina.
- Niitä käytetään desinfiointiaineina.
- Niitä on käytetty joidenkin räjähteiden, kuten pentaerytritolitetranitraatin (TNPE) valmistukseen.
Ketonien käyttö jokapäiväisessä elämässä
Jotkut ketonien käyttötavat ovat:
- Niitä käytetään liuottimien valmistuksessa. Erityisesti asetonia käytetään laajalti maalien ja lakkojen poistamiseen.
- Niitä käytetään joidenkin kumien ja voiteluaineiden valmistukseen.
- Niitä käytetään maalien, lakkojen ja lakkojen valmistukseen.
- Niitä käytetään lääkkeiden ja kosmetiikan valmistukseen.
Aldehydi- ja ketonimyrkyllisyys
- Aldehydit. Kosketus aldehydien kanssa ärsyttää ihoa, silmiä ja hengitysteitä. Lisäksi aldehydeille altistuminen on yhdistetty sairauksiin, kuten syöpään, kosketusihottumaan sekä maksa- ja hermostoa rappeutuviin sairauksiin. WHO (World Health Organization) pitää esimerkiksi formaldehydiä syöpää aiheuttavana yhdisteenä.
- ketonit. Toistuva altistuminen ketoneille voi vahingoittaa keskushermostoa. Tämä voi aiheuttaa muistin menetystä, heikkoutta, lihassärkyä ja kramppeja. Lisäksi, jos iho joutuu kosketuksiin ketonien kanssa, ilmenee kuivuutta ja halkeamia. Toisaalta, jos ketoneja hengitetään, ilmaantuu hengitysteiden ärsytystä ja yskää.
Viitteet
- Llorens Molina, JA. (2018). “Aldehydit ja ketonit: Esimerkkejä.” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) "Tollens-reagenssi: aldehydien tunnistamisesta niiden käyttöön nanoteknologiassa. Historialliset näkökohdat ja didaktiset sovellukset.”V. 111 nro. 3. Espanjan kuninkaallinen kemian seura.
- William Bauer, Jr. (2000) «Metakryylihappo ja johdannaiset» julkaisussa Ullmann’s Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI: 10.1002/14356007.a16_441.
- "Ne paljastavat uuden myrkyllisyyden mekanismin syöpää aiheuttavien yhdisteiden ryhmässä, jotka ovat peräisin ruokavaliosta ja ympäristöstä" (2022) www.conicet.gov.ar Saatavilla: https://www.conicet.gov.ar/ Käytetty: 20.6.2023.
Seuraa:
- Alkoholit
- Sokerit
- Alkaanit



