Exemple de liaison peptidique
Chimie / / July 04, 2021
le Liaison peptidique est celui dans lequel deux molécules d'acides aminés sont liées par condensation.
Pour mieux comprendre les liaisons peptidiques, les Acides Aminés doivent d'abord être définis :
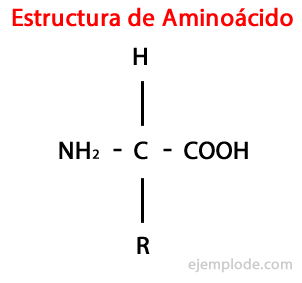
Les Les acides aminés sont des molécules organiques court contenant au moins un groupe amino (-NH2), de nature alcaline, et un groupe carboxyle (-COOH), de caractère acide.
Bien que les êtres vivants synthétisent, à des fins différentes, des types très divers d'acides aminés, les plus importants sont ceux qui font partie des protéines, qui appartiennent tous à la classe des acides -aminés.
Les acides -aminés sont caractérisés par le fait que les groupes acide et amino sont attachés au même atome de carbone, appelé carbone . De plus, ce carbone se lie, comme troisième substituant, à un atome d'hydrogène et, comme quatrième substituant, un groupe supplémentaire de taille et de caractéristiques diverses, qui différencie chaque acide aminé de les autres.
Le quatrième substituant est appelé Chaîne latérale d'acide aminé et est souvent représenté sous une forme simplifiée par la lettre R.
Comme les quatre substituants du carbone sont différents et adoptent un arrangement tétraédrique autour de celui-ci, les acides -aminés présents isomérie optique, c'est-à-dire lorsqu'une molécule a un forme alternative qui ressemble à un image miroir son, qui finalement n'est pas une molécule égale. Ces deux formes isomères de la molécule sont affectées des lettres D ou L, selon la façon dont les substituants sont disposés dans l'espace. Tous les acides aminés contenus dans les protéines sont L.
Les acides aminés sont classés selon leur caractère chimique dans Polaire et Apolaire. Les polaires à leur tour sont divisés en Neutre et Chargé (qui peut être acide ou basique). Les Non polaire peut être aliphatique ou aromatique.
Peptides et liaison peptidique
Les peptides sont le produit de l'union covalente d'acides aminés par des liaisons amides, formant par condensation de l'extrémité carboxyle de l'une et de l'extrémité aminée de l'autre, libérant une molécule d'eau dans le réaction. Cette union s'appelle Peptide Bond.
Le mécanisme de cette réaction est présenté ci-dessous, dans lequel le Groupes amino et carboxyle, et la condensation des molécules d'acides aminés se produit pour former le peptide.
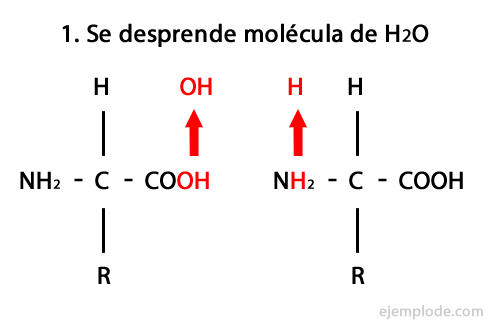
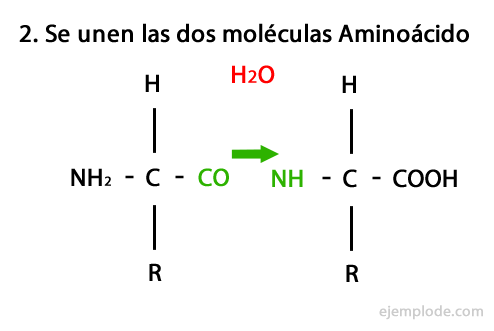

Les peptides, comme les acides aminés et les protéines, ont un groupe amino et un groupe carboxyle à leurs extrémités sans réagir.
Pour préciser la formule d'un peptide simple, et même d'une protéine, il suffit de lister les acides aminés qui le composent, en commençant par celui avec un groupe Amino gratuit, et se terminant par celui avec son groupe carboxyle libre.
Certains peptides présents dans le corps sont les Vasopressine, qui augmente la pression artérielle et augmente la réabsorption d'eau dans les reins; la Enképhaline, ce qui réduit la sensation de douleur; et la L'ocytocine, ce qui provoque la contraction de l'utérus.
Caractéristiques de liaison peptidique
La condensation du groupe Amino d'un acide aminé avec le carboxyle d'un autre, se déroule dans un solvant aqueux, Pour ce que ce n'est pas spontané, et donc la synthèse des protéines nécessite un apport d'énergie.
La liaison peptidique, comme dans toute liaison amide, présente une résonance entre deux formes extrêmes: la forme neutre, avec une liaison simple joignant le carbone carbonyle du premier acide aminé et l'azote aminé du second (C-N), et la forme avec séparation des charges dans laquelle les deux atomes sont liés par une double liaison (C = N). En réalité, la liaison peptidique n'adopte aucune des deux situations extrêmes, mais est un hybride résonnant des deux.
Il y a l'appel Plan peptidique, Il se compose de tous les atomes impliqués dans la liaison peptidique, qui rejoignent les deux acides aminés initiaux. D'une part, les atomes d'Azote et d'Hydrogène, avec leur Carbone α respectif dans le premier acide aminé. De l'autre, le Carbone de l'autre acide aminé, avec l'Oxygène et le Carbone du groupe Carbonyle.
Différences entre les peptides et les protéines
Les les peptides ont un faible nombre d'acides aminés, qui va de deux à quelques dizaines d'entre eux, et leur conformation en solution devient flexible.
le petites protéines, structurellement proches des gros peptides, ont une conformation définie et beaucoup moins flexible.
Il existe des protéines qui, comme les peptides, ont une conformation désordonnée et flexible, mais qui s'ordonnent lorsqu'elles interagissent avec d'autres macromolécules de la cellule.
20 exemples d'acides aminés qui participent à la liaison peptidique
- Glycine
- À la fille
- Valine
- Leucine
- Isoleucine
- Proline
- Méthionine
- Phénylalanine
- Tyrosine
- Tryptophane
- Sérine
- thréonine
- Cystéine
- Asparagine
- Glutamine
- L'acide aspartique
- Acide glutamique
- Lysine
- Arginine
- Histidine


