बाइनरी बिक्री के 30 उदाहरण
उदाहरण / / November 09, 2023
द्विआधारी लवण (तटस्थ लवण) एक धातु और एक अधातु के संयोग से बनते हैं। हैं रासायनिक यौगिक केवल दो से बना है रासायनिक तत्व. उदाहरण के लिए: सोडियम क्लोराइड (NaCl) और पोटेशियम ब्रोमाइड (KBr)।
- यह सभी देखें: धातु और अधातु
द्विआधारी लवण के उदाहरण
- सोडियम क्लोराइड (NaCl)
- आयरन (II) क्लोराइड (FeCl2)
- आयरन (III) क्लोराइड (FeCl3)
- कोबाल्ट(II) सल्फाइड (CoS)
- कोबाल्ट(III) सल्फाइड (Co2हाँ3)
- लेड(II) सल्फाइड (PbS)
- लेड(IV) सल्फाइड (PbS2)
- कैल्शियम क्लोराइड (CaCl2)
- सोडियम फ्लोराइड (NaF)
- लिथियम क्लोराइड (LiCl)
- स्ट्रोंटियम क्लोराइड (SrCl2)
- बेरियम क्लोराइड (BaCl2)
- एल्यूमिनियम क्लोराइड (AlCl3)
- मैग्नीशियम सल्फाइड (एमजीएस)
- रुबिडियम क्लोराइड (आरबीसीएल)
- कैल्शियम ब्रोमाइड (CaBr2)
- पोटेशियम सल्फाइड (K2एस)
- मैग्नीशियम ब्रोमाइड (MgBr2)
- जिंक सल्फाइड (Zn2एस)
- लिथियम ब्रोमाइड (LiBr)
- निकेल क्लोराइड (NiCl2)
- यूरेनियम (III) क्लोराइड (UCl3)
- सिल्वर ब्रोमाइड (AgBr)
- सिल्वर आयोडाइड (एजीआई)
- पोटेशियम ब्रोमाइड (KBr)
द्विआधारी लवणों का नामकरण
पारंपरिक नामकरण के अनुसार, गैर-धात्विक तत्व का नाम अंत में -ide के साथ लिखकर द्विआधारी लवण का नाम रखा जाता है। दूसरी ओर, धात्विक तत्व का नाम उसकी ऑक्सीकरण अवस्था के अनुसार लिखा जाता है:
- सबसे कम ऑक्सीकरण अवस्था के लिए, इसे अंत में -oso के साथ लिखा जाता है। उदाहरण के लिए: फेरस क्लोराइड (FeCl2), जहां लोहे की ऑक्सीकरण अवस्था 2+ होती है।
- उच्चतम ऑक्सीकरण अवस्था के लिए, इसे अंत -ico के साथ लिखा जाता है। उदाहरण के लिए: फेरिक क्लोराइड (FeCl3), जहां लोहे की ऑक्सीकरण अवस्था 3+ होती है।
व्यवस्थित नामकरण के अनुसार, द्विआधारी लवणों का नाम गैर-धात्विक तत्व का नाम एक उपसर्ग के साथ लिखकर दिया जाता है जो कि इसकी मात्रा को इंगित करता है। परमाणुओं यौगिक में इस तत्व का. इसके अलावा, अंत में -यूरो को गैर-धातु तत्व के नाम पर रखा गया है। फिर धात्विक तत्व का नाम रखा जाता है। उदाहरण के लिए: मैग्नीशियम डाइक्लोराइड (MgCl2) और आयरन ट्राइक्लोराइड (FeCl3).
स्टॉक के नामकरण के अनुसार, गैर-धातु तत्व का नाम अंत में -ide के साथ लिखकर द्विआधारी लवण का नाम दिया जाता है। फिर, धात्विक तत्व का नाम रखा जाता है और उसके बाद रोमन अंकों और कोष्ठकों में उसकी ऑक्सीकरण अवस्था लिखी जाती है। उदाहरण के लिए: आयरन (II) क्लोराइड (FeCl2) और कोबाल्ट (III) सल्फाइड (Co2हाँ3).
द्विआधारी लवणों का अनुप्रयोग
- इनका उपयोग खाद्य और दवा उद्योगों में रेफ्रिजरेंट के रूप में किया जाता है। उदाहरण के लिए: कैल्शियम क्लोराइड (CaCl2).
- इनका उपयोग धातु की सतहों को जंग से बचाने के लिए किया जाता है। उदाहरण के लिए: सोडियम फ्लोराइड (NaF)।
- इनका उपयोग कागज और निर्माण उद्योग में आर्द्रता को नियंत्रित करने के लिए किया जाता है। उदाहरण के लिए: कैल्शियम क्लोराइड (CaCl2).
- इनका उपयोग कांच उद्योग में अशुद्धियों को खत्म करने के लिए किया जाता है। उदाहरण के लिए: सिलिकॉन टेट्राक्लोराइड (SiCl4)।
- इनका उपयोग खाना पकाने की सामग्री के रूप में किया जाता है। उदाहरण के लिए: सोडियम क्लोराइड (NaCl).
द्विआधारी लवण के भौतिक गुण
- इनका गलनांक उच्च होता है क्योंकि ये किससे बने होते हैं आयोनिक बांड.
- घुलने या पिघलने पर ये विद्युत धारा प्रवाहित करते हैं।
- सबसे आम नमक में कम कठोरता होती है।
- वे संपीड़ित नहीं हैं.
- अधिकांश पानी में घुल सकते हैं।
द्विआधारी लवण कैसे प्राप्त होते हैं?
निम्नलिखित कुछ रासायनिक प्रतिक्रियाओं के माध्यम से बाइनरी लवण प्राप्त किए जा सकते हैं:
धातु और अधातु के बीच प्रतिक्रिया. उदाहरण के लिए: सोडियम (Na) और डाइक्लोराइड (Cl) के बीच प्रतिक्रिया2) सोडियम क्लोराइड (NaCl) उत्पन्न करता है।
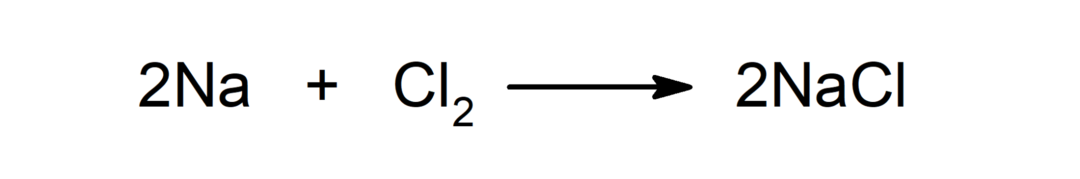
धातु और अम्ल के बीच प्रतिक्रिया. उदाहरण के लिए: पोटेशियम (K) और हाइड्रोक्लोरिक एसिड (HCl) के बीच प्रतिक्रिया से पोटेशियम क्लोराइड (KCl) और डाइहाइड्रोजन (H) बनता है2).
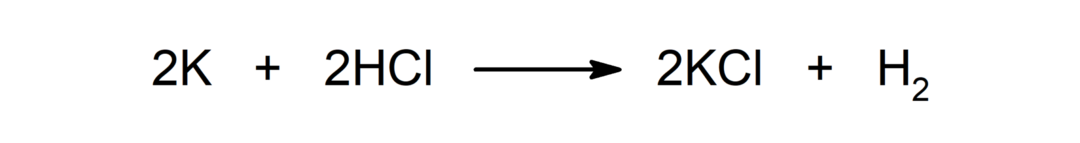
अम्ल और क्षार के बीच प्रतिक्रिया. उदाहरण के लिए: हाइड्रोक्लोरिक एसिड (HCl) और सोडियम हाइड्रॉक्साइड (NaOH) के बीच प्रतिक्रिया से सोडियम क्लोराइड (NaCl) और पानी (H) बनता है2दोनों में से एक)।
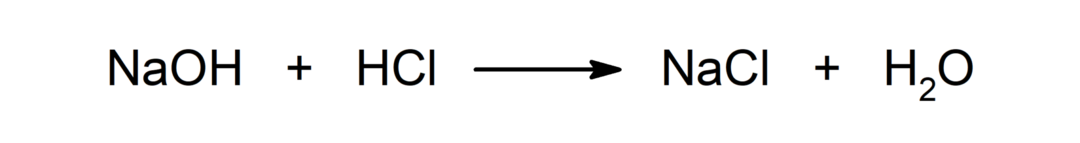
साथ में पीछा करना:
- ऑक्सीलवण
- तटस्थ लवण
- अम्ल लवण
संदर्भ
- सेरोन विलाल्बा, ए., नोवोआ रामिरेज़, सी. एस., और एल्पिज़ार जुआरेज़, ई. (2020). नामकरण वीडियो 1: द्विआधारी लवण और रासायनिक प्रतिक्रिया.
- एक्यूरियो एरियस, एम. वी., और डेलगाडो मेन्डेज़, एम. और। (2022). "हरलिंडा टोरल" शैक्षिक इकाई में हाई स्कूल रसायन विज्ञान में "बाइनरी यौगिकों" के लिए गेम-आधारित शिक्षण मार्गदर्शिका (स्नातक थीसिस, राष्ट्रीय शिक्षा विश्वविद्यालय)।
- कैबरेरा, एम. जे। एच। (2005). बाइनरी और टर्नरी यौगिकों के इलेक्ट्रॉनिक और संरचनात्मक गुणों के पहले सिद्धांतों से अध्ययन करें (डॉक्टरेट शोध प्रबंध, ला लगुना विश्वविद्यालय)।

