एंडोथर्मिक प्रतिक्रियाओं के उदाहरण
उदाहरण / / November 09, 2023
ए एंडोथर्मिक प्रतिक्रिया यह एक ऐसी प्रतिक्रिया है जो माध्यम से ऊष्मा के रूप में ऊर्जा को अवशोषित करती है। इन प्रतिक्रियाओं में, अभिकारकों को उत्पादों में बदलने के लिए, यह आवश्यक है कि वे गर्मी को अवशोषित करें, जिसके कारण उत्पादों में उन अभिकारकों की तुलना में अधिक ऊर्जा होती है जो उन्हें जन्म देते हैं। एंडोथर्मिक प्रतिक्रियाओं के कुछ उदाहरण हैं: प्रकाश संश्लेषण और जल इलेक्ट्रोलिसिस।
- यह सभी देखें: रासायनिक प्रतिक्रिएं
रोजमर्रा की जिंदगी में एंडोथर्मिक प्रतिक्रियाओं के उदाहरण
कुछ मुख्य एंडोथर्मिक प्रतिक्रियाएं हैं:
वायुमंडल में ओजोन का उत्पादन. वायुमंडल में ओजोन का उत्पादन तब होता है जब आणविक ऑक्सीजन (O2) पराबैंगनी विकिरण को अवशोषित करता है और टूट जाता है। तब एक ऑक्सीजन परमाणु (O) दूसरे ऑक्सीजन अणु (O) के साथ परस्पर क्रिया कर सकता है2) और ओजोन बनाते हैं (O3).

जल इलेक्ट्रोलिसिस. यह वह प्रक्रिया है जिसके द्वारा इसे लागू किया जाता है विद्युत शक्ति पानी को उसके दो घटकों, हाइड्रोजन (H) और ऑक्सीजन (O) में अलग करने के लिए।
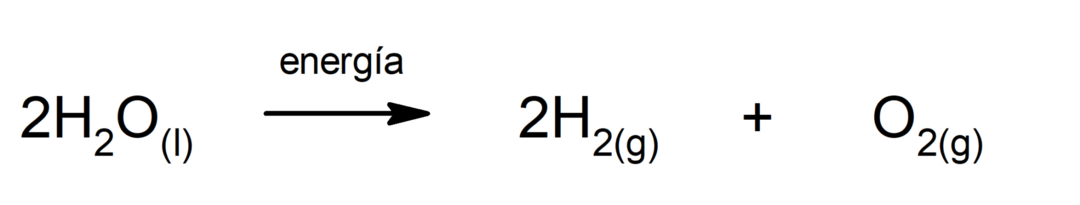
प्रकाश संश्लेषण. यह वह रासायनिक प्रतिक्रिया है जिसके द्वारा अवशोषण होता है सौर ऊर्जा
, कार्बन डाइऑक्साइड (CO2) ग्लूकोज में परिवर्तित हो जाता है। यह प्रतिक्रिया पौधों के पोषण का मुख्य मार्ग है।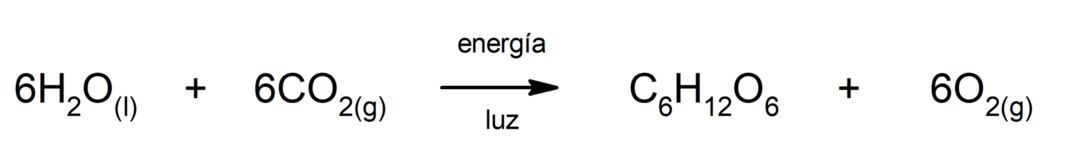
आयरन (II) सल्फाइड उत्पादन. सल्फर और लोहे के बीच प्रतिक्रिया होने के लिए ऊष्मा के रूप में ऊर्जा प्रदान करना आवश्यक है।
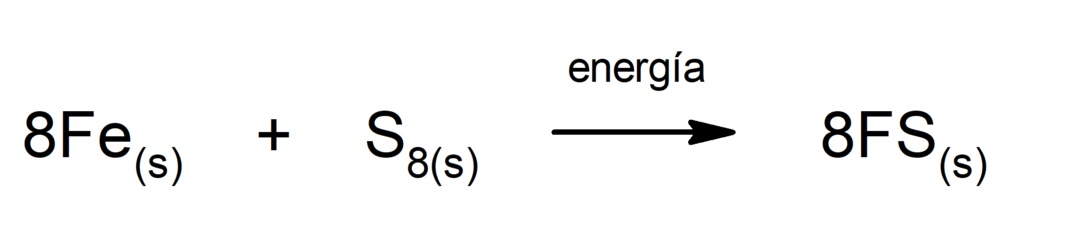
कार्बन डाइऑक्साइड का अपघटन (सीओ2). CO का अपघटन2 उच्च तापमान पर यह कार्बन मोनोऑक्साइड (CO) और ऑक्सीजन (O) पैदा करता है2).
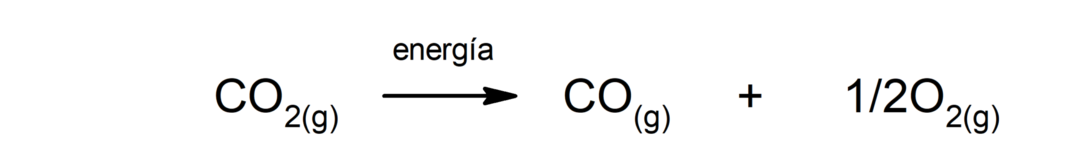
कैल्शियम कार्बोनेट का अपघटन (CaCO3). कैल्शियम कार्बोनेट गर्मी के अवशोषण के साथ विघटित होकर कैल्शियम ऑक्साइड (CaO) और कार्बन डाइऑक्साइड (CO) का उत्पादन करता है2).
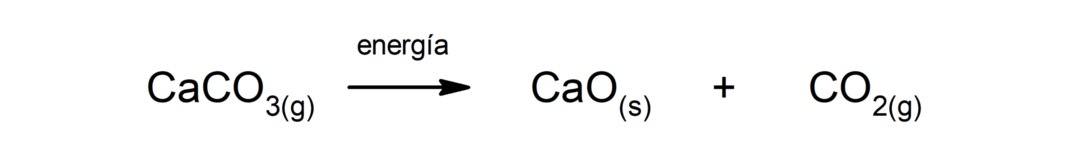
एंडोथर्मिक और एक्ज़ोथिर्मिक प्रतिक्रिया के बीच अंतर
एंडोथर्मिक और एक्ज़ोथिर्मिक प्रतिक्रियाओं के बीच मुख्य अंतर यह है कि एंडोथर्मिक प्रतिक्रियाएं गर्मी को अवशोषित करती हैं, जबकि एक्ज़ोथर्मिक प्रतिक्रियाएं गर्मी छोड़ती हैं।
इसके अलावा, एंडोथर्मिक प्रतिक्रियाएं एन्थैल्पी में वृद्धि के साथ जुड़ी होती हैं, जबकि एक्सोथर्मिक प्रतिक्रियाएं एन्थैल्पी में कमी के साथ जुड़ी होती हैं।
एन्थैल्पी एक थर्मोडायनामिक मात्रा है जो रासायनिक प्रतिक्रिया के दौरान स्थिर दबाव पर तापीय ऊर्जा के प्रवाह को परिभाषित करती है। इसे अक्षर H द्वारा दर्शाया जाता है, और इसकी भिन्नता यह परिभाषित करने के लिए मुख्य संकेतकों में से एक है कि कोई रासायनिक प्रतिक्रिया एंडोथर्मिक है या एक्ज़ोथिर्मिक।
- यदि किसी रासायनिक प्रतिक्रिया में एन्थैल्पी परिवर्तन शून्य से अधिक हो (ΔH > 0) एंडोथर्मिक है।
- यदि किसी रासायनिक प्रतिक्रिया में एन्थैल्पी परिवर्तन शून्य से कम हो (ΔH < 0) ऊष्माक्षेपी है।
साथ में पीछा करना:
- भौतिक-रासायनिक घटनाएँ
- रोजमर्रा की जिंदगी में रसायन विज्ञान
- रोजमर्रा की जिंदगी में रसायन विज्ञान
- कार्बनिक एवं अकार्बनिक रसायन
संदर्भ
- सोटो-कोर्डोबा, एस. (2016). एंडोथर्मिक प्रतिक्रियाएं। टेक रिपॉजिटरी कोस्टा रिका का तकनीकी संस्थान।
- कोरोमिनास, जे. (2017). रोजमर्रा की जिंदगी की रासायनिक प्रतिक्रियाएं। एलेम्बिक, (90), 8-26.
- सांचेज़, एम. टी। एम., और सांचेज़, एम. एम। (2002). ईएसओ छात्रों के लिए एंडोथर्मिक प्रतिक्रियाओं का प्रायोगिक अध्ययन. आरएसईक्यू के रसायन विज्ञान का इतिहास, (4), 36-39.