20 Primjeri kiselina
Miscelanea / / July 04, 2021
The kiseline čine važnu skupinu kemijski spojevi, vrlo široka. Kiseline su općenito definirane kao spojevi koji mogu donirati jedan ili više kationi vodik (H+) u drugi spoj, poznat kao baza. Iako se u stvarnosti kiseline definiraju prema nekoliko teorija:
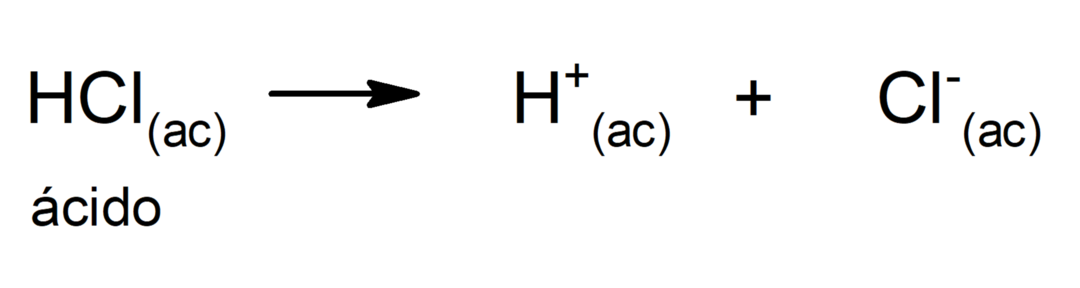 Ograničenje ove teorije je da se kiseline definiraju samo u vodenoj otopini.
Ograničenje ove teorije je da se kiseline definiraju samo u vodenoj otopini. 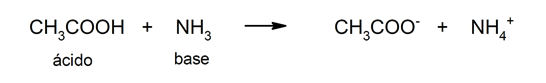

Svojstvo puštanja kationi vodika je ono zbog čega kiseline proizvode otopine pH manje od 7. Kiseline koje mogu osloboditi više od jednog protona (koristeći ovaj naziv za H+) nazivaju se poliprotični ili polifunkcionalni.
Svojstva kiseline
Glede njihovog Svojstva, kiseline se mogu predstaviti kao tekućine ili kao plinovi, rjeđe kao solidan. Kiseli okus koji možemo prepoznati i koji karakterizira ove spojeve nalazimo, na primjer, u limunsko voće, bogato limunskom kiselinom, ili ocat, koji je kisela otopina octena. To su organske kiseline.
postoje organske i anorganske kiseline; najjači su obično oni anorganski. Mnoge organske kiseline imaju važnu biološku ulogu. Među anorganskim postoji jedna, klorovodična kiselina, koja igra vrlo važnu ulogu u procesu probave. The
nukleinske kiseline Oni su također temeljni za život, jer su osnova genetskog materijala Stanice i sadrže ključ za sintezu protein.Tendencija gubitka protona je ono što određuje snagu kiseline.
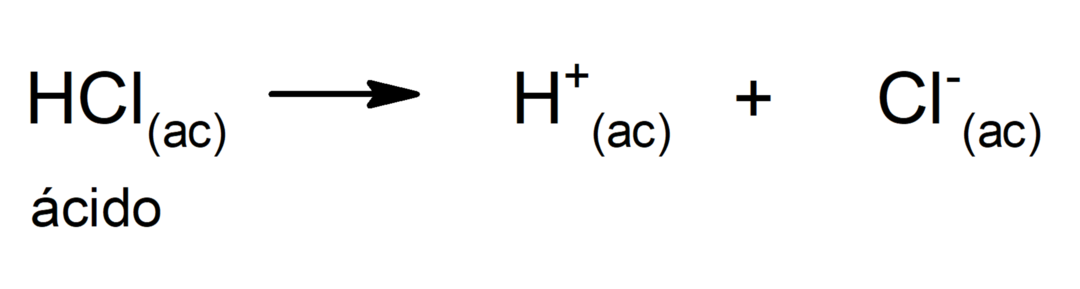
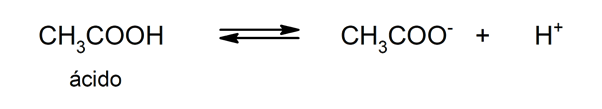
Upotreba kiselina
Kiseline imaju mnoge namjene, kako na industrijskoj tako i na domaćoj razini. Često se koriste kao aditivi i konzervansi u hrana, kozmetika, pića itd. Neke kisele čvrste tvari koriste se kao katalizatori (ubrzivači kemijskih reakcija) u petrokemijskoj ili papirnoj industriji.
Postoje i kiseline koje se koriste kao dezinficijensi (karbolna kiselina, salicilna kiselina). Osim toga, mogu se koristiti kao elektroliti u automobilskim akumulatorima, kao što je slučaj sa sumpornom kiselinom. Potonja jaka kiselina također se često koristi u preradi mineraliTakav je slučaj proizvodnje gnojiva iz kamenih fosfata.
Vrijedno je pojasniti da se određene tvari mogu otopiti samo u kiselim medijima i da se određene reakcije događaju samo u takvim uvjetima. Dušična kiselina i amonijak čine amonijev nitrat, također važno gnojivo za usjeve.
Primjeri kiselina
Dvadeset kiselina je navedeno u nastavku, kao primjer:
- Klorovodična kiselina (HClO4). To je jaka kiselinska tekućina a temperatura okoliš, jako oksidira.
- Dušična kiselina (HNO3). To je jaka i intenzivno oksidirajuća kiselina, koja se koristi za izradu određenih eksploziva, a također i dušičnih gnojiva.
- Askorbinska kiselina (C6H8ILI6). To je vitamin C, toliko potreban za zdravlje. Zaštitna je tvar zbog svojih antioksidativnih učinaka.
- Klorovodična kiselina (HCl(izmjenično)). To je jedina jaka kiselina koju ljudsko tijelo sintetizira, proces koji se posebno događa u želucu kako bi se izvršila razgradnja hrana u probavnom procesu.
- Vinska kiselina (C4H6ILI6). To je bijeli kristalni prah, koristi se u pripremi šumećih pića, u pekarstvu, vinskoj i farmaceutskoj industriji. Krema od zubnog kamenca koju nose neki recepti je vinska kiselina.
- Fluorovodonična kiselina (HF(izmjenično)). Zbog svoje sposobnosti napada staklo, koristi se u klesanju i graviranju.
- Sumporna kiselina (H2SW4). Jaka je kiselina par excellence, ima bezbroj primjena u raznim industrije i procesi sinteze.
- Trifluorooctena kiselina (C2VF3ILI2). Mnogima je dobro otapalo organski spojevi.
- Fosforna kiselina (H3PO4). Prisutan je (u niskim koncentracijama) u raznim cola napicima. Smatra se štetnim za zdravlje jer potiče dekalcifikaciju.
- Octena kiselina (CH3COOH). Glavna je komponenta octa. Kiselost koju stvara čini ga široko korištenim konzervansom hrane.
- Fluoroantimonska kiselina (SbHF6). To je najjača poznata superacid, koja za 10 puta premašuje kiselost čiste sumporne kiseline19.
- Kromna kiselina (H2CrO4). To je tamnocrveni prah, sudjeluje u procesu kromiranja. Također se koristi za glaziranje keramike.
- Indooctena kiselina (C10H9NE2). Glavni je predstavnik auksina, važnih za hormone rasta bilje.
- Deoksiribonukleinska kiselina (DNA). Ona je ta koja je ključ života, jer čini gene koji upravljaju sintezom bezbrojnih bjelančevina.
- Trikarboksilne kiseline. Sadrže skupinu karboksilnih kiselina koje imaju tri karboksilne skupine (-COOH). Limunska kiselina (C6H8ILI7) To je jedan od njih.
- Mravlja kiselina (CH2ILI2). Najjednostavnija je od organskih kiselina. Dugotrajno izlaganje ovoj kiselini može uzrokovati respiratorno zatajenje i smrt.
- Glukonska kiselina (C6H12ILI7). Soli ove kiseline naširoko se koriste u procesima čišćenja staklenog posuđa.
- Mliječna kiselina (C3H6ILI3). Važan je dio biokemijskih procesa.
- Benzojeva kiselina (C7H6ILI2). To je kiselina karakterističnog mirisa koja se naširoko koristi za konzerviranje hrane koja zahtijeva a pH kiselina.
- Jabučna kiselina (C4H6ILI5). Široko se koristi u farmaceutskoj industriji za proizvodnju laksativa.
- Ugljična kiselina (H2CO3). Ponegdje je to dio procesa formiranja špilja. Prisutan je u gaziranim pićima.

