Karakteristike halogena
Kemija / / July 04, 2021
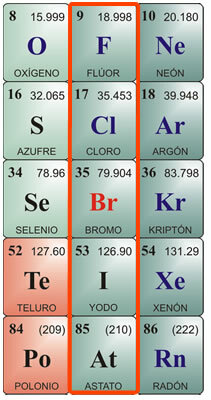
Halogeni su kemijski elementi koji se nalaze u skupini VIIA ili skupini 17 periodnog sustava. Sastoji se od elemenata fluor, klor, brom, jod i astat.
Naziv halogen potječe od grčkog i znači "proizvođač soli", jer ti elementi tvore soli s natrijem s karakteristikama sličnim uobičajenoj soli.
Zajedničke karakteristike halogena:
Oni su monovalentni elementi, odnosno imaju samo jedan valentni broj. U halogenima je valencija -1.
Imaju afinitet prema vodiku, tvoreći takozvane hidracide.
Imaju mali afinitet za kisik, pa ne stvaraju okside, već na vrlo visokim temperaturama.
Kombiniraju se s metalima da bi stvorili halogene soli.
Pojedinačne karakteristike halogena:
Karakteristike fluora:
Kemijski simbol F. Atomski broj 9, atomska težina 19. Fluor u čistom stanju je žuti plin, s talištem od -223 ° C i vrelištem od -187 ° C. Ne postoji besplatno u prirodi, pa mora biti izolirano. Prvi je put izoliran 1886. godine. Njegove fizičke karakteristike su: Zelenkasto-žuti plin, vrlo nagrizajući i nadražujući, oštrog mirisa, otrovan za ljude i životinje. Teško je ukapiti. Kemijske značajke: Kombinira se s vodikom, čak i na vrlo niskim temperaturama s egzotermnom reakcijom. Kombinira se s metalima, tvoreći soli. Razgrađuje klorovodičnu kiselinu, stvarajući klor, i razgrađuje vodu, oslobađajući kisik. Zbog afiniteta prema vodiku uzima ga iz organskih tvari, karbonizirajući ih. Jedan od njegovih glavnih spojeva je fluorovodonična kiselina, koja se može čuvati samo u posudama od platine ili voska, jer napada silicijum dioksid u staklu. Vrlo je hlapljiv i vrlo nagrizajući. U kombinaciji s metalima stvara fluoride.
Karakteristike klora:
Kemijski simbol Cl. Atomski broj 17, atomska težina 35,5. Talište - 102 ° C, vrelište -37 ° C. Klor je otkriven 1774. godine, a izoliran 1811. godine. Fizička svojstva: Riječ je o zelenkasto-žutom plinu koji u prirodi ne postoji slobodan, jer se uglavnom nalazi u kombinaciji s solima. Ima zadah i otrovni miris. Kemijska svojstva: Klor je vrlo sličan vodiku, kombinirajući se u egzotermnoj reakciji dajući solnu kiselinu. Klorovodična kiselina, koja se naziva i muriatska kiselina ili pušeća sol, bila je poznata još od starog Rima. Pronađen je u plinovitom stanju u vulkanima, a otopljen je u vodi nekih rijeka u blizini vulkana. Vrlo je nagrizajući za kožu i otrovan ako se proguta. Stvara ga želudac za probavu. Ostali važni spojevi klora su hipokloriti, posebno natrijev hipoklorit, koji se, kada se otopi u vodi, koristi kao sredstvo za izbjeljivanje vode, dezinficijens i steril. Neutralizira kiseline.
Karakteristike broma:
Kemijski simbol Br. Atomski broj 35, atomska težina 79,9. Talište -7,3 ° C, vrelište 58,8 ° C. U prirodi se ne nalazi slobodno, ali u kombinaciji s metalima stvara bromide. Izolira se elektrolizom. Fizička svojstva: To je tamnocrvena tekućina iritantnog mirisa; na sobnoj temperaturi daje iritantnu gustu narančasto-crvenu paru, uzrokujući kašalj i suzenje; Otrovno je. Otapa se u eteru ili kloroformu i teško se otapa u vodi. Kemijska svojstva: Brom napada organsku tvar; kod živih bića nagriza kožu i uzrokuje čireve koji se teško liječe. Njegova glavna upotreba kombinira se s metalima koji tvore bromide, koji se koriste u industrijske svrhe, poput srebrovog bromida, koji se prije koristio u fotografiji. Također se koriste u niskim koncentracijama kao antiseptik. U kombinaciji s vodikom rezultira bromovodičnom kiselinom, bezbojnim plinom oštrog mirisa i okusa, koji se uglavnom koristi za napad na metale i dobivanje bromida.
Značajke Jod:
Kemijski simbol I. Atomski broj 53, atomska težina 126,9. Točka topljenja 113 ° C; vrelište 184 ° C. Ne postoji besplatno u prirodi. Nalazi se kao jodidi u krevetima morskih algi i kao dio minerala u nekim namirnicama, poput potočarke, ulja bakalara i školjaka. Fizička svojstva: Jod je čvrsto, kristalno tijelo, crnkasto sive boje, metalnog sjaja, jakog i neugodnog mirisa. Slabo je topljiv u vodi i vrlo topljiv u alkoholu. Kemijska svojstva: Kombinira se s metalima tvoreći jodide; također s metaloidima, poput sumpora i fosfora. Ima veći afinitet za kisik od ostalih halogena. U kombinaciji s amonijakom stvara dušikov jodid, koji je eksplozivan plin. U kombinaciji s vodikom stvara jodovodnu kiselinu, bezbojni plin oštrog mirisa i okusa koji puši u prisutnosti zraka. Otapa se u vodi i razgrađuje pod djelovanjem svjetlosti i topline. Ako molekula kiseline sadrži kisik, tada nastaje jonska kiselina, koja je kristalna krutina s oksidacijskim svojstvima. Jod se koristi u alkoholnoj otopini kao dezinficijens i antiseptik.
Značajke Astatus:
Na simbolu. Atomski broj 85, atomska težina 210. Ne postoji besplatno u prirodi. Točka topljenja 254 ° C; vrelište 962 ° C. Astatin je prvi put sintetiziran četrdesetih godina prošlog stoljeća, jer je to element koji se alfa zrakama oslobađa od razgradnje atoma bizmuta. Radijski je element s vrlo kratkim životnim vijekom; izotop koji traje najduže je At210, s maksimalnim životnim vijekom od oko 8 sati. Smatra se da su njegova kemijska svojstva vrlo slična svojstvima joda; fizički bi mogao imati izgled i svojstva sličnija onima metala. Iako je radioaktivni element, ne predstavlja opasnost po zdravlje, jer se obično ne nalazi u prirodi. U laboratoriju ima samo nekoliko primjena za označavanje atoma u proučavanju subatomske tvari.



