Definisi Laju Reaksi dan Kesetimbangan Kimia
Bermacam Macam / / December 14, 2021
Definisi konseptual
Suatu reaksi berada dalam kesetimbangan kimia ketika laju reaksi maju sama dengan laju reaksi balik.

Insinyur kimia
Semua reaksi kimia memiliki spontanitas tertentu terhadapnya Keseimbangan, dan untuk menyelidikinya kita melakukannya melalui tanda G, Energi Gibbs free, yang menyiratkan bahwa, melalui nilai besarnya ini, kita dapat memprediksi apakah suatu reaksi akan terjadi dalam arti tertentu atau tidak.
Variasi Energi Bebas Gibbs dinyatakan, secara umum, dalam kondisi standar sebagai perbedaan antara energi produk dan reaktan juga dalam keadaan standar:
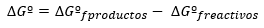
Sedangkan jika reaksi terjadi pada kondisi non-standar, hubungan antara Gº dan G ditentukan sebagai berikut: ekspresi:
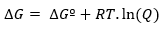
Dimana Q adalah hasil bagi reaksi.
Untuk memahami implikasi dari kecepatan reaksi dan kesetimbangan kimia kita harus mempelajari tanda G:
Jika G negatif, itu menyiratkan bahwa reaksi itu spontan (terjadi) dalam arti langsung.
Jika G positif, berarti reaksi tidak spontan (tidak terjadi) dalam arti langsung.
Sedangkan jika G = 0, tidak akan ada perubahan, karena sistem berada dalam kesetimbangan, dan seperti yang telah disebutkan, kecepatan Laju reaksi langsung sama dengan laju reaksi tidak langsung. Ini menyiratkan bahwa hasil bagi reaksi Q sama dengan konstanta kesetimbangan K, sehingga tidak ada kecenderungan untuk mendukung arah reaksi tertentu.
Karena Q didefinisikan sebagai:
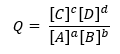
Untuk reaksi umum:
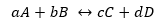
Sedangkan K mengambil bentuk yang sama, tetapi dengan konsentrasi dalam kesetimbangan.
Jika kita kembali ke kasus di mana G negatif, ini berarti bahwa hasil bagi reaksi Q lebih kecil dari K (konstanta kesetimbangan), menyiratkan bahwa konsentrasi produk lebih rendah dari yang seharusnya jika reaksi berlangsung Keseimbangan. Oleh karena itu, dalam hal spontanitas, menjadi spontan dalam arti langsung.
Sedangkan jika G positif, akan ada produk yang lebih banyak di atas yang seharusnya ada jika sistem berada dalam kesetimbangan, dengan Q lebih besar dari K. Oleh karena itu, reaksi spontan dalam arah sebaliknya.
Perlu dicatat bahwa definisi Q dan K yang ketat diberikan dalam hal aktivitas produk dan reaktan, mendefinisikan aktivitas dalam hal konsentrasi atau tekanan sebagai:
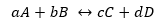
baiklah:
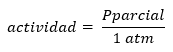
Dari sana dapat disimpulkan bahwa baik Q dan K tidak berdimensi dan dapat dinaikkan baik dalam konsentrasi maupun tekanan parsial.
Ketika konsentrasi atau tekanan parsial produk dan reaktan dijaga konstan dari waktu ke waktu, situasinya terjadi kesetimbangan kimia, sejauh situasi kesetimbangan dinamis tercapai karena laju reaksi langsung dan terbalik dengan identik. Penting untuk menyoroti dinamika keseimbangan, kecepatan pembentukannya dan mengkonsumsi produk dan reagen adalah sama, itulah sebabnya konsentrasi atau tekanan parsial tidak itu bervariasi.
Jika kondisi menjauh dari situasi kesetimbangan, spesies tertentu akan menang atas yang lain dan dari sana muncul ekspresi yang menghubungkan kecepatan reaksi langsung dan terbalik, Kc:
Misalkan reaksi yang terlihat di atas:
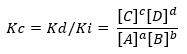
Dimana Kd dan Ki masing-masing adalah konstanta laju reaksi dalam arah maju atau mundur.
Sekali lagi, jika Kc> 1, ini menyiratkan bahwa Ki lebih kecil dari Kd, oleh karena itu, ada tingkat konversi yang tinggi dari produk menjadi reaktan. Dalam hal ini, kesetimbangan bergeser ke arah produk.
Kebalikannya terjadi jika Kc <1, menyiratkan bahwa laju reaksi langsung lebih kecil dari laju reaksi tidak langsung dan ada sedikit konsumsi reaktan, kesetimbangan bergeser ke arah reaktan. Sedangkan jika Kc = 1, kecepatannya sama dan sistem dalam keadaan setimbang. Penting untuk mendefinisikan dua masalah: pertama, nilai konstanta ini bergantung secara eksklusif pada suhu dan, pada gilirannya, bervariasi sesuai dengan besaran yang digunakan untuk menyatakan konsentrasi atau tekanan produk dan reaktan. Akhirnya, hukum Kesetimbangan kimia menyesuaikan untuk mengencerkan larutan atau gas di bawah tekanan rendah.
Topik dalam Laju Reaksi dan Kesetimbangan Kimia


