Caratteristiche dei lantanidi
Chimica / / July 04, 2021
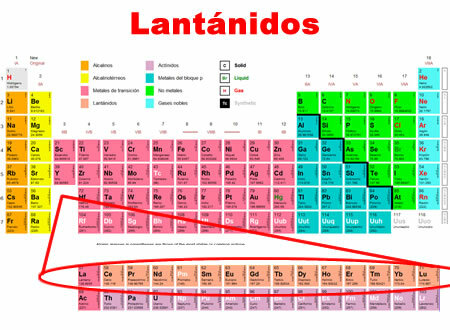
I lantanidi sono gli elementi chimici che vanno dal lantanio al lutezio. Condividono caratteristiche comuni, per cui sono classificati in una categoria speciale in fondo alla tavola periodica.
Principali caratteristiche dei lantanidi:
- Si trovano nel periodo 6 della tavola periodica.
- Coprono 15 elementi, dal 57 al 71.
- Condividono la struttura del Lantanio, a cui si aggiunge un livello energetico f, meno reattivo chimicamente.
- Sono state chiamate terre rare perché allo stato naturale sono sempre combinate per formare ossidi.
- Alcuni sono relativamente abbondanti.
- Sebbene abbiano valenze variabili, la maggior parte ha valenze +3.
- All'aumentare del suo numero atomico, il suo raggio diminuisce.
- Hanno tutti un aspetto metallico lucido.
Caratteristiche individuali dei lantanidi:
Lantanio (La).
- Numero atomico 57
- Peso atomico: 139
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 920 ° C
- Punto di ebollizione: 3457 ° C
Fu scoperto nel 1839. Nell'industria viene utilizzato in leghe con altri lantanidi per realizzare pietre più leggere; in ottica è utilizzato per vetri ottici. Viene utilizzato anche per le spugne di idrogeno, utilizzate per contenere i gas. In medicina viene utilizzato sotto forma di carbonato di lantanio, per il trattamento dell'insufficienza renale, poiché ha l'affinità di mescolarsi con i fostati, riducendo l'iperfosfemia.
Cerio (Ce)
- Numero atomico 58
- Peso atomico: 140
- Stato: Solido morbido
- Aspetto: metallico, grigio argento, simile al ferro
- Valencia: +3, +4
- Punto di fusione: 798 ° C
- Punto di ebollizione: 3426°C
Fu scoperto nel 1803. È il lantanide più abbondante. Viene utilizzato per realizzare catalizzatori, principalmente per automobili (convertitori catalitici) e per il cracking dell'olio. In forma di ossido viene utilizzato per lucidare occhiali e lenti. Sebbene non abbia funzioni biologiche note, in medicina viene utilizzato negli unguenti per ustioni.
Praseodimio (Pr)
- Numero atomico 59
- Peso atomico: 144
- Stato: Solido morbido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 931°C
- Punto di ebollizione: 3520 ° C
Fu scoperto nel 1841 e isolato nel 1885. Nell'industria viene utilizzato in leghe con magnesio per realizzare motori di aeroplani; Viene utilizzato per conferire un colore giallo a vetri e smalti. Le leghe di nichel hanno proprietà magnetiche. Reagisce con gli alogeni per produrre fluoruri, cloruri, bromuri e ioduri.
Neodimio (Nd)
- Numero atomico 60
- Peso atomico: 139
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1024 ° C
- Punto di ebollizione: 3100°C
Fu scoperto nel 1885, quando fu isolato il praseodimio; il neodimio fu isolato fino al 1925. È uno dei lantanidi più reattivi. Nell'industria viene utilizzato per colorare vetri e smalti. A causa della sua capacità di assorbire la luce, viene utilizzato in astronomia per creare cristalli con cui vengono calibrati spettrometri e filtri infrarossi. Uno dei suoi usi principali è quello di realizzare magneti ad alta intensità magnetica. Questi magneti vengono utilizzati per strumenti di precisione, come quelli utilizzati nei dischi rigidi dei computer, nonché per alcuni altoparlanti di formato sottile.
Promezio (Pm)
- Numero atomico 61
- Peso atomico: 145
- Stato solido
- Aspetto: ?
- Valencia: +3
- Punto di fusione: 1100°C
- Punto di ebollizione: 3000 ° C
La sua esistenza fu prevista nel 1902, ma non fu dimostrata fino al 1944. Questo lantanide non si trova in natura, essendo la fonte del suo ottenimento e studio della fissione dell'uranio. Quando la fissione dell'uranio in un reattore nucleare, uno degli atomi prodotti da questa separazione atomica è il promezio. Ha caratteristiche radioattive, che gli conferiscono fosforescenza, e viene utilizzato per calibratori e batterie nucleari utilizzate nei veicoli spaziali.
Samario (Mm)
- Numero atomico 62
- Peso atomico: 150
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1072°C
- Punto di ebollizione: 1803°C
Fu scoperto nel 1853 e isolato nel 1879. Ha diversi isotopi e almeno due di loro sono radioattivi. Nell'industria viene utilizzato nell'ottica per realizzare cristalli che assorbono la luce infrarossa. Viene anche usato come catalizzatore per ottenere alcol e come elemento in alcune lampade fluorescenti e televisori. Quanto alla salute, se inalato (come l'ossido usato per lucidare i cristalli), può provocare embolie polmonari o danneggiare il fegato. Gli isotopi radioattivi sono utilizzati nella radioterapia dei pazienti terminali.
Europio (Ue)
- Numero atomico 63
- Peso atomico: 152
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +2, +3
- Punto di fusione: 826°C
- Punto di ebollizione: 1527 ° C
Fu scoperto nel 1890. È il più reattivo dei lantanidi. È stato utilizzato in lampade fluorescenti e televisori, tuttavia per causare embolia polmonare se lo è inalato o danneggia il fegato se accumulato nel corpo umano, non ha quasi nessun uso industriale. Nella ricerca atomica viene utilizzato poiché assorbe i neutroni.
Gadolinio (Gd)
- Numero atomico 64
- Peso atomico: 157
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1312°C
- Punto di ebollizione: 3250 ° C
Il Gadolinio ha pochi usi, il principale dei quali è la refrigerazione industriale magnetica, poiché aumenta le sue proprietà magnetiche alle basse temperature; ma poiché questo tipo di refrigeratori richiede l'uso di arsenico, non vengono utilizzati nella refrigerazione domestica. In medicina viene utilizzato come mezzo di contrasto per la risonanza magnetica nucleare.
Terbio (Tb)
- Numero atomico 65
- Peso atomico: 159
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +4
- Punto di fusione: 1356°C
- Punto di ebollizione: 3230 ° C
Fu scoperto nel 1843 e isolato nel 1905. È molto importante nell'industria elettronica, in quanto è uno degli elementi utilizzati per realizzare i semiconduttori. Altri usi sono per realizzare tubi fluorescenti e cinescopi. È anche usato come catalizzatore nelle celle a combustibile. Sebbene non abbia funzioni biologiche, la sua inalazione o ingresso nel corpo umano ha effetti tossici, che colpiscono principalmente il fegato.
Disprosio (dy)
- Numero atomico 66
- Peso atomico: 162,5
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +2, +3
- Punto di fusione: 1407 ° C
- Punto di ebollizione: 2567 ° C
Fu scoperto nel 1843 e isolato nel 1905. È molto importante nell'industria elettronica, in quanto è uno degli elementi utilizzati per realizzare i semiconduttori. Altri usi sono per realizzare tubi fluorescenti e cinescopi. È anche usato come catalizzatore nelle celle a combustibile. Sebbene non abbia funzioni biologiche, la sua inalazione o ingresso nel corpo umano ha effetti tossici, che colpiscono principalmente il fegato.
Olmio (Ho)
- Numero atomico 67
- Peso atomico: 166
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1474 ° C
- Punto di ebollizione: 2700°C
Fu scoperto nel 1878 e il suo nome deriva dalla città della sua scoperta, Stoccolma, in latino, Holmia. Non ha quasi nessun uso pratico; tuttavia, viene utilizzato in alcune industrie come catalizzatore per reazioni chimiche, oltre che per alcuni componenti elettronici. Viene anche utilizzato per modificare la frequenza e l'intensità del raggio laser.
Erbio (Er)
- Numero atomico 68
- Peso atomico: 167
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1795 ° C
- Punto di ebollizione: 2863°C
Fu scoperto nel 1843. È usato nell'industria nucleare come tampone di neutroni. In forma di ossido è un colorante per i cristalli, che conferisce loro una tonalità rosa; Questi cristalli sono utilizzati nell'ottica e nella gioielleria. Viene anche utilizzato per realizzare fibre ottiche.
Tulio (Tm)
- Numero atomico 69
- Peso atomico: 167
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1545 ° C
- Punto di ebollizione: 1947 ° C
Fu scoperto nel 1879. Nonostante la sua scarsa disponibilità, a causa delle sue caratteristiche radioattive, il suo utilizzo principale è come sorgente di raggi X in apparecchiature portatili e per laser a stato solido.
Itterbio (Yb)
- Numero atomico 70
- Peso atomico: 173
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 824 ° C
- Punto di ebollizione: 1194 ° C
Fu scoperto nel 1878 e isolato nel 1907. Gli isotopi radioattivi vengono utilizzati per apparecchiature a raggi X portatili che funzionano senza elettricità. Viene anche utilizzato per migliorare le leghe di acciaio e aumentarne la resistenza, caratteristica che viene utilizzata in odontoiatria, grazie al miglioramento delle proprietà meccaniche dell'acciaio. Deve essere maneggiato con cura in quanto può causare irritazioni e ustioni. Inoltre, quando reagisce con l'aria, può causare un'esplosione o un incendio.
Lutezio (Lu)
- Numero atomico 71
- Peso atomico: 175
- Stato solido
- Aspetto: metallico, bianco argento
- Valencia: +3
- Punto di fusione: 1652°C
- Punto di ebollizione: 3402°C
Fu scoperto nel 1907. È l'elemento chimico meno abbondante nella crosta terrestre. Nonostante la sua scarsa disponibilità, viene utilizzato per la raffinazione del petrolio e come catalizzatore per reazioni di chimica organica. Alcuni isotopi radioattivi sono stati testati anche per i trattamenti di radioterapia.
