Esempio di chimica organica
Chimica / / July 04, 2021
Il Chimica organica è la parte di Chimica Generale che si occupa dello studio e della classificazione funzionale dei composti chimici il cui elemento strutturale è il Carbonio, presente in abbondanza nel materia vivente; si crea così un universo ben distinto dalla Chimica Inorganica, dedicato ai composti chimici classificati come minerali.
L'atomo di carbonio ha quattro elettroni nell'ultimo guscio della sua configurazione elettronica. Questa caratteristica, insieme a quella del suo raggio atomico, gli permette di essere legato da legami covalenti ad altri atomi dello stesso elemento, in numerose catene, formando una grande diversità di composti chimici stabile.
Puoi controllare Legami covalenti.
Tali composti chimici, oltre agli atomi di carbonio che conferiscono loro la struttura primordiale, contengono atomi di idrogeno come principale complemento della valenza del carbonio. Inoltre, in questa diversità di composti, ci sono quelli con l'intervento di atomi di ossigeno, Azoto, Alogeni, Zolfo e persino Fosforo, elementi alcalini e alcalino terrosi e metalli di transizione. A seconda di chi è coinvolto nella molecola, saranno le proprietà fisiche e chimiche della sostanza finale.
Il composti organici sono presenti in tutto il materia vivente; promuovere e sostenere tutti funzioni biologiche, a differenza delle sostanze inorganiche o minerali, che sono state utilizzate dall'uomo per scopi commerciali, per la sperimentazione o per svolgere determinati compiti domestici.
Storia della chimica organica
Prima del 1828 si faceva già la distinzione tra Chimica Organica e Chimica Inorganica. La materia organica è stata associata a una creazione attraverso a "forza vitale", e all'inorganico con il non vivente, con il minerale. Date queste concezioni, non ci si poteva aspettare di ottenere composti organici da materiali inorganici in laboratorio.
Tuttavia, nel 1828 Friedrich Wöhler (1800-1882) riuscì a preparare una sostanza organica, Urea CO (NH2)2, un importante prodotto del metabolismo animale, da composti inorganici. Trattamento Cianato di piombo Pb (CNO)2 con ammoniaca NH3 ottenere Cianato di ammonio NH4CNO; Questo composto si è formato, infatti, ma quando la soluzione è stata fatta bollire per cristallizzare l'ammonio cianato, si è trasformata in urea.
Questo cambiamento chimico è un esempio di Raggruppamento interno, in cui non cambia il numero o la classe degli atomi nella molecola, ma solo il loro ordine al suo interno. Questi tipi di trasformazioni sono molto comuni nella chimica organica.
La scoperta di Wöhler ha avviato l'abbandono della teoria della forza vitale, in seguito completamente scartato venendo seguito dalla preparazione di molti altri composti organici nel laboratorio. Nonostante ciò, sussistono le qualificazioni di Inorganico e Organico, poiché i composti inorganici sono correlati ai prodotti minerali ei composti organici, che sono in realtà composti di carbonio e idrogeno e loro derivati, sono del tipo prodotto dagli organismi viventi.
Sebbene le leggi della chimica generale si applichino ugualmente a entrambi i composti, varie cause giustificano e rendono necessaria questa divisione. Pertanto, i composti organici e inorganici differiscono in diverse proprietà, come ad esempio: la loro solubilità preferito in solventi organici (etere, alcool, cloroformio, ecc.) e in acqua, rispettivamente, la sua Stabilità (i composti organici si decompongono a temperature relativamente basse), e il Carattere delle reazioni; per i composti inorganici sono ionici, semplici e praticamente istantanei, e per i composti organici sono covalenti, complessi e lenti.
Composti organici
Sono noti composti di carbonio con catene fino a novanta atomi. Il Catene Gli atomi di carbonio possono essere lineare e ramificato e hanno legami covalenti singoli o legami doppi o tripli. È noto che più di 2.500 composti contengono solo carbonio e idrogeno (Idrocarburi).
Isomeria dei composti organici
Nei composti inorganici, una formula rappresenta generalmente un singolo composto; quindi, c'è solo una sostanza di formula H2SW4. La molecola di acido solforico contiene due atomi di idrogeno, uno di zolfo e quattro di ossigeno, in una disposizione specifica e unica. Nei composti organici è raro che ciò accada. Così, ad esempio, ci sono due composti che rispondono alla formula C2H6Oppure, alcol etilico o etanolo e etere dimetilico.

Più complessa è la molecola, cioè maggiore è il numero di atomi di carbonio, maggiore è il numero di possibili isomeri.
Analisi dei composti organici
L'analisi di un composto organico comprende la analisi qualitativa, il analisi quantitativa e il Analisi funzionale. Nel caso in cui si supponga che il composto sia in uno stato impuro, viene preventivamente purificato mediante Cristallizzazione, Distillazione, sublimazione, Estrazione, eccetera. Il criterio di purezza può essere giudicato in base alle sue costanti fisiche, come punto di fusione, punto di ebollizione, densità, solubilità, forma cristallina, indice di rifrazione, ecc.
Il analisi qualitativa Si verifica indagando la presenza degli elementi che compongono il composto, in particolare Carbonio, Idrogeno e Azoto, e talvolta Alogeni, Zolfo e Fosforo.
Il analisi quantitativa Viene effettuato utilizzando come base i metodi utilizzati per l'analisi qualitativa. Il punto di partenza è una certa quantità di sostanza che va incontro a combustione, e l'anidride carbonica viene raccolta e pesata. carbonio e vapore acqueo formati per calcolare la percentuale di carbonio e idrogeno nel composto. I risultati dell'analisi quantitativa facilitano il calcolo del formula empirica, sebbene la formula molecolare possa essere trovata solo dopo la determinazione del peso molecolare della sostanza. Ma il problema non è ancora risolto, perché la stessa formula molecolare può corrispondere a diversi isomeri.
Classificazione dei composti organici
In base alla loro struttura, i composti organici sono divisi in composti alifatico, aromatico sì eterociclico. I composti alifatici sono legati al metano CH4, sono a catena aperta, ad eccezione delle cicloparaffine, e devono il loro nome al fatto che i grassi animali e vegetali appartengono a questo gruppo.
Il composti aromatici, catena chiusa, strettamente imparentato con il benzene, C6H6, e devono il loro nome al fatto che molti di loro hanno odori fragranti e gradevoli.
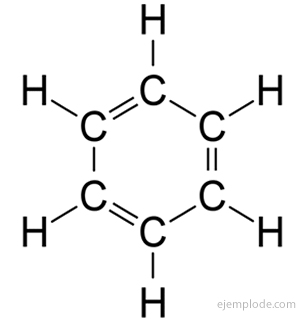
Anello del benzene
Il composti eterociclici Sono composti a catena chiusa in cui nell'anello è presente un elemento diverso dal carbonio.
Per loro costituzione, sono:
Idrocarburi, che a sua volta, per il tipo di collegamenti che possiede, è classificato come alcani, alcheni sì alchini. Inoltre rientrano in questa categoria i Cicloalcani, il Benzene e i loro derivati costituiti solo da Carbonio e Idrogeno.
Composti eterociclici
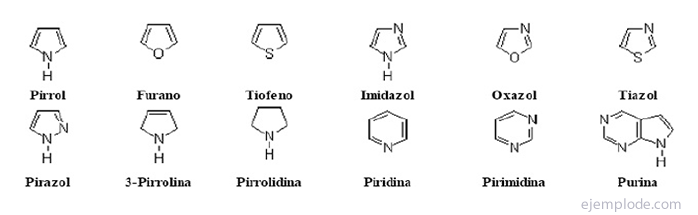
Derivati alogenati:R-X
Nitrocomposti:R-NO2
Acidi solfonici:R-SO3H
Nitrili (OR alchilcianuri) e isonitrili:R-CN e R-NC. Differiscono nel modo in cui l'atomo di azoto è legato nella molecola.
Alcoli:R-OH
Fenoli: Composti basati su uno scheletro costituito da un anello benzenico con l'aggiunta di un gruppo ossidrile.

Eteri:R-O-R
Mercaptani: R-SH
tioeteri:R-S-R
Tioacidi:R-COSH
Aldeidi:R-CHO
Chetoni:R-CO-R
Acidi carbossilici:R-COOH
Esci:R-COOM (M per metallo)
Esteri: R-COO-R
Anidridi: R-CO-O-OC-R
ammine:R-NH2, R-NH-R, 2R-N-R
Carboidrati tipo Aldosa:-CHOH-CHOH-CHO
Carboidrati di tipo chetosio:-CHOH-CO-CH2Oh
Composti organometallici:R-M-R
Alogenuri metallo-alchilici:R-MX (noto anche come reagenti di Grignard)


