Esempio di gas ideali e reali
Fisica / / July 04, 2021
UN gas ideale è quello le cui proprietà come Pressione, temperatura e volume coperti, mantengono sempre una proporzione o un rapporto costante tra loro. In altre parole, il suo comportamento segue la Legge dei Gas Ideali, che è rappresentata come segue:
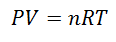
Per arrivare a questa formula si parte da La Legge generale dello stato gassoso, che descrive che esiste una relazione costante tra le proprietà del gas in ogni momento in un processo. Le proprietà di cui si parla sono le Pressione nel sistema in cui si trova il gas, il Volume che occupa il gas, e il Temperatura di gas.
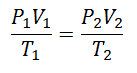
Si decise prima o poi di formare un'espressione più semplice, dando alla costanza una lettera per accompagnare l'espressione:
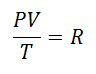
Era chiamato Costante universale di gas al fattore R, e il suo valore è il seguente:
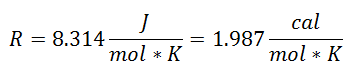
E poiché la costante universale dei gas si applica per ogni mole del gas, il, Numero di moli di gas come un ulteriore fattore, per coprire tutta la sostanza presente nell'impianto durante il processo. Avremo già l'equazione finale in questa forma:
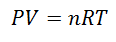
L'equazione di cui sopra è Legge dei gas perfetti, e si applica ai gas che si trovano a una temperatura compresa tra moderata e alta. Pertanto, una qualsiasi delle variabili può essere calcolata, determinando le altre.
Differenza tra gas ideali e gas reali
Questa legge del gas ideale Non si applica per i gas che sono a basse temperature o vicino al punto in cui diventano liquidi.
Le basse temperature provocano a meno movimento delle particelle gas, e questi si depositeranno maggiormente, occupando un volume diverso rispetto a quando erano completamente dispersi.
Inoltre, per lo stesso motivo, eserciterebbero a Pressione irregolare in tutto il sistema. La proporzionalità inizierà a fallire e la formula non avrà la stessa validità per i calcoli.
In tal caso, dovrebbero essere utilizzate le equazioni per i gas reali.
UN Gas reale è quello le cui proprietà non si adeguano nel relazionarsi esattamente come nella Legge dei Gas Ideali, quindi il modo di calcolare queste proprietà viene modificato.
Equazioni di stato per gas reali
1.- Equazione virale:
Per un gas che resta a Temperatura costante, il rapporto tra Pressione e Volume o Pressione e volume specifico (volume occupato da ciascuna unità di massa del gas).
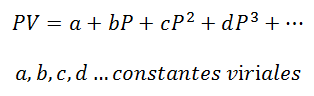
Le costanti virali sono caratteristiche di ciascun gas, con valori specifici che dipendono dalla Temperatura.
È possibile eseguire solo calcoli di pressione e volume; La temperatura è determinata in precedenza osservando il processo. Per questi calcoli vengono azzerate le variabili dell'equazione viriale:
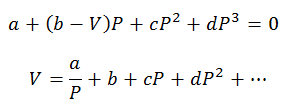
Le costanti del viriale per risolvere le equazioni sono ottenute da tabelle specializzate.
2.- EquazioneVan der Waals su:
L'equazione di Van der Waals è un'altra espressione utilizzata per calcolare le proprietà di un gas reale e, come l'equazione del viriale, richiede anche le sue costanti:

Le costanti vengono interrogate anche nelle tabelle.
3.- EquazioneLeone Rossoch-Kwong:
Questa equazione funziona molto bene per fare calcoli con gas a quasi tutte le temperature e pressioni medie, ma senza essere troppo alte, come centinaia di atmosfere.
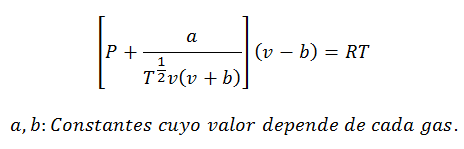
Le costanti vengono interrogate anche nelle tabelle.
Puoi cancellare la pressione, la temperatura e il volume per fare i tuoi calcoli. Rimangono le autorizzazioni:
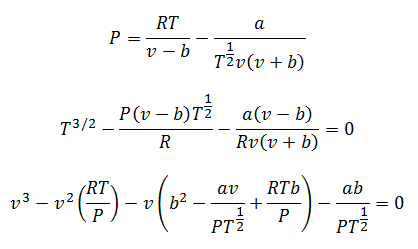
4.-Equazione di Berthelot:
È possibile calcolare qualsiasi variabile con questa equazione. Solo ha due diverse modalità: per basse pressioni e per alte pressioni.
Per basse pressioni:

Per alte pressioni:
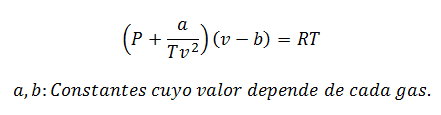
Le costanti vengono interrogate anche nelle tabelle.
5.-Equazione del fattore di comprimibilità
Questa equazione è una variante più semplice della legge dei gas ideali; viene aggiunto solo il fattore "z", detto Fattore di Comprimibilità. Questo fattore si ottiene dal Grafico del Fattore di Comprimibilità Generalizzato, in funzione della Temperatura, della Pressione o del Volume specifico, a seconda di quanto disponibile.
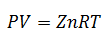
Esempi di gas ideali e reali
Come il personaggio ideale o reale Dipende dalle condizioni di Pressione, Temperatura in cui si trova il Gas, Non è possibile stabilire un elenco limitato, quindi viene presentato un elenco di gas, che ovviamente può essere trovato nell'idealità e nella realtà.
- Ammoniaca
- Refrigerante R134 (DiFluoroDiCloro Etano)
- Diossido di carbonio
- Monossido di carbonio
- Ossigeno
- Azoto
- Idrogeno
- Diossido di azoto
- Triossido di diazoto
- Pentossido di diazoto
- Eptossido di diazoto
- Diossido di zolfo
- Triossido di zolfo
- Cloro
- Elio
- Neon
- Argon
- Krypton
- Xeno
- Metano
- Etano
- Propano
- Butano