15 דוגמאות לדיפוזיה ואוסמוזה
Miscellanea / / July 04, 2021
ה דיפוזיה ואוסמוזה הם תהליכים של תחבורה פסיבית (הם אינם דורשים אנרגיה נוספת כדי להתרחש, בניגוד להובלה פעילה) של חלקיקים של אחד או יותר חומרים נמצא בריכוזים שונים של מומס והם נמצאים במגע אחד עם השני, דרך קרום חדיר למחצה (מקרה מסוים של אוסמוזה) או דרך אחרת.
מה זה שידור?
דיפוזיה היא א תהליך פיזי המבוסס על זרימת חלקיקים של חומר מאזור בעל ריכוז גבוה של מומס לקראת ריכוז נמוך, עד שהריכוז זהה בערך בשניהם אזורים. תנועת החלקיקים מבוססת על שלהם אנרגיה קינטיתבמילים אחרות, אין קלט אנרגיה חיצוני להופעת דיפוזיה. לדוגמה: מעבר חמצן בכליות הריאות.
תנועה זו מתרחשת בכל אחד מה- מצבי צבירה של ה חוֹמֶר, אך הוא נצפה ביתר קלות במקרה של נוזלים וגזים. הנטייה של התנועה היא להיווצרות של a לְעַרְבֵּב אחיד משני סוגי החלקיקים.
המדען אדולף הפכפך הקים בשנת 1855 כמה חוקים הנושאים את שמו, ומתארים מקרים שונים של התפשטות החומר במדיום שבתחילה אין שיווי משקל. חוקים אלה מתייחסים ל צְפִיפוּת של זרימת החלקיקים עם הפרש הריכוז בין שני המדיה הנפרדת, המקדם שלה דיפוזיה וחדירות של הממברנה (במקרה והמדיום המפריד הוא קרום למחצה).
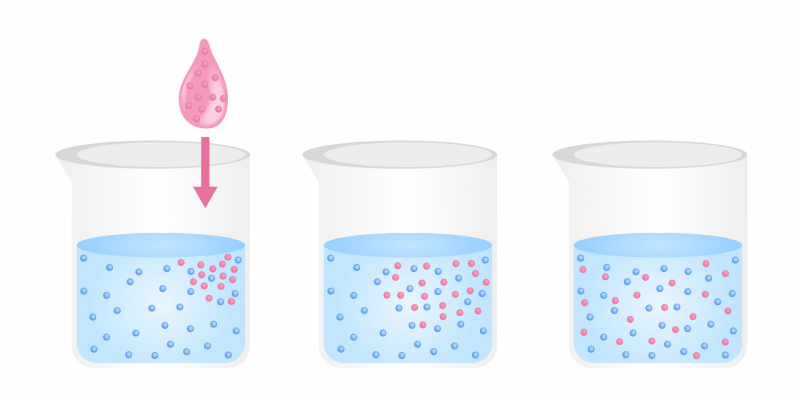
דוגמאות לדיפוזיה
- מעבר חמצן בכליות הריאות.
- דחפים עצביים, הכוללים יונים נתרן ואשלגן על פני קרום האקסונים.
- אם אתה לוקח זוג מפזר המורכב משניים מתכות מובאים במגע דרך פניהם, הם מחוממים מעל נקודת ה היתוך ואז להתקרר, יוודא שההרכב השתנה: התרחשה דיפוזיה של אטומי ניקל לעבר נחושת ולהיפך.
- ההתחממות ושינוי הצבע של כוס קפה כשמוסיפים חלק ניכר מחלב קר.
- כניסת הגלוקוז לתאי הדם האדומים, המגיעה מהמעי.
- בשפך, יש דיפוזיה פחות צפופה של מי נהר שזורמים מעל מים מ יָם.
- אם שמים כף סוכר בכוס מים, מולקולות של סוכרוז מפוזר במים.
- ניתן לראות פיזור גזים כאשר אדם מבושם נכנס למקום סגור, וכולם חשים מיד את הריח. אותו דבר קורה כשמישהו מעשן בתוך הבית.
מהי אוסמוזה?
אוסמוזה מהווה סוג של דיפוזיה, אך עם שני מאפיינים מסוימים:
באופן זה נצפה כי הממיס נוטה לעבור דרך הממברנה לכיוון ה- התפרקות שריכוזם גבוה יותר, אשר בסופו של דבר מייצר עלייה בכמות הממיס בחלק המרוכז ביותר (במומס) וירידה בכמות חלק פחות מרוכז (במומס), כלומר הממס נע מהאזור עם הריכוז הנמוך ביותר במומס לאזור עם הריכוז הגבוה ביותר מומס. זהו תהליך שחוזר על עצמו עד שריכוז התמיסה (המומס והממיס) שווה משני צידי הקרום.
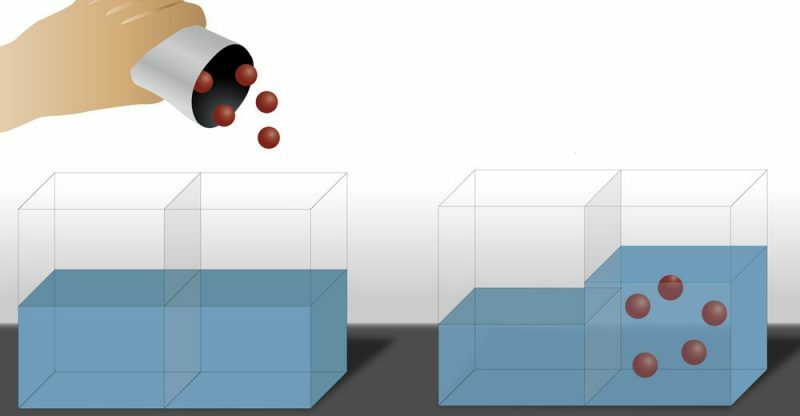
יש גם את אוסמוזה הפוכה, שם המעבר של הממיס מתרחש בכיוון ההפוך מאוסמוזה קונבנציונאלית, כלומר הממס עובר מהמיסה מרוכז יותר במומס לפחות מרוכז במומס. כדי להשיג זאת, מופעל לחץ על הפתרון מרוכז יותר במומס.
כי זה חשוב?
ה מְסִיסוּת המומס בממיס ואופי הקרום החדיר למחצה שישמש הם הגורמים הבסיסיים הקובעים את היעילות של התהליך האוסמוטי: אחד הגורמים המשפיעים על מה שמכונה 'מסיסות' הם האינטראקציות בין מרכיבי התפרקות.
ה תהליך אוסמוטי זה חיוני בתהליכים ביולוגיים שבהם המים הם הממס, במיוחד בתהליכים שמטרתם לשמור על איזון המים והאלקטרוליטים בתוך יצורים חיים, ויסות מפלסי המים בתא או בגוף באופן כללי: ללא תהליך זה, לא יכולה להיות שום ויסות של נוזלים וספיגה של חומרים מזינים.
דוגמאות לתהליך האוסמוזה
- יצורים חיים חד תאיים החיים במים מתוקים נכנסים לכמויות גדולות של מים.
- ספיגת מים על ידי השורשים באורגניזמים צמחיים, המאפשרת צמיחה.
- השגת מים מתאי האפיתל במעי הגס.
- פיצלו תפוח אדמה, הניחו מעט סוכר עם מים בקצה אחד וצלחת עם מים בצד השני. תפוח האדמה משמש כממברנה, ולאחר זמן מה נראה כי בתמיסה שיש בה סוכר יש כעת יותר נוזלים.
- הורמון ADH המאפשר ספיגה מחודשת של מים על ידי צינור האיסוף בכליות.
- חיסול שתן מדולל מאוד לפיו הדגים מוציאים את הנוזל המרבי עם אובדן מינימלי של אתה יוצא.
- חיסול מים בזיעה אצל אנשים.
- מסננים לטיהור מים עובדים עם אוסמוזה הפוכה, מכיוון שהם מיוצרים עם חוֹמֶר המאפשר מעבר של מים, אך לא של מולקולות גדולות יותר.
לעקוב עם:


