20 화학 염기의 예
잡집 / / July 04, 2021
라 불려진다 화학 염기 물에 용해되면 하이드 록실 이온 (OH–). 예를 들면 : 수산화칼슘, 수산화 구리, 수산화 아연.
화학 염기는 알칼리, 수산기 (OH)를 해리하고 방출함으로써–), pH 즉 용액이 알칼리성이됩니다. 이것은 산,이 경우 pH가 감소하고 용액이 산성이되기 때문입니다.
기지에는 쓴 맛 특성. 그의 후 해산, 결과 용액은 (이온의 존재로 인해) 전류를 전도하고 일반적으로 피부와 기타 인간 및 동물 조직에 부식성이며 자극적입니다.
기지 산을 중화시키다, 종종 형성 너 나가. 알칼리 용액은 미끄 럽거나 비눗물을 느끼는 경향이 있습니다. 이것은 그들이 즉시 비누화를 생산하기 때문에 발생합니다. 지방 피부 표면에 존재합니다.
수산화물의 경우 용해도 에 달려있다 금속: 그룹 (I)의 것들은 물에 가장 잘 용해되는 반면, 다음과 같은 원소의 수산화물은 산화도 (II)는 덜 용해되고 산화도 (III) 또는 (IV)는 거의 불용성. 아민 및 염기 핵산 그들은 유기물 중에서 가장 널리 퍼진 기지입니다.
기초를 정의하는 이론
화학적 염기를 정의하는 이론에는 여러 가지가 있습니다.
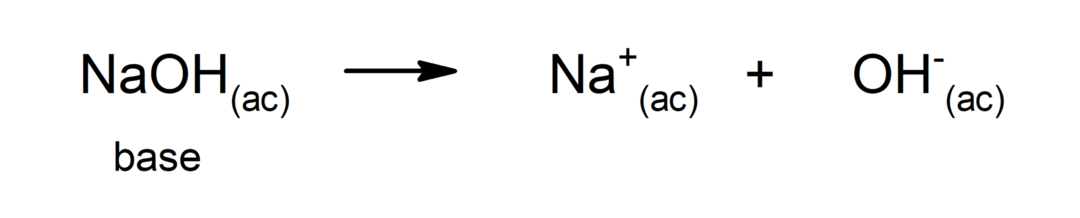
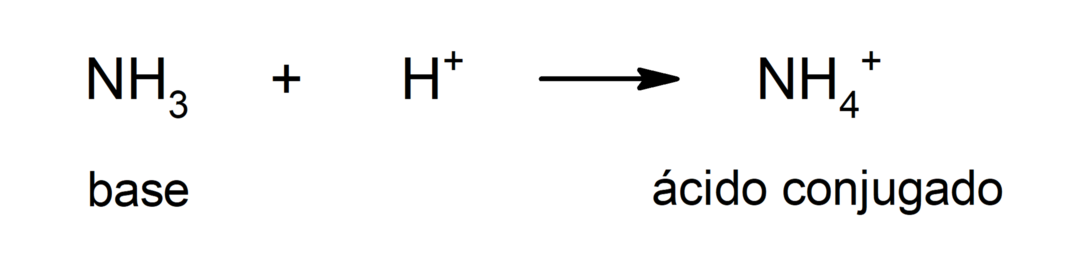

그래서 OH 이온–비 결합 전자쌍을 H+좌표 또는 dative 유대를 형성하기 위해 (그것은 유형의 공유 결합 어디에 하나만 원자 결합을 형성하는 것은 물 분자가 형성되는 전자 쌍을 제공합니다.
기지의 용도
그만큼 수산화 나트륨 그것은에서 널리 이용됩니다 산업: 이른바 가성 소다입니다. 비누 제조에서 지방 삶은 동물이나 야채 수산화물 나트륨 및 따라서 나트륨 스테아 레이트가 형성됩니다.
수산화 나트륨은 오븐 클리너 제조, 종이 펄프 제조 및 일부 가정용 클리너에도 사용됩니다. 널리 사용되는 또 다른 염기는 건축에 사용되는 소석회 인 수산화칼슘입니다.
화학 염기의 예
- 수산화칼슘-Ca (OH) ₂
- 수산화 칼륨-KOK
- 수산화 바륨-Ba (OH) ₂
- 수산화 마그네슘-Mg (OH) ₂
- 암모니아-NH₃
- 수산화 구리 (II)-Cu (OH) ₂
- 수산화철 (II)-Fe (OH) ₂
- 수산화 알루미늄-AI (OH) ₃
- 수산화 아연-Zn (OH) ₂
- 수산화 나트륨-NaOH
- 수산화 니켈 (II)-Ni (OH) ₂
- 세제 비누




