20 Cheminių reiškinių pavyzdžiai
Įvairios / / July 04, 2021
The cheminiai reiškiniai (arba cheminės reakcijos) yra tie reiškiniai, kuriuose vyksta medžiagos pokyčiai, susidaro naujos medžiagos, vadinamos „produktais“, o kitos, vadinamos „reagentais“, suyra. Pavyzdžiui: medienos puvinys, popieriaus deginimas, kompostavimas.
Cheminės reakcijos gali būti spontaniškas (reakcijos, vykstančios be energijos ar katalizatorių) arba nėra spontaniškas (reakcijos, kurioms gali prireikti energijos, katalizatorių ar kokio nors išorinio įsikišimo). Daug kartų, norint įvykti reakcija, būtina, kad reagentai turėtų a temperatūra specifinis, a pH nustatyta slėgio vertė ir kt.
Taip pat gali būti būtina kontroliuoti greitis į kurias vyksta cheminės reakcijos. The katalizatoriai Tai yra medžiagos, kurios pridedamos prie cheminės reakcijos, kad padidėtų jos greitis, o inhibitoriai - medžiagos, sulėtinančios cheminių reakcijų greitį. Kiti veiksniai, turintys įtakos cheminės reakcijos greičiui, yra temperatūra, slėgis, reagentų koncentracija ir pačios reakcijos pobūdis.
Tai gali jums pasitarnauti:
Cheminių reiškinių tipai
Cheminės reakcijos gali būti:
Neorganinės reakcijos. Įsikišti neorganiniai junginiai ir gali būti klasifikuojami pagal:
- Prasmė, kuria įvyksta reakcija.
-
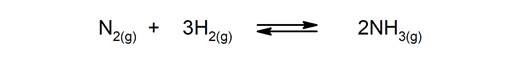
Grįžtamos reakcijos. Jie vyksta abiem būdais, todėl produktai gali suskaidyti ir vėl sudaryti reagentus.
-
Negrįžtamos reakcijos. Jie vyksta tik vienu būdu.

-
Grįžtamos reakcijos. Jie vyksta abiem būdais, todėl produktai gali suskaidyti ir vėl sudaryti reagentus.
- Reaguojančios dalelės tipas.
-
Rūgščių ir šarmų reakcijos. Vyksta H jonų pernaša+.

-
Oksidacijos-redukcijos reakcijos. Vienas iš reagentų oksiduojasi (padidina jo skaičių) oksidacija), o kitas yra sumažėjęs (jo oksidacijos skaičius mažėja). Šiose reakcijose vyksta elektronų perdavimas.

-
Rūgščių ir šarmų reakcijos. Vyksta H jonų pernaša+.
- Reakcijos greitis.
-
Greitos reakcijos. Jie atsiranda per labai trumpą laiką.
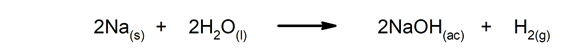
-
Lėtos reakcijos Jie užtrunka ilgai.
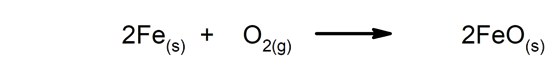
-
Greitos reakcijos. Jie atsiranda per labai trumpą laiką.
- Energijos, kurią ji skleidžia arba sugeria, forma.
-
Egzoterminės reakcijos. Atsiradę jie išskiria šilumą.
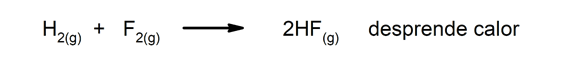
-
Endoterminės reakcijos. Kai jie atsiranda, jie sugeria šilumą.

-
Egzolumininės reakcijos. Kai jie atsiranda, jie skleidžia šviesą.

-
Endolumininės reakcijos. Norint atsitikti, jiems reikia šviesos.

-
Egzoterminės reakcijos. Atsiradę jie išskiria šilumą.
- Transformacijos tipas.
-
Sintezės ar papildymo reakcijos. Dvi medžiagos susijungia ir sudaro naują medžiagą.
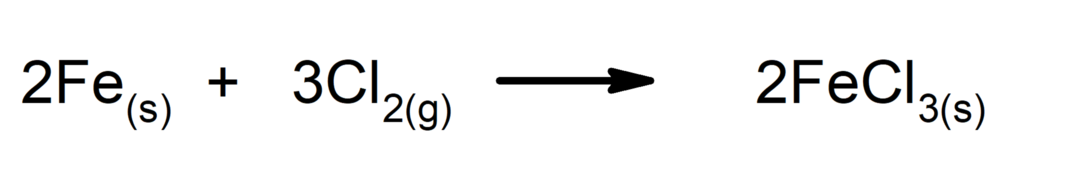
-
Skilimo reakcijos. Viena ar kelios medžiagos suskaidomos į paprasčiausias jų sudedamąsias dalis.
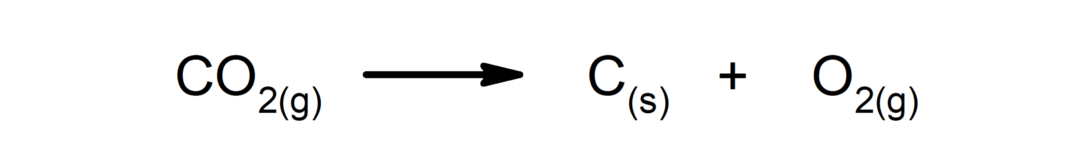
-
Perkėlimo ar pakeitimo reakcijos. Vienas elementas ar junginys pakeičia kitą junginyje, jį išlaisvindami.
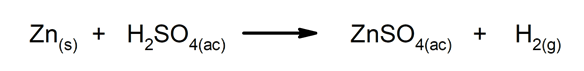
-
Dvigubo pakeitimo reakcijos. Du junginiai keičiasi elementais arba junginiais tuo pačiu metu.

-
Sintezės ar papildymo reakcijos. Dvi medžiagos susijungia ir sudaro naują medžiagą.
Organinės reakcijos. Tai yra reakcijos, į kurias įsikiša organiniai junginiai. Jie turi daug klasifikacijų, atsižvelgiant į reaguojančio organinio junginio tipą ir jo patiriamos reakcijos tipą. Keletas pavyzdžių:
-
Alkanų halogeninimas. Vandenilis yra pakeistas a alkanas halogenu.
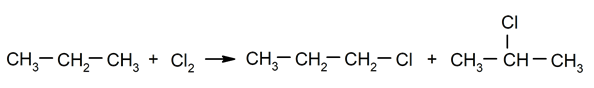
-
Alkanų deginimas. Jei degimas bus baigtas, alkanas reaguoja su deguonimi, kad susidarytų anglies dioksidas ir vanduo.
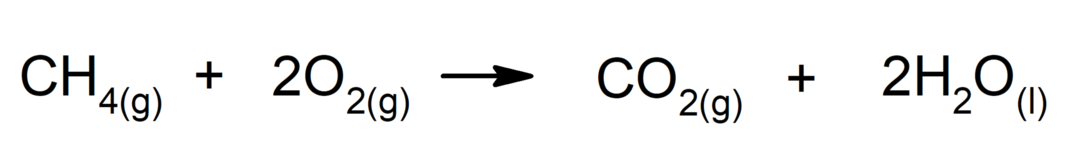
-
Halogeninimas alkenai. Halogenai pakeičia vieną arba abu angliavandenilius, dalyvaujančius dviguboje jungtyje.
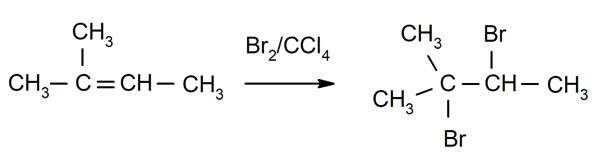
-
Alkenų hidrinimas. Vandeniliai pridedami prie anglies junginių, dalyvaujančių dviguboje jungtyje, kad susidarytų atitinkamas alkanas.
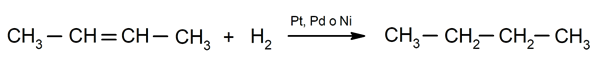
Cheminių reiškinių svarba
Daugelis cheminių reiškinių palaikyti gyvenimą gyvų būtybių, tokių kaip žmogaus virškinimas ir gyvūnai, augalų fotosintezė ir abiejų kvėpavimas.
Kitas labai svarbus cheminis procesas, ypač jo gyvenime mikroorganizmaiyra fermentacija, kuris paprastai naudojamas gaminant maistas kaip sūriai, jogurtai, vynai ir alus.
Visi padidinti ir augimas a gyva būtybė Tai apima jame vykstančias chemines reakcijas, kurias kartais skatina tam tikros aplinkos sąlygos.
Cheminių reiškinių pavyzdžiai
Aplink mus yra daugybė cheminių reiškinių ar procesų, kurie juos apima:
- Medienos puvinys
- Degimas popieriaus
- Pasipriešinimas antibiotikai bakterijos
- Pienas, kuris tampa rūgštus
- Dezinfekuoti žaizdą alkoholio
- Vaisių druskos naudojimas kovojant su rėmeniu
- Deganti žvakė
- Kraujo krešėjimas
- Raumenų nuovargis po intensyvių pratimų
- Mirtis vabzdžiai insekticidais
- Rokforo sūrio gavimas
- Sidro gavimas
- Jogurto gavimas
- Kompostavimas
- Silosavimas
- Bioetanolio gavimas iš melasos
- Išbrinkusios skardinės skardinės
- Supuvęs kiaušinis
- Grotelių rūdijimas
- Biodyzelino gavimas iš palmių aliejaus
Cheminiai reiškiniai pramonėje
Tam tikri cheminiai reiškiniai taip pat yra pagrindiniaiindustrija. Pirmiausia, deginimas angliavandeniliai (pvz., benzino, dyzelino ar žibalo) gamina Energija paleisti mašinas, kurios tvarko begales pramonės procesų.
Kita vertus, plieno pramonė, popierius, plastikas, statybinės medžiagos, dažai, narkotikai, gaminiai agro ir kt., pagrįsti įvairiais cheminiais reiškiniais, tokiais kaip cinkavimas, elektrolizė ir daugelis kiti daugiau.
Iš kartos naujų energijos šaltinių (kaip biodyzelinas ir bioetanolis) taip pat remiasi tokio tipo reiškiniais.
Energijos virsmas
Cheminiuose reiškiniuose yra įprasta energijos transformacija. Pavyzdžiui, kai cheminė energija, esanti tam tikros molekulės ryšiuose, virsta elektros energija arba išsiskiria kaip šilumos (tai įvyksta egzoterminiuose reiškiniuose, pavyzdžiui, kai druskos rūgštis sumaišoma su cinku), vyksta Energija. Tas pats atsitinka, kai šviesos energija yra užfiksuota ir transformuota į cheminę energiją.
Kai kuriems cheminiams procesams vykdyti reikia šilumos ir jie vadinami „endoterminiais“. Kitiems reikalingi katalizatoriai ar kofaktoriai.
