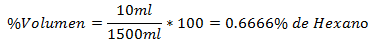Koncentracijos pavyzdys: moliškumas, molingumas, normalumas ir procentinė dalis
Chemija / / July 04, 2021
The Susikaupimas yra apibrėžiamas kaip Tam tikros tirpale esančios medžiagos kiekis arba proporcija. Sprendimas yra a vienalytis mišinys (matoma vienos fazės) kietas, skystas ar dujinis, todėl koncentraciją galima išreikšti įvairiai.
Būtina apibrėžti, kad sprendimą sudaro du pagrindiniai komponentai: Tirpiklis ir tirpiklis, ir paprastai, koncentracija yra skirta išreikšti, kiek ištirpusio tirpalo yra sumaišytas visame tirpale. Tačiau Koncentracija gali išreikšti bet kurio iš jų kiekį ar proporciją.
Koncentracijos išraiška
Chemijoje medžiagos kiekį tirpale galima išreikšti keliais skirtingais būdais: Moliškumas, molingumas, normalumas, procentinė masė, procentinė dalis pagal tūrį.
Iš šių penkių vienetų visus galima naudoti kietiems, skystiems ir dujiniams tirpalams. Tačiau, pavyzdžiui, moliškumas yra labiausiai naudojamas kietiems tirpalams.
Molarizmo pavyzdžiai
The Moliškumas nurodo, kiek molių medžiagos yra kiekviename pilno tirpalo litre. Atliekant tūrinę analizę, tai yra chemijoje dažniausiai naudojamas skystų tirpalų vienetas. Tai žymima raide „M“.
Žinant ištirpusio tirpalo gramus, jie padalijami iš ištirpusios medžiagos molekulinės masės. Taigi gaunami tirpale esantys tirpinio moliai.
Tada ištirpusios medžiagos moliai padalijami tirpalo litrais, taigi gaunami molingumo vienetai: ištirpusios medžiagos moliai / ištirpinimo litras.
1. - 0,5 litro magnio hidroksido [Mg (OH) tirpalui2], o jei magnio hidroksido molekulinė masė yra 58 g / mol. Jūs turite jo 36 gramus.
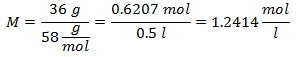
2. 1 litro kalcio hidroksido [Ca (OH) tirpalas2], o jei kalcio hidroksido molekulinė masė yra 74 g / mol. Jūs turite jo 42 gramus.

3. - 3 litrų natrio chlorido (NaCl) tirpalui ir jei natrio chlorido molekulinė masė yra 58 g / mol. Jūs turite 28 gramus jo.
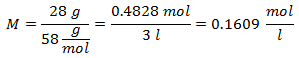
4. - 5 litrų kalcio chlorido (CaCl.) Tirpalui2), ir jei kalcio chlorido molekulinė masė yra 110 g / mol. Jūs turite jo 13 gramų.
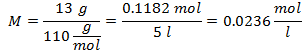
5. - 10 litrų natrio sulfato (Na2SW4), o jei natrio sulfato molekulinė masė yra 142 g / mol. Jūs turite jo 96 gramus.
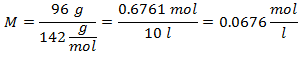
Moliškumo pavyzdžiai
The Molingumas nurodo, kiek ištirpusios medžiagos molių yra 1000 gramų tirpiklio sprendime. Tai plačiausiai chemijoje naudojamas kietųjų tirpalų vienetas. Tai žymima raide „m“.
Žinant ištirpusio tirpalo gramus, jie padalijami iš ištirpusios medžiagos molekulinės masės. Taigi gaunami tirpale esantys tirpinio moliai.
Tada ištirpusios medžiagos moliai koreguojami kiekvienam nustatytam 1000 gramų tirpalo kaip apskaičiavimo pagrindą, taigi gaunami molingumo vienetai: Tirpiosios medžiagos moliai / 1000g Tirpiklis
1. - Tirpalui su 1000g mineralinio tirpiklio ir 36 g magnio hidroksido [Mg (OH)2], o jei magnio hidroksido molekulinė masė yra 58 g / mol.

2. - 2000 g mineralinio tirpiklio ir 42 g kalcio hidroksido [Ca (OH) tirpalui2], o jei kalcio hidroksido molekulinė masė yra 74 g / mol.
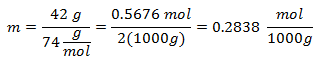
3. - 3000g mineralinio tirpiklio ir 28 g natrio chlorido (NaCl) tirpalui ir jei natrio chlorido molekulinė masė yra 58 g / mol.
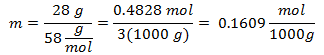
4. - 5000 g mineralinio tirpiklio ir 13 g kalcio chlorido (CaCl2), ir jei kalcio chlorido molekulinė masė yra 110 g / mol.
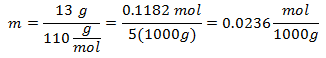
5. - 10 000 g mineralinio tirpiklio ir 96 g natrio sulfato (Na2SW4), o jei natrio sulfato molekulinė masė yra 142 g / mol.
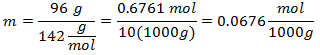
Tirpiklių kiekis laikomas 1000g kartotiniais, kad liktų 1000 gramų kaip atskaitos taškas ir jų neįtrauktų, o tai turi įtakos skaičiavimui.
Normalumo pavyzdžiai
The Normalumas nurodo, kiek medžiagos ekvivalentų yra kiekviename litre viso tirpalo. Normalumas yra kitas chemijoje dažniausiai naudojamas skystųjų tirpalų vienetas, atliekant tūrinę analizę. Tai žymima raide "N".
Ekvivalentas yra vienetas, gaunamas dalijant ištirpusios medžiagos gramus (g) iš jo ekvivalentinio svorio (mažas). Ekvivalentinis svoris (Peq) gaunamas dalijant molekulinę masę (PM) iš aktyviosios Valensijos (*), kurią lengviau stebėti rūgštyse ir bazėse. Pavyzdžiui, aktyvioji druskos rūgšties Valensija (HCl) yra 1; aktyvioji kalcio hidroksido Valensija [Ca (OH)2] yra 2 dėl kiekviename esančio vandenilio (H +) ir hidroksilo (OH-) jonų.
Tada ištirpusių medžiagų ekvivalentai padalijami tirpalo litrais, taigi gaunami normalumo vienetai: ištirpusių medžiagų ekvivalentai / tirpalo litras.
1. - 0,5 litro magnio hidroksido [Mg (OH) tirpalui2], o jei magnio hidroksido molekulinė masė yra 58 g / mol. Jūs turite jo 36 gramus.
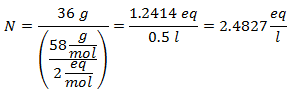
2. 1 litro kalcio hidroksido [Ca (OH) tirpalas2], o jei kalcio hidroksido molekulinė masė yra 74 g / mol. Jūs turite jo 42 gramus.
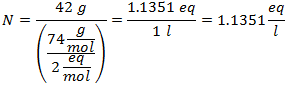
3. - 3 litrų natrio chlorido (NaCl) tirpalui ir jei natrio chlorido molekulinė masė yra 58 g / mol. Jūs turite 28 gramus jo.
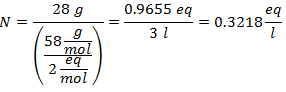
4. - 5 litrų kalcio chlorido (CaCl.) Tirpalui2), ir jei kalcio chlorido molekulinė masė yra 110 g / mol. Jūs turite jo 13 gramų.
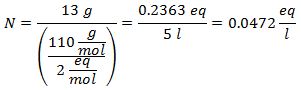
5. - 10 litrų natrio sulfato (Na2SW4), o jei natrio sulfato molekulinė masė yra 142 g / mol. Jūs turite jo 96 gramus.
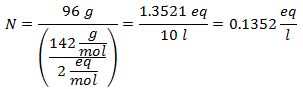
Svorio procentinės dalies pavyzdžiai
The Svorio procentinė dalis yra koncentracijos išraiška, atsirandanti dalijant Tirpalo kiekis gramais tarp viso tirpalo gramų. Gavus dešimtainį skaičių, jis padauginamas iš 100 ir išreiškiamas simboliu „%“. Šis vienetas paprastai naudojamas matuoti koncentracijas kietuose arba granuliuotuose mišiniuose.
1. - viso 1300 g mišinyje yra 13 g kalcio karbonato. Svorio procentinė dalis yra:
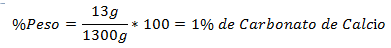
2. - 100 g mišinyje yra 26 g cukraus. Svorio procentinė dalis yra:
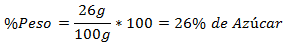
3. - 250 g viso mišinyje yra 60 g natrio chlorido. Svorio procentinė dalis yra:
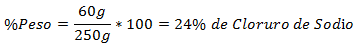
4. - Iš viso 800 g mišinyje yra 150 g kalcio hidroksido. Svorio procentinė dalis yra:
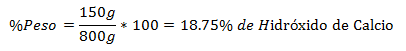
5. - 1500 g viso mišinyje yra 10 g natrio bikarbonato. Svorio procentinė dalis yra:
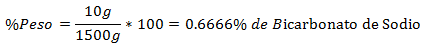
Tūrio procentų pavyzdžiai
The Tūrio procentas yra koncentracijos išraiška, atsirandanti dalijant kiekis tirpinio tūrio vienetais, padalytas iš viso tirpalo tūrio. Gavus dešimtainį skaičių, jis padauginamas iš 100 ir išreiškiamas simboliu „%“. Šis vienetas paprastai naudojamas koncentracijoms matuoti skystų arba dujinių komponentų mišiniuose.
1. - viso 1300 ml mišinyje yra 130 ml etanolio. Tūrio procentas yra:
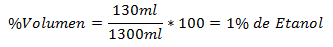
2. 100 ml mišinyje yra 26 ml glicerino. Tūrio procentas yra:
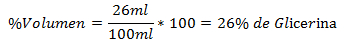
3. - 250 ml viso mišinio sudėtyje yra 60 ml etilo eterio. Tūrio procentas yra:
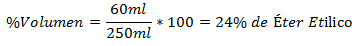
4. - Iš viso 800 ml mišinyje yra 150 ml glikolio. Tūrio procentas yra:
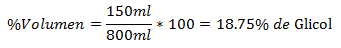
5. - 1500 ml mišinyje yra 10 ml heksano. Tūrio procentas yra: