20 Alkānu piemēri
Miscellanea / / July 04, 2021
The alkāni tie ir sava veida ogļūdeņraži kurā mainīgs skaits oglekļa atomu ir savienoti kopā ar atsevišķām saitēm, piemēram, skelets, un katrs oglekļa atoms savukārt ir piesaistīts ūdeņraža atomiem, kurus galu galā var aizstāt ar citiem atomi vai funkcionālās grupas. Piemēram: hloroforms, metāns, oktāns.
The molekulārā formula no atvērtās lineārās ķēdes alkāniem ir CnH2n + 2kur C apzīmē oglekli, H apzīmē ūdeņradi un n apzīmē oglekļa atomu skaitu. Alkāni ir piesātināti ogļūdeņraži, kas nozīmē, ka tiem nav dubultu vai trīskāršu saišu. Lai nosauktu tos, jūs izmantojat sufikss "-Ano" pēc oglekļa ķēdes nosaukšanas, izmantojot priedēklis kas atbilst oglekļa atomu skaitam (et- (2), pro- (3), but- (4), pen- (5), hex- (6), hep- (7) utt.).
Tas var kalpot jums:
Alkānu klasifikācija
Alkānos tos parasti atpazīst divas lielas grupas: atvērta ķēde (saukta arī par aciklisku) un slēgta (vai cikliska).
Kad atvērtas ķēdes savienojumi Tie neaizstāj ūdeņražus, kas pavada katru oglekļa atomu, tos sauc par lineāriem alkāniem: tie ir vienkāršākie alkāni. Ja tie uzrāda jebkura sava ūdeņraža aizvietojumu ar vienu vai vairākām oglekļa ķēdēm, tos sauc par sazarotajiem alkāniem. Visizplatītākie aizvietotāji ir etilgrupas (CH
3CH2-) un metilgrupa (CH3-).Savukārt molekulā ir savienojumi ar vienu ciklu (monocikliskie) un citi ar vairākiem (policikliskie). The cikliskie alkāni tie var būt homocikliski (tie veidojas tikai ar oglekļa atomu iejaukšanos) vai heterocikliski (kuros piedalās citi atomi, piemēram, skābeklis vai sērs).
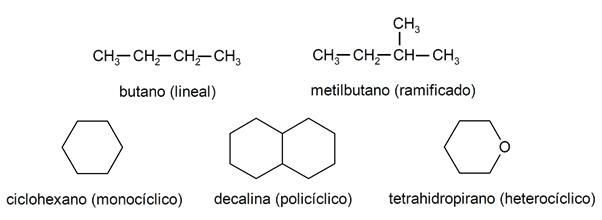
Alkānu fizikālās īpašības
Kopumā fizikālās īpašības alkānu sastāv no molekulmasas (savukārt saistīta ar oglekļa ķēdes garumu). Tie, kuriem ir vismazākais ogļūdeņražu skaits, ir gāzveida uz temperatūra vidē, tie ir no 5 līdz 18 oglekļa atomiem šķidrumi, un virs šī skaitļa ir ciets (līdzīgs vaskam).
Būdami mazāk blīvi nekā ūdens, viņi mēdz uz tā peldēt. Parasti alkāni nešķīst ūdenī un šķīst organiskos šķīdinātājos.
Punkts vārīšanās un kodolsintēze alkānu daudzums ir atkarīgs no to daudzuma molekulmasa, tas ir, no oglekļa ķēdes garuma, lai gan tie daudzkārt ir atkarīgi arī no atomu telpiskā izvietojuma. Lineārajiem un cikliskajiem alkāniem viršanas temperatūra ir augstāka nekā sazarotajām.
Alkānu ķīmiskās īpašības
Alkāniem raksturīga būtne ķīmiskie savienojumi no ļoti slikta reaktivitāte, tāpēc tos sauc arī par "parafīniem" (latīņu valodā parum affinis nozīmē "zema afinitāte"). Tie ir savienojumi, kuriem ir ļoti liela aktivācijas enerģija, kad tie ir iesaistīti ķīmiskās reakcijas. Vissvarīgākā reakcija, kas var notikt alkāniem, ir sadedzināšana radot skābekļa, siltuma, oglekļa dioksīda un ūdens klātbūtnē.
Alkāni ir pamats būtiskai dažādu reakciju, kas saistīta ar rūpnieciskie procesi ļoti svarīgi, jo tā ir tradicionālākā degviela. Tie parādās arī kā tādu bioloģisko procesu galaprodukti kā metanogēna fermentācija, ko veic daži mikroorganismi.
Alkānu piemēri
Daži alkānu piemēri (ieskaitot dažus labi zināmus lineārus un sazarotus):
- Hloroforms (filmas iedomātā nosaukums trihlormetāns; CHCl3). Šīs vielas tvaikus agrāk izmantoja kā anestēzijas līdzekļus. Šim nolūkam tā darbība ir pārtraukta, jo tika konstatēts, ka tas sabojā orgāniem piemēram, aknas vai nieres. Mūsdienās to galvenokārt izmanto kā šķīdinātāju vai dzesēšanas šķidrumu.
- Metāns (CH4). Tas ir visvienkāršākais alkāns no visiem: to veido tikai viens oglekļa atoms un četri ūdeņraža atomi. Tā ir gāze, kas dabiski rodas, sadaloties dažādiem organiskiem substrātiem, un ir galvenā dabasgāzes sastāvdaļa. Pēdējā laikā tas ir atzīts par vienu no gāzēm, kas visvairāk veicina tā saukto siltumnīcas efektu.
- Oktāns (C.8H18). Tas ir astoņu oglekļa alkāns, un tam ir liela nozīme, jo tas nosaka ligroīna galīgo kvalitāti, kas ir samaisa dažādu ogļūdeņražu. Šo kvalitāti mēra ar degvielas oktāna skaitli vai oktāna skaitli, kas par atskaiti ņem zemu detonējošu (100. indekss) un ļoti detonējošu (0.indekss).
- Heksāns (C.6H14). Tas ir svarīgs šķīdinātājs, no tā ieelpošanas ir jāizvairās, jo tas ir ļoti toksisks.
- Butāns (C.4H10). Kopā ar propānu (C.3H8) veido tā sauktās sašķidrinātās naftas gāzes (LPG), kas naftas ieguves procesā veidojas gāzes maisiņos. Pašlaik tiek veicināta benzīna vai dīzeļdegvielas aizstāšana ar sašķidrinātu naftas gāzi kā degvielu kopš tā laika videi draudzīgāka ogļūdeņraža (sadedzinot tas izdala tikai oglekļa dioksīdu un ūdeni).
- Icosano (C.20H42). Tas ir divdesmit oglekļa alkāns (prefikss “ico” nozīmē divdesmit)
- Ciklopropāns (C.3H6). Agrāk to lietoja kā anestēzijas līdzekli
- n-heptāns (C.7H16). Tas ir tas, kuru ņem par atskaiti benzīna oktāna skaitļa nulles punktam, kas būtu vismazāk vēlams, jo tas deg eksplozīvi. To iegūst no dažu sveķiem augi.
- 3-etil-2,3-dimetilpentāns (C.9H20)
- 2-metilbutāns (C.5H12)
- 3-hlor-4-n-propilheptāns (C.10H21Cl)
- 3,4,6-trimetilheptāns (C.10H22)
- 1-brom-2-feniletāns (C.8H9Br)
- 3-etil-4-metilheksāns (C.9H18)
- 5-izopropil-3-metilnonāns (C.13H28)
- Kubietis (C.8H8)
- 1-brompropāns (C.3H7Br)
- 3-metil-5-n-propiloktāns (C.12H26)
- 5-n-butil-4,7-dietildekāns (C.18H28)
- 3,3-dimetildekāns (C.12H26)



