Hoe ontstaan zuren, basen en zouten?
Diversen / / July 04, 2021
Er zijn verschillende theorieën om de zuren en de basissen, waaronder Arrhenius, Brönsted-Lowry en Lewis.
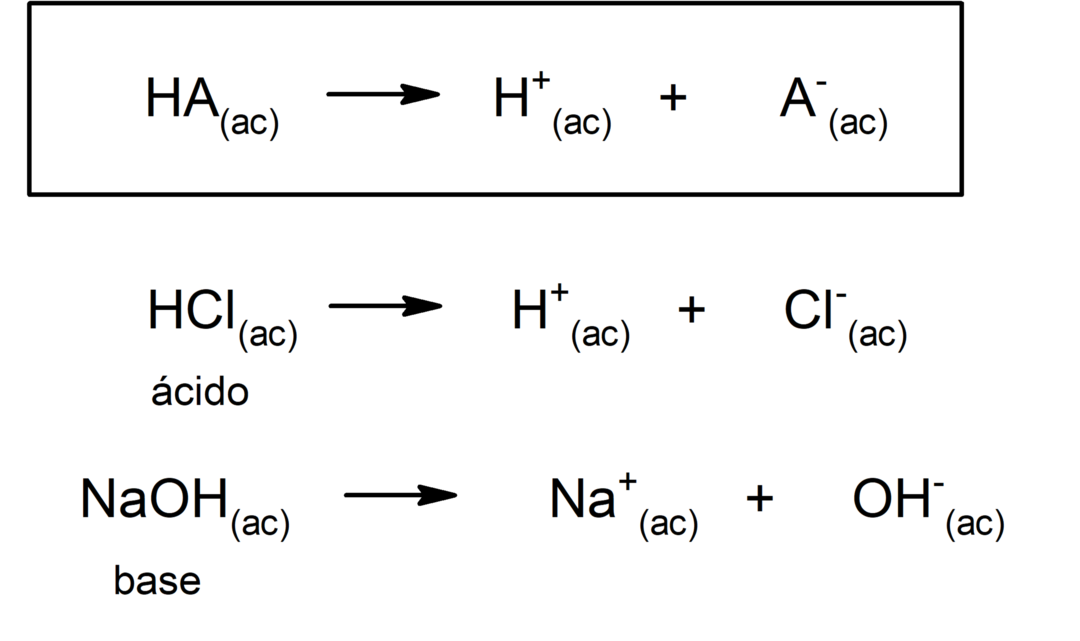
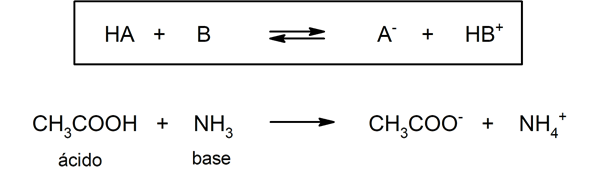
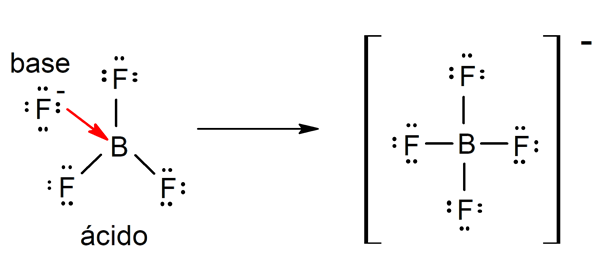
Type zuren oxzuren worden meestal gevormd door reactie tussen een niet-metaaloxide met water, terwijl zuren van het type hydraciden worden gevormd door de combinatie van a niet-metalen met waterstof in waterige oplossing. Bijvoorbeeld:zwavelzuur (H2SW4) het is een oxazuur en zoutzuur (HCl(ac)) het is een waterzuur.
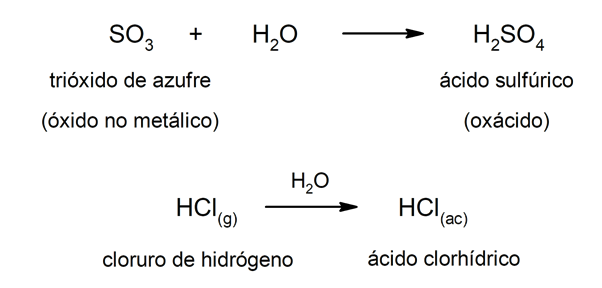
Aan de andere kant kunnen basen worden gevormd als gevolg van de reactie tussen a metaaloxide En het water. Bijvoorbeeld: magnesiumhydroxide (Mg (OH)2).
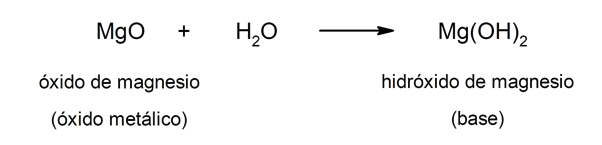
Algemene kenmerken van zuren en basen
Over het algemeen zijn zuren: zuur en bijtend. De bases zijn ook corrosief, bitter van smaak, bijtend bij contact met de huid en zeepachtig aanvoelend. Aan de andere kant hebben zure oplossingen een pH lager dan 7, terwijl baseoplossingen een pH hoger dan 7 hebben.
Zuur- en basesterkte
De neiging van een zuur dissociëren en de pH verlagen, wordt vaak "zuursterkte" genoemd. Een zuur is sterk wanneer het volledig kan dissociëren in een waterige oplossing en is zwak wanneer de dissociatie gedeeltelijk plaatsvindt. Voorbeelden van sterke zuren zijn perchloor (HClO
4), zwavelzuur (H2SW4), joodwaterstof (HI), broomwaterstof (HBr), zoutzuur (HCl) en salpeterzuur (HNO3). Aan de andere kant, azijnzuur (CH3COOH), citrus (C6H8OF7) en benzoëzuur (C6H5COOH) zijn zwak.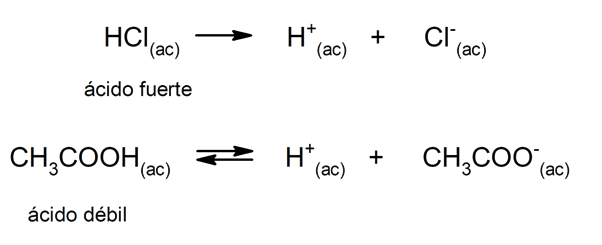
Evenzo kunnen ze worden beschouwd als: sterke bases degenen die volledig dissociëren in waterige oplossing, en zwak wanneer hun dissociatie gedeeltelijk plaatsvindt. Voorbeelden van sterke basen zijn kaliumhydroxide (KOH), natrium (NaOH), lithium (LiOH) en magnesium (Mg (OH)2). Aan de andere kant, ammoniak (NH3) is een zwakke basis.
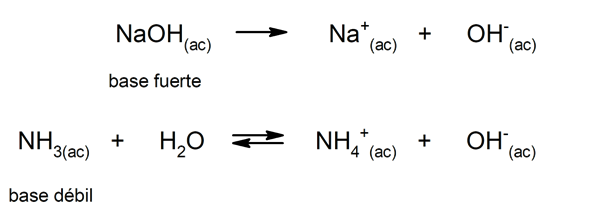
Hoe worden zouten gevormd?
De jij gaat uit zijn ionische verbindingen van verschillende complexiteit, overvloedig van aard en in het algemeen gevormd door de combinatie van zuren met basen in een neutralisatiereactie, die een afgifte van genereert Water. Ze kunnen ook worden gevormd als gevolg van de reactie tussen een metaal en een zuur, een metaal en een niet-metaal, of de reactie tussen verschillende zouten.
De zouten kunnen worden ingedeeld in:
Distributie en belang
Zuren zijn erg belangrijk zowel bij industrie zoals in de natuur. Zoutzuur maakt bijvoorbeeld deel uit van ons spijsverteringsstelsel en is voor ons nodig om de voedingsbestanddelen die in ons lichaam aanwezig zijn af te breken voedsel. Deoxyribonucleïnezuur, beter bekend als DNA, vormt de chromosomen, waarin de genetische informatie wordt gecodeerd die nodig is om ze te coderen. levende wezens vermenigvuldigen en ontwikkelen. Boorzuur is een prominent bestanddeel in de glasindustrie.
De calciumcarbonaat Het is een zeer overvloedig zout in verschillende soorten kalksteenrotsen. Door hoog aandeel temperaturen (900 ° C) uit calciumcarbonaat, calciumoxide of ongebluste kalk wordt verkregen. Het toevoegen van water aan ongebluste kalk produceert calciumhydroxide, gebluste kalk genaamd, wat een base is. Deze materialen ze worden gebruikt in de bouw.
Volgen met: