20 Voorbeelden van amiden
Voorbeelden / / November 06, 2023
De amiden Zijn organische chemische verbindingen derivaten van carbonzuren, waarbij de hydroxylgroep (-OH) van de carboxylgroep (-COOH) van het zuur is vervangen door een aminogroep (-NH2, -NH-R, -N-(R)2waarbij R een willekeurige koolstofketen is).
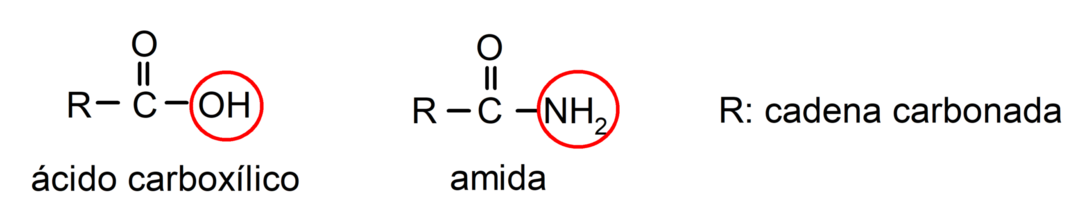
Amiden zijn dat wel organische moleculen die de amidegroep bevatten, die bestaat uit een carbonylgroep en een aminogroep. Bijvoorbeeld: etanamide, propanamide en N-methyl-ethanamide.

- Zie ook: Aldehyden en ketonen
Soorten amiden
Amiden kunnen worden geclassificeerd op basis van het aantal waterstofatomen (die aan de stikstof van de aminogroep zijn gebonden) die zijn vervangen door verschillende substituentgroepen. In deze zin zijn er primaire, secundaire en tertiaire amiden.
- Primaire amiden. Het zijn amiden waarbij de waterstofatomen van de aminogroep niet zijn gesubstitueerd. Bijvoorbeeld:

- Secundaire amiden. Het zijn amiden waarbij een van de waterstofatomen van de aminogroep is gesubstitueerd. Bijvoorbeeld:

- Tertiaire amiden. Het zijn amiden waarbij twee van de waterstofatomen van de aminogroep zijn gesubstitueerd. Bijvoorbeeld:

Nomenclatuur van amiden
Volgens de gebruikelijke nomenclatuur worden amiden genoemd als derivaten van carbonzuren volgens de volgende regels:
- Het koolstofatoom dat overeenkomt met de carbonylgroep bevindt zich op positie 1 en uit dit koolstofatoom wordt de langste koolstofketen gekozen. Bijvoorbeeld:

- Primaire amiden worden genoemd met behulp van het voorvoegsel dat overeenkomt met het aantal koolstofatomen van het carbonzuur dat aanleiding gaf tot deze amiden. Bijvoorbeeld:

Volgens de Internationale Unie voor Pure en Toegepaste Chemie (IUPAC), aminen Ze worden benoemd met behulp van de volgende regels:
- Secundaire en tertiaire amiden worden genoemd met behulp van het voorvoegsel dat overeenkomt met het aantal koolstofatomen van het carbonzuur dat aanleiding gaf tot deze amiden. Bovendien wordt voor elke waterstof van de aminogroep die is gesubstitueerd, een N geplaatst. Zo worden de verschillende substituenten benoemd, waarbij hun hoeveelheid wordt aangegeven, en aan het einde van de naam wordt het woord amide geplaatst. Bijvoorbeeld:

- Wanneer het molecuul prioriteitsgroepen heeft ten opzichte van de amidegroep, wordt het amide als substituent genoemd. In deze gevallen wordt de amidegroep carbamoyl genoemd. Bijvoorbeeld:
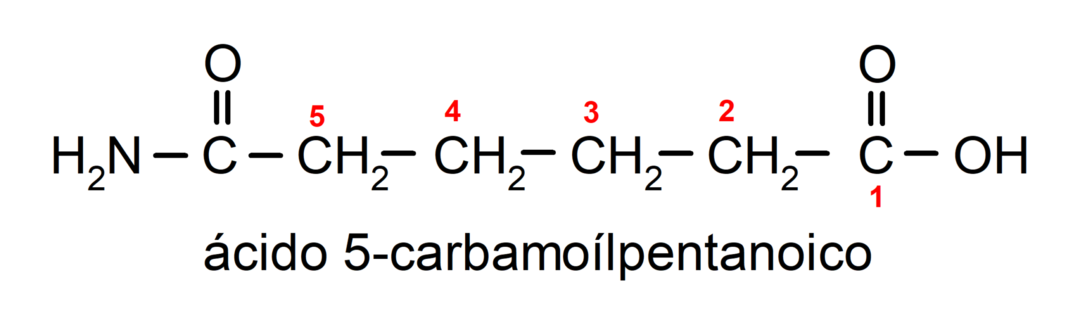
- Wanneer het molecuul wordt gevormd door een cyclus en een amidegroep, wordt de cyclus als hoofdketen genomen en wordt het achtervoegsel -carboxamide geplaatst. Bijvoorbeeld:

Fysische eigenschappen van amiden
- Amiden zijn vast bij kamertemperatuur, met uitzondering van methanamide.
- Ze hebben hoge kookpunten, zelfs hoger dan die van de overeenkomstige carbonzuren.
- Amiden zijn goede oplosmiddelen.
- Het zijn zwakke basen.
Chemische reacties van amiden
- Amiden reageren met een waterig zuur om het overeenkomstige carbonzuur en een ammoniumzout te vormen. Bijvoorbeeld:

- Amiden reageren met alkali om het overeenkomstige carbonzuur en een carboxylaatzout te vormen. Bijvoorbeeld:
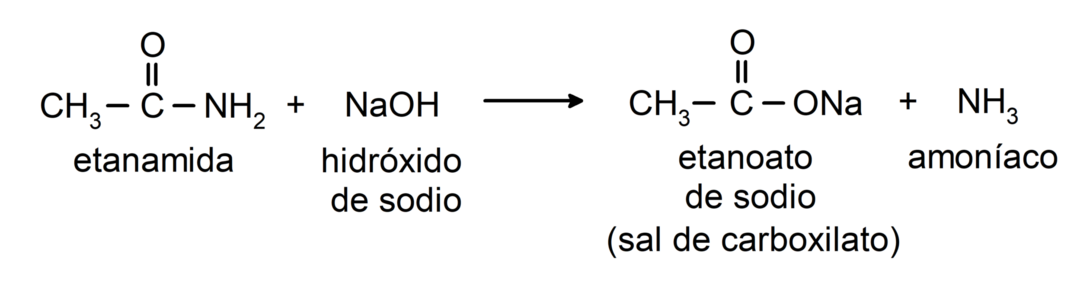
- Amiden worden gereduceerd tot aminen in aanwezigheid van lithiumaluminiumtetrahydride:
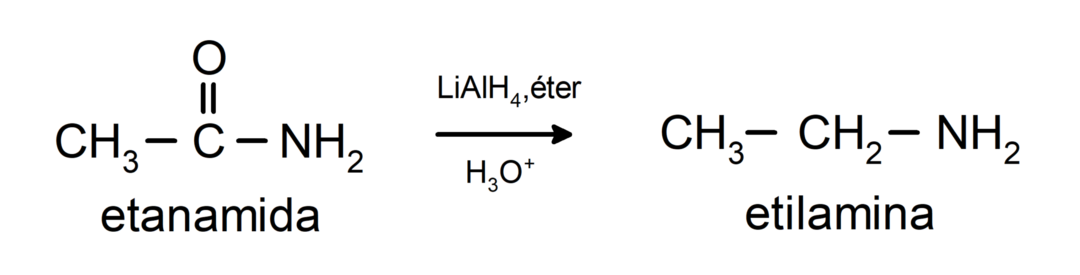
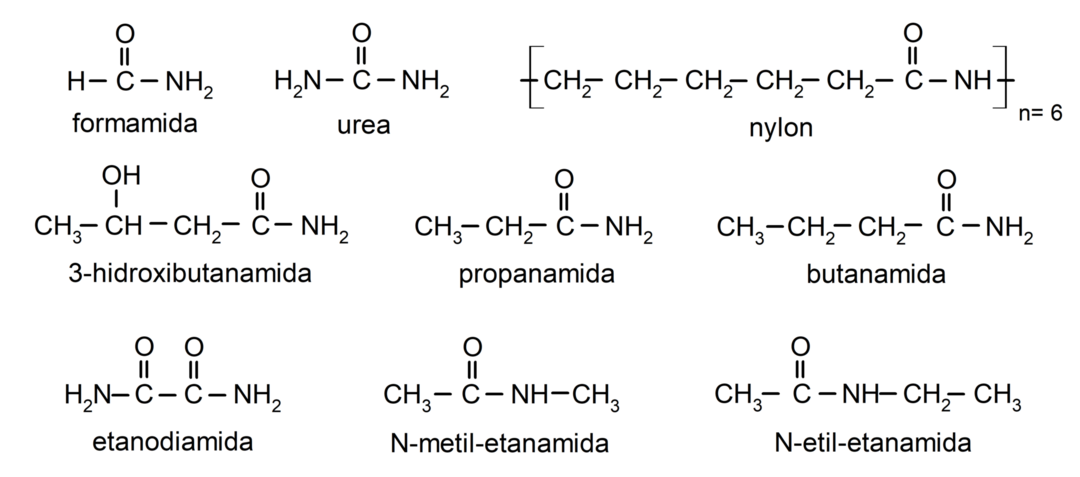
Voorbeelden van amiden
- formamide
- ureum
- nylon
- ε-caprolactam
- ethaanamide
- propaanamide
- butaanamide
- ethaandiamide
- N-methyl-ethaanamide
- N-ethylethaanamide
- N-propyl-ethaanamide
- N, N-dimethylbutaanamide
- benzeencarboxamide
- 4-broom-3-methylcyclohexaancarboxamide
- 3-hydroxybutaanamide

Gebruik van amiden
Amiden worden veel gebruikt in de farmaceutische industrie. Daarnaast worden ze gebruikt als losmiddelcomponenten in de kunststofindustrie. Aan de andere kant worden ze gebruikt als emulgatoren, oppervlakteactieve stoffen en oplosmiddelen. Ureum is bijvoorbeeld een amide dat veel wordt gebruikt in de farmaceutische industrie en de nylonindustrie.
Referenties
- Ramírez-Barrón, S. N., Sáenz-Galindo, A., López-López, L., en Cantú-Sifuentes, L. (2013). Amiden, toepassing en synthese. Wetenschappelijk tijdschrift van de Autonome Universiteit van Coahuila, 5(9).
- Caglieri, S. C., & Pagnan, M. (2013). Theoretisch onderzoek naar de zure hydrolyse van alifatische en aromatische amiden. Technologische informatie, 24(3), 35-40.
- Martínez, C. H. M., Gomez, L. EN. P., de Escobar, M. S., & Escalante, F. NAAR. (2002). organische chemie. Universiteit van Las Palmas de Gran Canaria, vice-rectoraat voor studies en onderwijskwaliteit.
Volgen met:
- Aldehyden
- Alcoholen
- Macronutriënten en micronutriënten
- Organische en anorganische verbindingen
