Lanthanide egenskaper
Kjemi / / July 04, 2021
Lanthanides er de kjemiske elementene som spenner fra Lanthanum til Lutetium. De deler vanlige egenskaper, som de er klassifisert for i en spesiell kategori nederst i det periodiske systemet.
Hovedtrekk ved lanthanider:
- De er lokalisert i periode 6 i det periodiske systemet.
- De dekker 15 elementer, fra 57 til 71.
- De deler strukturen til Lanthanum, som tilsettes et energinivå f, som er mindre kjemisk reaktivt.
- De ble kalt sjeldne jordarter fordi de i en naturlig tilstand alltid kombineres for å danne oksider.
- Noen er relativt rikelig.
- Selv om de har variable valenser, har de fleste valenser +3.
- Når atomnummeret øker, reduseres radiusen.
- De har alle et skinnende metallisk utseende.
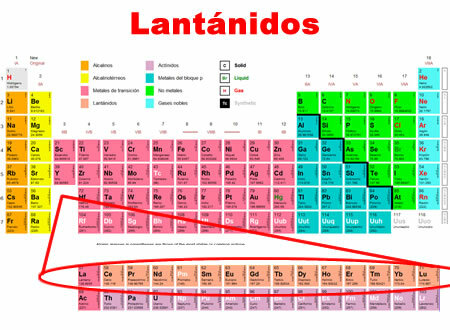
Individuelle egenskaper ved lantanider:
Lanthanum (La).
- Atomnummer 57
- Atomvekt: 139
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 920 ° C
- Kokepunkt: 3457 ° C
Det ble oppdaget i 1839. I industrien brukes det i legeringer med andre lanthanider for å lage lettere steiner; i optikk brukes den til optiske briller. Det brukes også til hydrogensvamper, som brukes til å inneholde gasser. I medisin brukes det i form av lantankarbonat, for behandling av nyresvikt, da det har en affinitet å blande seg med fostater, og redusere hyperfosfemi.
Cerium (Ce)
- Atomnummer 58
- Atomvekt: 140
- Tilstand: Mykt fast stoff
- Utseende: Metallisk, sølvgrå, jernlignende
- Valencias: +3, +4
- Smeltepunkt: 798 ° C
- Kokepunkt: 3426 ° C
Det ble oppdaget i 1803. Det er den mest utbredte lantanidet. Den brukes til å lage katalysatorer, hovedsakelig for biler (katalysatorer) og for oljesprenging. I oksidform brukes det til å polere briller og linser. Selv om den ikke har noen kjente biologiske funksjoner, brukes den i medisin i brannsalver.
Praseodymium (Pr)
- Atomnummer 59
- Atomvekt: 144
- Tilstand: Mykt fast stoff
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 931 ° C
- Kokepunkt: 3520 ° C
Den ble oppdaget i 1841 og isolert i 1885. I industrien brukes det i legeringer med magnesium for å lage flymotorer; Det brukes til å gi glass og emaljer en gul farge. Nikkellegeringer har magnetiske egenskaper. Reagerer med halogener for å produsere fluorider, klorider, bromider og jodider.
Neodym (Nd)
- Atomnummer 60
- Atomvekt: 139
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1024 ° C
- Kokepunkt: 3100 ° C
Det ble oppdaget i 1885, da praseodymium ble isolert; neodym ble isolert til 1925. Det er en av de mest reaktive lantanidene. I industrien brukes det til å fargelegge glass og emaljer. På grunn av sin evne til å absorbere lys, brukes det i astronomi til å lage krystaller som infrarøde spektrometre og filtre er kalibrert med. En av dens viktigste bruksområder er å lage magneter med høy magnetisk intensitet. Disse magnetene brukes til presisjonsinstrumenter, for eksempel de som brukes i datamaskinens harddisker, samt noen slanke formathøyttalere.
Promethium (Pm)
- Atomnummer 61
- Atomvekt: 145
- Solid tilstand
- Utseende: ?
- Valencias: +3
- Smeltepunkt: 1100 ° C
- Kokepunkt: 3000 ° C
Dens eksistens ble spådd i 1902, men kunne ikke bevises før 1944. Dette lantanidet finnes ikke i naturen, da det er kilden for å oppnå og studere fisjon av uran. Når uran spaltning i en kjernefysisk reaktor, er prometium et av atomene som produseres fra denne atomseparasjonen. Den har radioaktive egenskaper som gir den fosforesens og brukes til kalibratorer og kjernefysiske batterier som brukes i romskip.
Samarium (Sm)
- Atomnummer 62
- Atomvekt: 150
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1072 ° C
- Kokepunkt: 1803 ° C
Den ble oppdaget i 1853 og isolert i 1879. Den har flere isotoper, og minst to av dem er radioaktive. I industrien brukes det i optikk til å lage krystaller som absorberer infrarødt lys. Det brukes også som en katalysator for å skaffe alkohol, og som et element i noen lysrør og TV. Når det gjelder helse, kan det forårsake lungeemboli eller påvirke leveren, hvis det inhaleres (for eksempel oksidet som brukes til å polere krystaller). Radioaktive isotoper brukes til strålebehandling av dødssyke pasienter.
Europium (Eu)
- Atomnummer 63
- Atomvekt: 152
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +2, +3
- Smeltepunkt: 826 ° C
- Kokepunkt: 1527 ° C
Den ble oppdaget i 1890. Det er den mest reaktive av lanthanidene. Det har blitt brukt i lysrør og fjernsyn, men for å forårsake lungeemboli hvis det er det inhalert eller skadet leveren hvis den akkumuleres i menneskekroppen, har den nesten ingen industrielle bruksområder. I atomforskning brukes den siden den absorberer nøytroner.
Gadolinium (Gd)
- Atomnummer 64
- Atomvekt: 157
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1312 ° C
- Kokepunkt: 3250 ° C
Gadolinium har få bruksområder, den viktigste er magnetisk industriell kjøling, siden den øker sine magnetiske egenskaper ved lave temperaturer; men siden denne typen kjølere krever bruk av arsen, brukes de ikke i husholdningskjøling. I medisin brukes det som kontrastmiddel for magnetisk-nukleær resonans.
Terbium (Tb)
- Atomnummer 65
- Atomvekt: 159
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +4
- Smeltepunkt: 1356 ° C
- Kokepunkt: 3230 ° C
Den ble oppdaget i 1843 og isolert i 1905. Det er veldig viktig i elektronikkindustrien, da det er et av elementene som brukes til å lage halvledere. Andre bruksområder er å lage lysrør og billedrør. Det brukes også som katalysator i brenselceller. Selv om den ikke har biologiske funksjoner, har innånding eller inntreden i menneskekroppen toksiske effekter, som hovedsakelig påvirker leveren.
Dysprosium (Dy)
- Atomnummer 66
- Atomvekt: 162,5
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +2, +3
- Smeltepunkt: 1407 ° C
- Kokepunkt: 2567 ° C
Den ble oppdaget i 1843 og isolert i 1905. Det er veldig viktig i elektronikkindustrien, da det er et av elementene som brukes til å lage halvledere. Andre bruksområder er å lage lysrør og billedrør. Det brukes også som katalysator i brenselceller. Selv om den ikke har biologiske funksjoner, har innånding eller inntreden i menneskekroppen toksiske effekter, som hovedsakelig påvirker leveren.
Holmium (Ho)
- Atomnummer 67
- Atomvekt: 166
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1474 ° C
- Kokepunkt: 2700 ° C
Det ble oppdaget i 1878 og navnet stammer fra byen oppdagelsen, Stockholm, på latin, Holmia. Den har nesten ingen praktiske bruksområder; den brukes imidlertid i noen bransjer som en katalysator for kjemiske reaksjoner, så vel som for noen elektroniske komponenter. Det brukes også til å endre frekvensen og intensiteten til laserstrålen.
Erbium (Er)
- Atomnummer 68
- Atomvekt: 167
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1795 ° C
- Kokepunkt: 2863 ° C
Det ble oppdaget i 1843. Den brukes i atomindustrien som en nøytronbuffer. I oksydform er det et fargestoff for krystaller, noe som gir dem en rosa fargetone; Disse krystallene brukes i optikk og smykker. Det brukes også til å lage fiberoptikk.
Thulium (Tm)
- Atomnummer 69
- Atomvekt: 167
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1545 ° C
- Kokepunkt: 1947 ° C
Den ble oppdaget i 1879. Til tross for den lave tilgjengeligheten, på grunn av de radioaktive egenskapene, er den viktigste bruken som røntgenkilde i bærbart utstyr og til solid state-lasere.
Ytterbium (Yb)
- Atomnummer 70
- Atomvekt: 173
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 824 ° C
- Kokepunkt: 1194 ° C
Den ble oppdaget i 1878 og isolert i 1907. Radioaktive isotoper brukes til bærbart røntgenutstyr som fungerer uten strøm. Det brukes også til å forbedre stållegeringer og øke motstanden, en egenskap som brukes i tannbehandling på grunn av forbedring av ståls mekaniske egenskaper. Det må håndteres med forsiktighet, da det kan forårsake irritasjon og forbrenning. I tillegg kan det forårsake en eksplosjon eller brann når det reagerer med luft.
Lutetium (Lu)
- Atomnummer 71
- Atomvekt: 175
- Solid tilstand
- Utseende: Metallisk, sølvhvit
- Valencias: +3
- Smeltepunkt: 1652 ° C
- Kokepunkt: 3402 ° C
Det ble oppdaget i 1907. Det er det minst rikelige kjemiske elementet i jordskorpen. Til tross for lav tilgjengelighet brukes den til oljeraffinering og som en katalysator for organiske kjemiske reaksjoner. Noen radioaktive isotoper er også testet for strålebehandling.