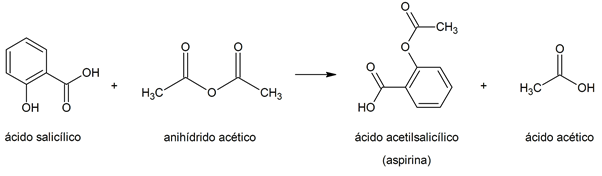20 Exemplos de reações químicas
Miscelânea / / July 04, 2021
É chamado reação química ao processo pelo qual um ou mais substancias quimicas (chamados de “reagentes”) são transformados e dão origem a outros (chamados de “produtos”). Assim, para que os reagentes gerem produtos por meio de uma reação química, um rearranjo de átomos Y moléculas em que ocorre uma troca de energia. Por exemplo: combustão, oxidação, reações ácido-base.
O compostos químicos ter energia química nas ligações entre os átomos que os compõem. As reações químicas são geralmente expressas por meio de equações, onde os reagentes são indicados à esquerda e os produtos à direita, ligando ambas as partes com uma seta para a direita se a reação for reversível ou uma seta para frente e para trás se for uma reação reversível.
Quando são indicadas as quantidades ou proporções em que os reagentes reagem e os produtos são obtidos, falamos de reações estequiométricas.
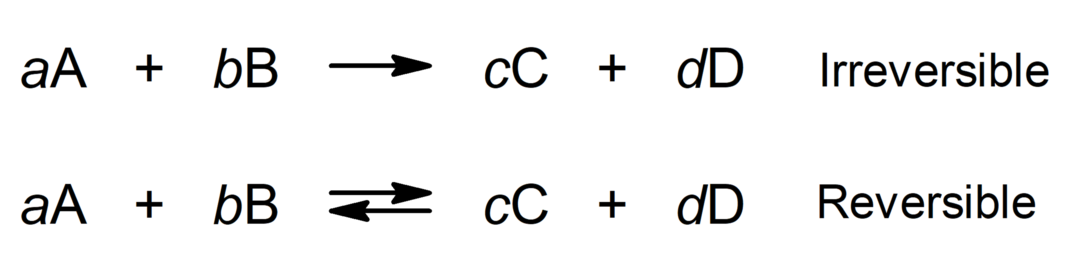
Onde:
- A e B são os reagentes.
- C e D são os produtos.
- a, b, c, d são os coeficientes estequiométricos (número de moléculas ou átomos de um certo tipo que participam de uma equação química).
Reações químicas pode ser classificado de acordo com o tipo de energia que eles liberam ou absorvem. Nesse sentido, podem ser exotérmicos ou endotérmicos (se liberarem ou absorverem quente), exoluminosas ou endoluminosas (se liberam ou absorvem luz), exoelétricas ou endoelétricas (se produzem ou precisam eletricidade).
As leis das reações químicas
Nas reações químicas, as leis são cumpridas. O mais importante é o Lei da conservação de massa ou lei de Lavoisier, formulado por este químico em 1774, que postula que em toda reação química a massa dos reagentes é igual à massa dos produtos.
Era Dalton que completou a explicação desta lei alguns anos depois, indicando que em uma reação química o número de átomos não variam ao comparar reagentes com produtos, apenas sua organização muda, então a massa de se conservas.
Outro parâmetro importante nas reações químicas é o seu velocidade de reação já que nem todos levam o mesmo tempo para produzir. A taxa de reação é definida como a quantidade de produto que aparece por unidade de tempo ou a quantidade de reagente que desaparece por unidade de tempo.
Embora cada reação tenha uma velocidade diferente, certos fatores podem fazer com que ela tenda a aumentar ou diminuição: a superfície de contato entre as partículas reagentes e a temperatura são algumas das eles.
O catalisadores São substâncias que aumentam a velocidade de uma reação, sem modificar sua estrutura. Muitas vezes, esse papel é desempenhado por alguns metais.
Exemplos de reações químicas
As reações químicas ocorrem continuamente na natureza, no corpo humano, nas fábricas, nas estações de tratamento de efluentes, etc. Alguns exemplos são:
-
Combustão
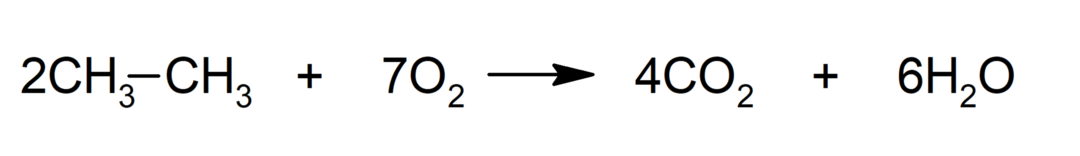
-
Substituição
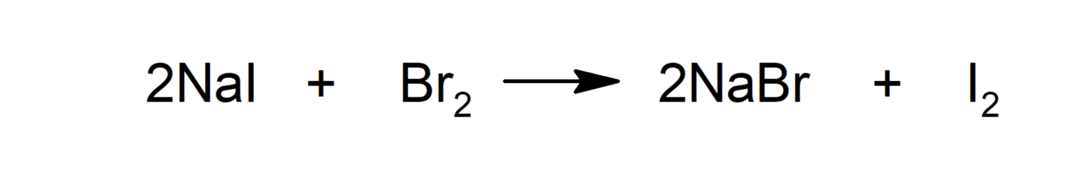
-
Adição
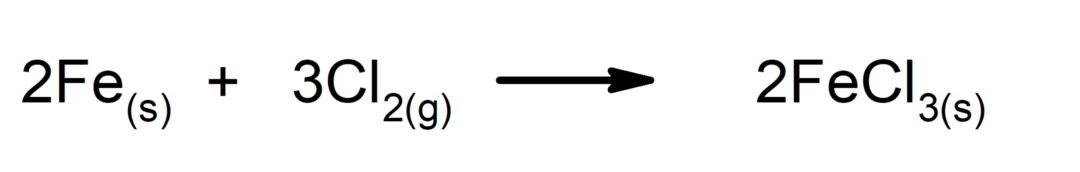
-
Eliminação
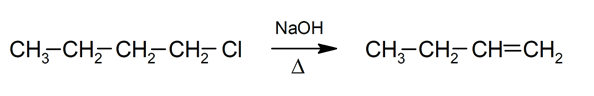
-
Oxidação
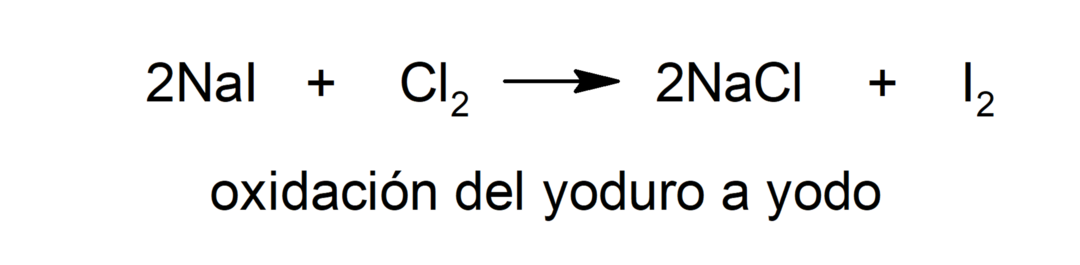
-
Redução
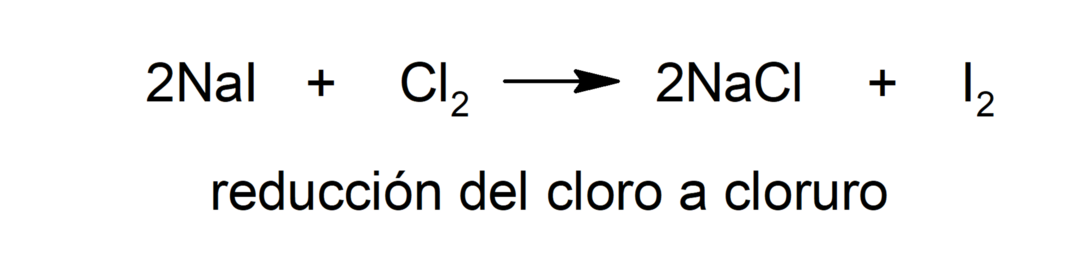
-
Reações ácido-base
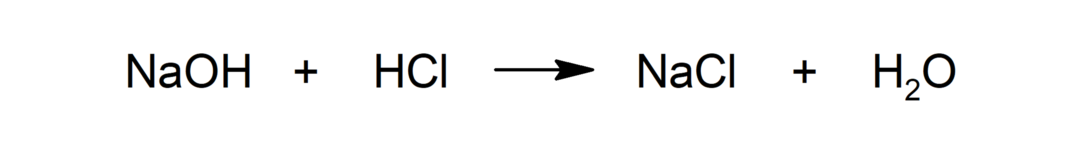
-
Oxigenação
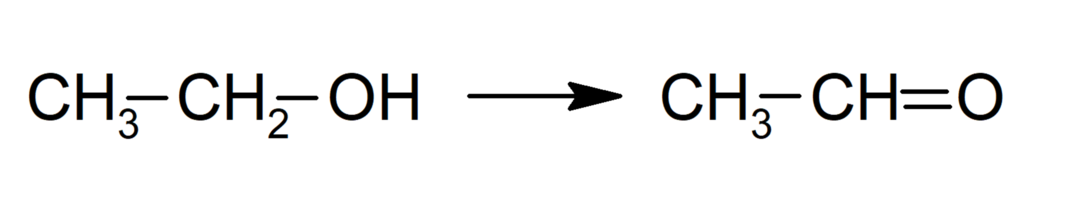
-
Transaminação

-
Cloração
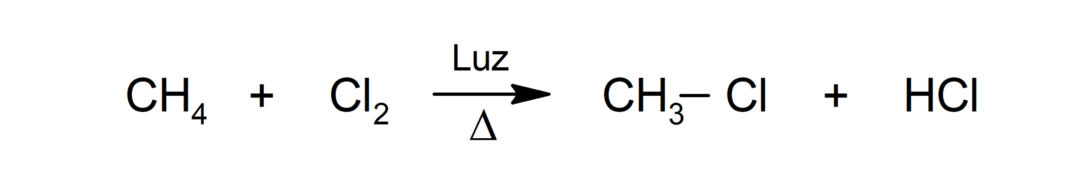
-
Carbonilação

-
Nitrosilação. É uma reação em que um grupo nitrosil se liga a uma proteína, após sua síntese pelos ribossomos.

-
Peroxidação
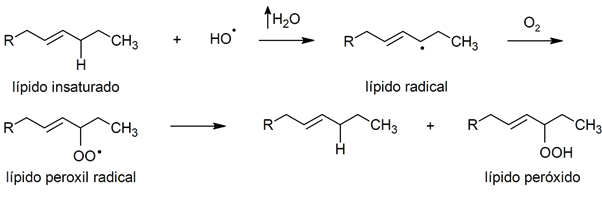
-
Fotólise da água
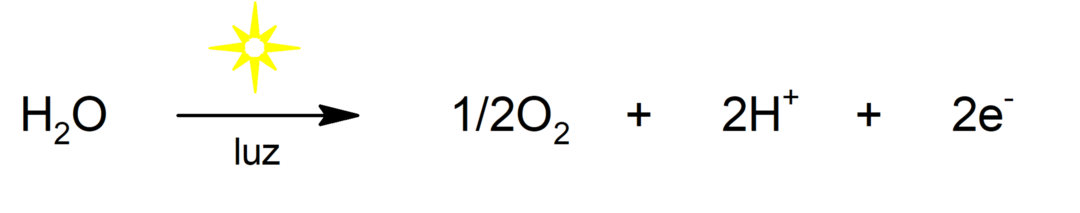
-
Sulfação
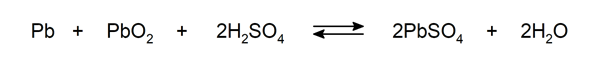
-
Carbonatação
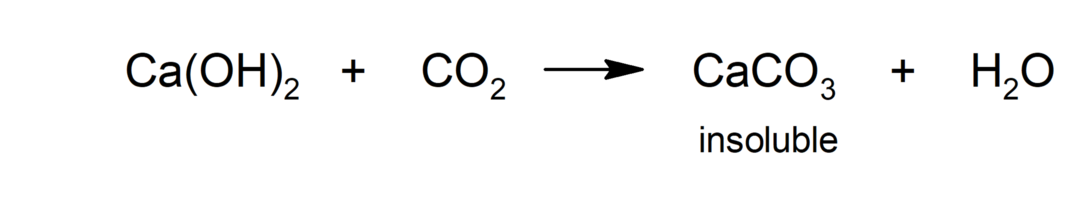
- Ozonização. É uma reação alternativa à cloração para descontaminar a água.
-
Esterificação
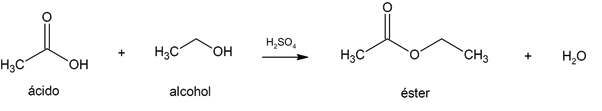
-
Hidrogenação de alcenos
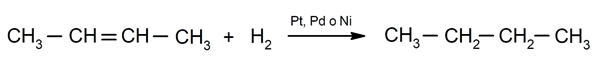
-
Acetilação