10 Exemple de amestecuri de gaze
Miscellanea / / July 04, 2021
Amestecuri de substanțe gazoase Acestea sunt unele dintre cele mai ușor de realizat, deoarece este foarte posibil ca substanțele care se află în această stare de agregare să fie amestecate. De exemplu: Amestec de neon, argon și xenon, insecticid cu aerosoli, aer și heliu.
Practic toate gazele pot fi combinate nelimitat, bineînțeles condiționate de unele chimice, fizice și fundamental legate de aspectele de siguranță ale utilizatorilor care manipulează. La fel ca diferitele tipuri de amestecuri care se stabilesc între substanțe, amestecuri de gaze au și proprietăți care le sunt unice.
Studiul amestecuri fizzy este de obicei la fel de util ca cel al gazelor în stare pură: aceleași cunoștințe despre aer care sunt prezente în atmosfera ar fi imposibilă dacă nu s-ar cunoaște proporțiile și comportamentele gazelor mixte.
În acest fel, este esențial să cunoști unele Caracteristici de amestecuri de gaze, cum ar fi proprietatea presiunii parțiale (cea exercitată de fiecare dintre gazele din amestec) și cel al fracției molare (raportul dintre numărul de moli dintr-o componentă gazoasă și cel al amestecului total sifon). Moli exprimă cantitatea de gaz din amestec.
Legea lui Dalton afirmă că presiunea totală a unui amestec de gaze este egală cu suma presiunilor parțiale ale fiecăruia unul dintre gazele individuale care participă la acesta (aceasta este condiționată de gazele care nu reacționează între Da). Presiunea parțială este înțeleasă aici ca fiind cea pe care fiecare gaz ar exercita-o dacă ar fi găsită doar în același recipient și în aceleași condiții de temperatura. A) Da:
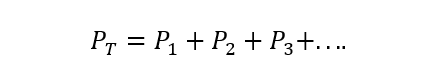
Unde PT este presiunea totală și P1, P2 Și p3 sunt presiunile parțiale ale gazelor ipotetice 1, 2 și 3 din amestecul de gaze.
Folosind Legea lui Dalton, a fost dezvoltată o expresie pentru a calcula presiune parțială a unui gaz dintr-un amestec gazos dacă îi cunoaștem presiunea totală și fracția molară.
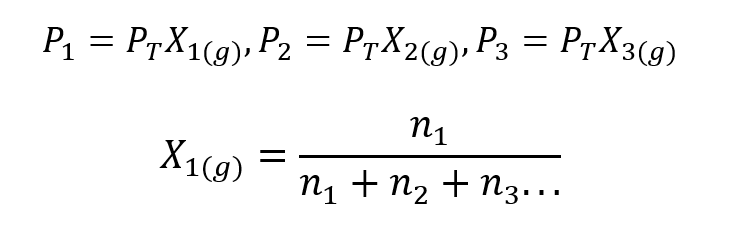
Unde X1, X2 Da X3 sunt fracțiile molare ale gazelor ipotetice 1, 2 și 3 din amestecul de gaze și n1, n2 Da n3 sunt cantitățile de substanță din fiecare dintre aceste gaze din același amestec.
Unul dintre proprietăți principale din componentele din amestecuri este concentrația, care poate fi exprimată în diferite unități. În cazul amestecurilor de gaze, concentrația componentelor sale poate fi exprimată în ppm (părți pe milion), o unitate menționată la volumul său. Adică, o anumită cantitate de ppm dintr-un component dintr-un amestec de gaze este raportul dintre volumul acelei cantități și volumul fiecărui milion de unități de amestec.
Este important să rețineți că ppm a unui gaz depinde de temperatura și presiunea gazului. Din acest motiv, pentru a calcula ppm-ul unui gaz, se folosesc de obicei condiții normale de presiune și temperatură. (CNPT), care dau o stare normală la 0 grade Celsius de temperatură și 1013 hectopascali (1 bar) de Presiune. Dacă aceste condiții nu sunt utilizate, trebuie să specificați care vor fi utilizate.
Vă poate servi:
Exemple de amestecuri de gaze
Următoarea listă conține amestecuri de gaze, specificând elementele care apar în amestec:
- Aer (amestec de 21% oxigen și 79% azot, plus alte gaze în proporții mici)
- Cronigón (amestec de argon 99% și oxigen 1%)
- Trimix (amestec de oxigen, azot și heliu)
- Se amestecă neon, argon și xenon
- Amestec de 85% metan, 9% etan, 4% propan și 2% butan.
- Hexafluorură de sulf și aer
- Insecticid cu aerosoli
- Aer și heliu
- Nitrox (amestec de aer, îmbogățit în oxigen și azot)
Urmărește cu: