20 Exemple de săruri acide
Miscellanea / / July 04, 2021
În Chimie anorganică sărurile se numesc compuși care se obțin atunci când a acid atomii săi de hidrogen sunt înlocuiți cu cationi metalici (deși uneori cu cationi nemetalici, de exemplu, cationul de amoniu, NH4+). În cazul specific al săruri acide, hidrogenii acidului sunt parțial substituiți, adică cel puțin un hidrogen nesubstituit rămâne ca parte a sării. Prin faptul că se disting de săruri neutre, în care hidrogenii acidului sunt total substituiți.
ieși afară se formează de obicei prin reacția dintre a acid și a hidroxid (baza). În aceste reacții, în mod normal, baza își pierde grupările hidroxil (-OH), iar acidul le pierde. atomi hidrogen (H), formând o sare neutră; dar dacă acidul în cauză conservă cel puțin unul dintre atomii săi de hidrogen, modificând sarcina electrică a reacției, vom obține o sare acidă sau o sare hidrogenată.
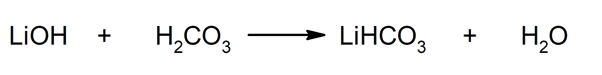
Astfel, de exemplu, bicarbonatul de litiu și apa se obțin din reacția dintre hidroxidul de litiu și acidul carbonic:
Nomenclatura sărurilor acide
Sărurile acide pot fi denumite în conformitate cu trei tipuri nomenclatura cea mai frecventă:
Exemple de săruri acide
- Bicarbonat de sodiu (NaHCO3). Numit și hidrogen carbonat de sodiu (IV), este un solid cristalin alb, solubil în apă, care poate fi găsit în natură în stare mineral sau poate fi produs în laborator. Este una dintre cele mai cunoscute săruri acide și este utilizată pe scară largă în cofetărie, farmacologie sau fabricarea iaurtului.
- Bicarbonat de litiu (LiHCO3). Această sare acidă a fost utilizată ca agent de captare a CO2 în situații în care un astfel de gaz este nedorit, ca în misiunile spațiale nord-americane „Apollo”.
- Fosfat dihidrogen potasic (KH2PO4). Este un solid cristalin, inodor, solubil în apă, utilizat pe scară largă în diverse industrii, cum ar fi drojdia de alimente, agent de chelare, întăritor nutrițional și asistent în procesele de fermentare.
- Bisulfat de sodiu (NaHSO4). Este o sare acidă formată prin neutralizarea acidului sulfuric. Este utilizat pe scară largă industrial în rafinarea metalelor și a produselor de curățare. Deși este extrem de toxic pentru unele echinoderme, este utilizat ca aditiv în hrana animalelor de companie și în fabricarea bijuteriilor.
- Hidrogen sulfurat de sodiu (NaHS). Este un compus periculos de manipulat, deoarece este foarte coroziv și toxic. Poate provoca arsuri severe ale pielii și leziuni oculare, deoarece este, de asemenea, combustibil.
- Hidrogen fosfat de calciu (CaHPO4). Se utilizează ca supliment alimentar în cereale pentru vite. Este un solid insolubil în apă, dar capabil să cristalizeze atunci când este hidratat prin consumul a două molecule de apa.
- Hidrogen carbonat de amoniu ([NH4] HCO3). Cunoscut și sub numele de „bicarbonat de amoniu”, este utilizat în industria alimentară ca drojdie chimic, deși are dezavantajul de a prinde amoniac și de a da mâncării un gust prost dacă este utilizat în exces. Este, de asemenea, utilizat la stingătoarele de incendiu, la fabricarea pigmentului și la extinderea cauciucului.
- Bicarbonat de Barisau (Ba [HCO3]2). Este o sare acidă care, atunci când este încălzită, poate inversa reacția de producție și este extrem de instabilă, cu excepția soluției. Este utilizat pe scară largă în industria ceramicii.
- Bisulfit de sodiu (NaHSO3). Această sare este extrem de instabilă și în prezența oxigenului derivă în sulfat de sodiu (Na2SW4), motiv pentru care este folosit în industria alimentară ca conservant și deshidratant pentru alimente. Este un agent de reducere extrem și utilizat în mod obișnuit de om, folosit și în fixarea culorilor.
- Citrat de calciu (AC3[C6H5SAU7]2). Cunoscută în mod obișnuit sub numele de sare amară, este utilizată ca conservant alimentar și ca supliment nutritiv atunci când este legată de aminoacidul lizină. Este o pulbere cristalină albă, inodoră.
- Fosfat monocalcic (Ca [H2PO4]2). Este un solid incolor care se obține din reacția hidroxidului de calciu și a acidului fosforic, utilizat pe scară largă ca agent de dospire sau ca îngrășământ în munca agricolă.
- Fosfat dicalcic (CaHPO4). De asemenea, cunoscut sub numele de fosfat de monohidrogen de calciu, are trei forme cristaline diferite care sunt utilizate ca aditiv în alimente și este prezent în pastele de dinți. În plus, se formează în mod natural în calculii renali și în așa-numita „calculi renali”.
- Fosfat de monomagneziu (MgH4P2SAU8). Este o sare albă, cristalină și inodoră, parțial solubilă în apă. Este utilizat în conservarea alimentelor, ca acidulant, ca corector de aciditate sau agent în tratamentul făină.
- Diacetat de sodiu (NaH [C2H3SAU2]2). Această sare este utilizată ca agent aromatizant și conservant în mese, ceea ce previne sau întârzie apariția ciuperci și micobacterii, atât în produse ambalate sub vid, cum ar fi produsele din carne, cât și în industria făinii.
- Bicarbonat de calciu (Ca [HCO3]2). Este o sare hidrogenată care provine din carbonatul de calciu, prezent în minerale precum calcarul, marmura și altele. Această reacție implică prezența apei și a CO2, deci poate apărea spontan în peșteri și peșteri bogate în calciu.
- Fluorură de acid rubidiu (RbHF). Această sare se obține din reacția acidului fluorhidric (hidrogen și fluor) și a rubidiului, un metal alcalin. Rezultatul este un compus toxic și coroziv care trebuie manipulat cu prudență.
- Fosfat de monoamoniu ([NH4] H2PO4). Este o sare solubilă în apă produsă prin reacția amoniacului și a acidului fosforic. Se folosește de obicei ca îngrășământ, deoarece dă solului nutrienți de azot și fosfor necesare creșterii plantelor. De asemenea, face parte din pulberea ABC din stingătoarele de incendiu.
- Ortoborat de hidrogen de zinc (Zn [HBO3]). Este o sare folosită ca antiseptic și ca aditiv în fabricarea ceramicii.
- Fosfat monosodic (NaH2PO4). Este utilizat mai ales în laboratoare, ca „tampon” sau soluție tampon, care previne modificările bruște ale pH-ului unei soluții.
- Hidrogen ftalat de potasiu (KHP). De asemenea, numit „ftalat acid de potasiu”, este o sare solidă și stabilă în aerul obișnuit, motiv pentru care este adesea folosit ca standard primar în măsurători de pH. De asemenea, este util ca agent tampon în reacții chimice.
Urmărește cu:

