30 Exemple de alcool
Exemple / / November 06, 2023
The alcooli sunt compuși chimici organici care conțin în structura lor gruparea funcțională hidroxil (- OH) atașată la un carbon (- C). Grupul (- C – OH) se numește „carbinol”. Câteva exemple de alcooli sunt: metanol, etanol și 1-propanol.
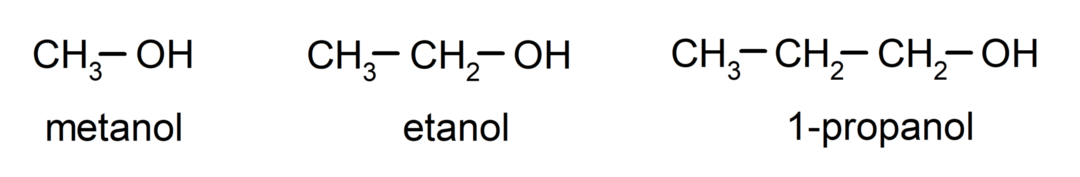
Alcoolii sunt compuși chimici cu diverse utilizări în viața de zi cu zi, deoarece au proprietăți antibacteriene și antiseptice. Pe de altă parte, pot fi periculoase pentru sănătatea umană atunci când sunt ingerate necontrolat.
De asemenea, nu toate alcoolurile pot fi ingerate de oameni.
- Vezi și: Amine și cetone
Tipuri de alcooli
În funcție de numărul de atomi de carbon de care este atașat atomul de carbon care are gruparea hidroxil atașată, un alcool poate fi:
- Alcool primar. Atomul de carbon care are atașată gruparea hidroxil este, de asemenea, atașat la un singur atom de carbon. De exemplu:
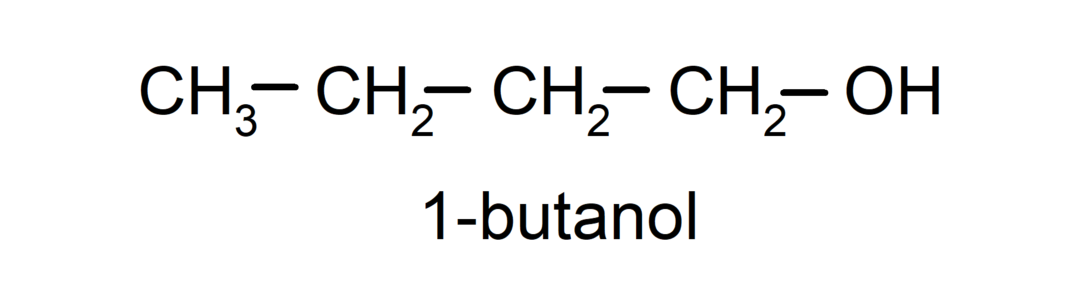
- Alcool secundar. Atomul de carbon care are atașată gruparea hidroxil este, de asemenea, legat de alți doi atomi de carbon. De exemplu:
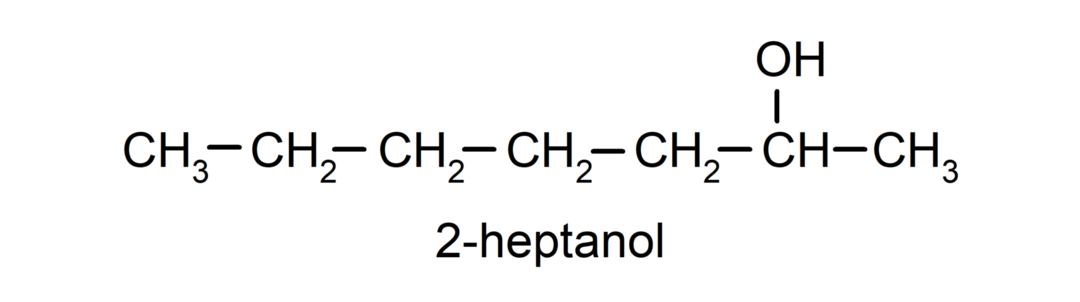
- Alcool terțiar. Atomul de carbon care are atașată gruparea hidroxil este, de asemenea, atașat la trei atomi de carbon. De exemplu:
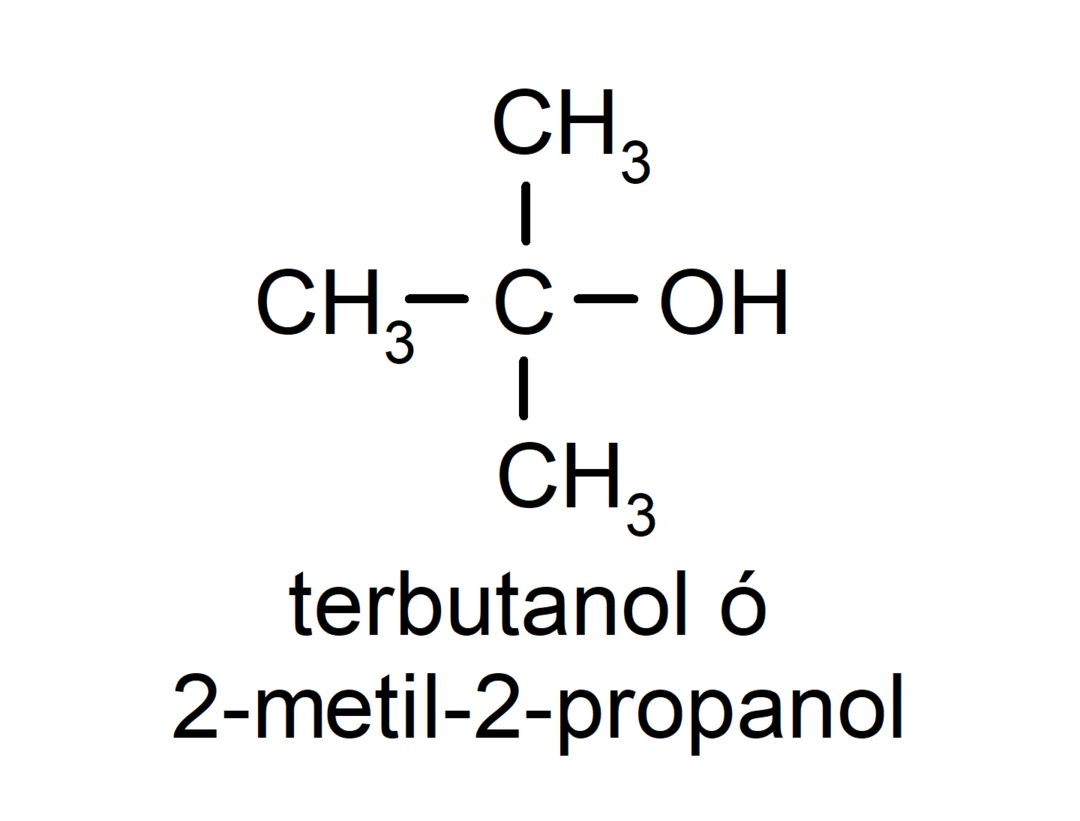
În funcție de numărul de grupări hidroxil pe care le are, un alcool poate fi:
- Diol. Are două grupări hidroxil în structura sa. De exemplu:
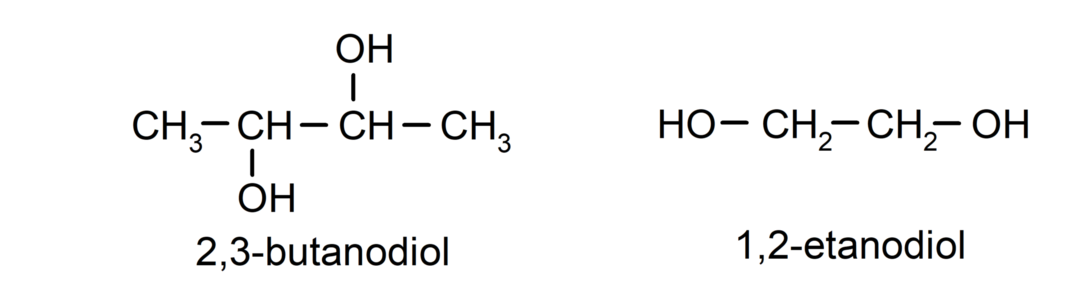
- Triol. Are trei grupări hidroxil în structura sa. De exemplu:
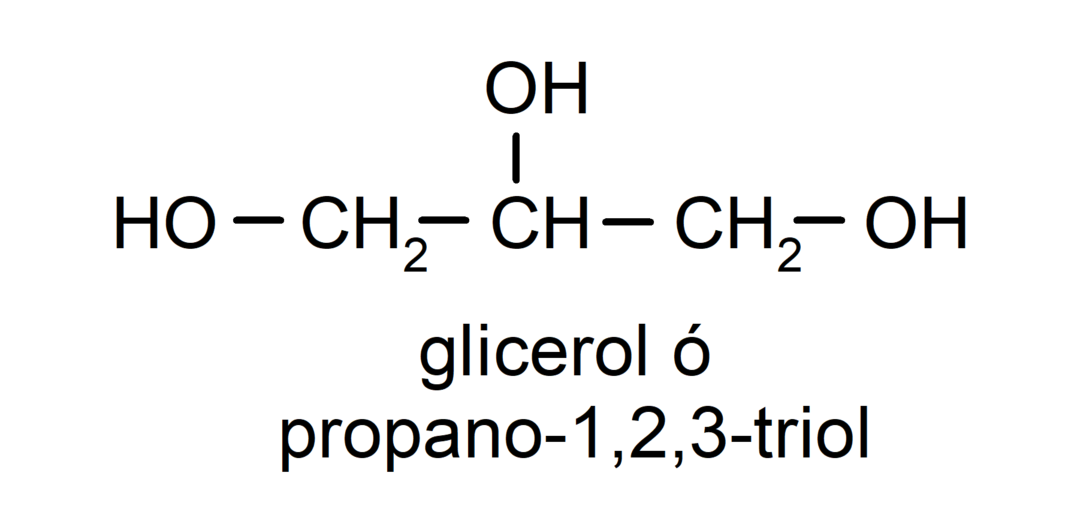
- Polialcool. Are multe grupări hidroxil în structura sa. De exemplu:
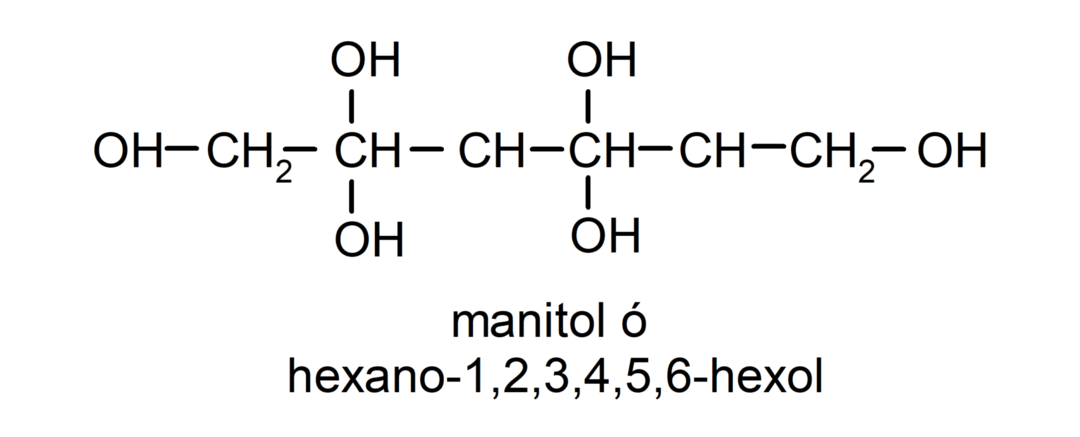
Proprietățile fizice ale alcoolilor
Unele dintre proprietățile fizice ale alcoolilor sunt:
- Punct de fierbere. Punctul de fierbere în alcooli este destul de ridicat datorită prezenței grupării hidroxil, care permite formarea legăturilor de hidrogen. În plus, cu cât sunt prezente mai multe grupări funcționale hidroxil în lanțul de carbon, cu atât este mai mare Punct de fierbere a alcoolilor.
- Polaritate. Alcoolii sunt compuși destul de polari.
- Solubilitate. Alcoolii cu greutate moleculară mică sunt solubili în apă. Pe de altă parte, cu cât lanțul de carbon al alcoolilor este mai mare, cu atât solubilitatea lor în apă este mai mică. În plus, cu cât alcoolii au mai multe grupări hidroxil, cu atât solubilitatea lor în apă este mai mare.
- Starea de agregare. Majoritatea alcoolilor sunt lichizi la temperatura camerei (25ºC) și au mirosuri caracteristice.
Proprietățile chimice ale alcoolilor
Unele dintre proprietățile chimice ale alcoolilor sunt:
- Alcoolii se comportă ca acizii și bazele.. Comportamentul lor ca acizi poate fi observat în reacțiile cu metale active pentru a elibera hidrogen gazos și a forma alcoxizi.

Comportamentul lor ca baze poate fi observat în reacții precum reacția metanolului cu bromură de hidrogen pentru a forma bromură de metiloxoniu.
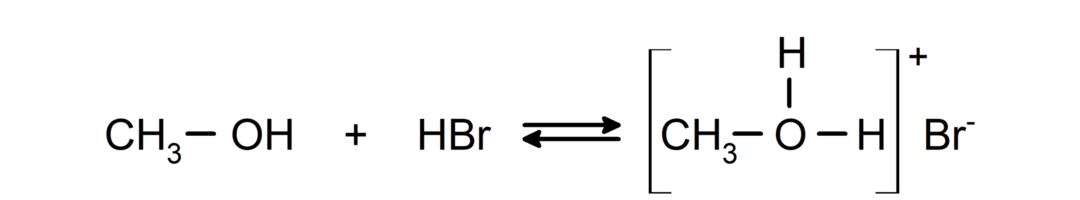
- Alcoolii suferă reacții de halogenare. Ele reacţionează cu halogenuri de hidrogen pentru a forma halogenuri de alchil.
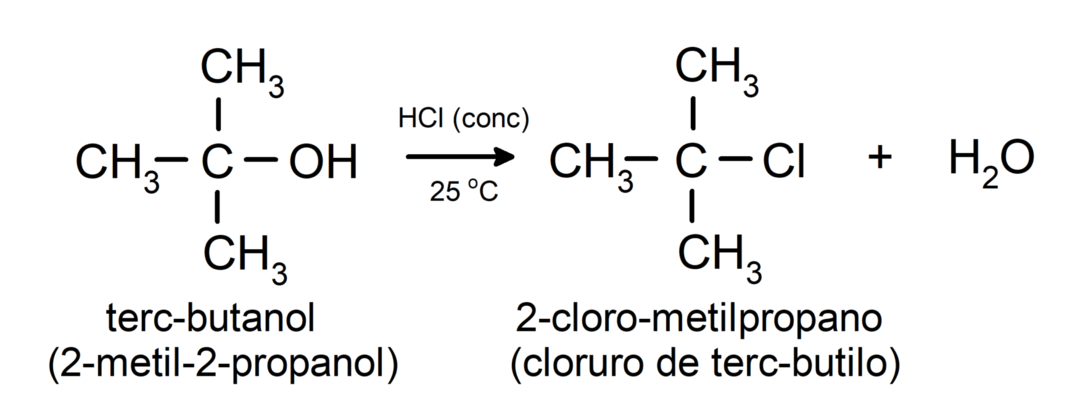
-
Alcoolii suferă reacții de oxidare când reacţionează cu anumiţi compuşi oxidanţi. Produșii reacțiilor de oxidare depind de tipul de alcool care reacționează, adică dacă este primar, secundar sau terțiar.
Oxidarea alcoolului primar pentru a forma aldehidă sau acid carboxilic.
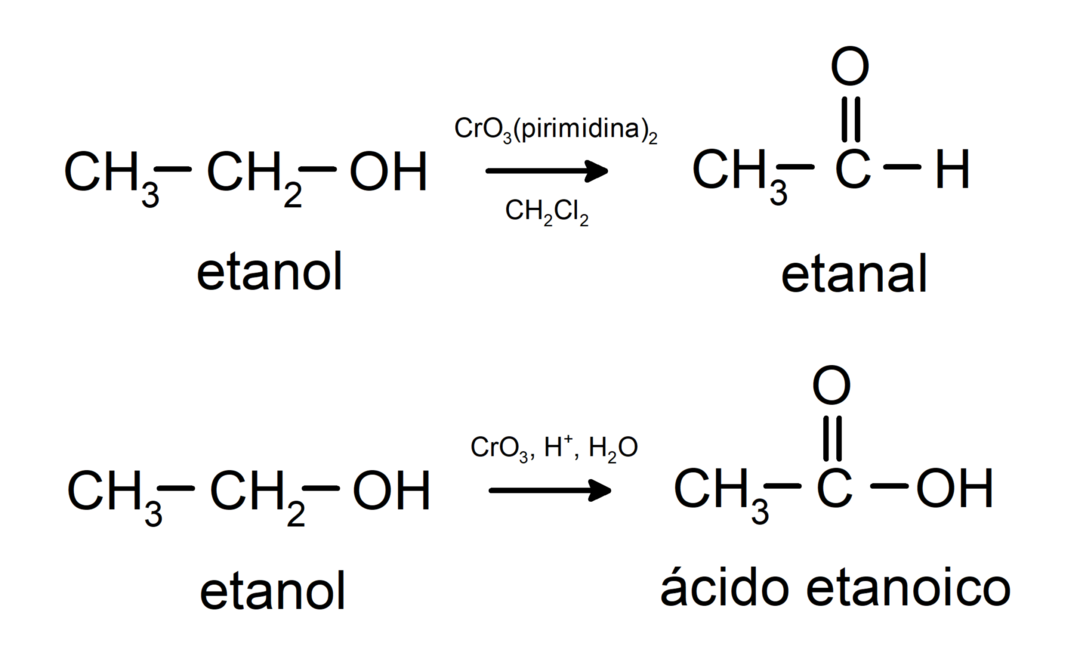
Oxidarea alcoolului secundar pentru a forma cetonă.
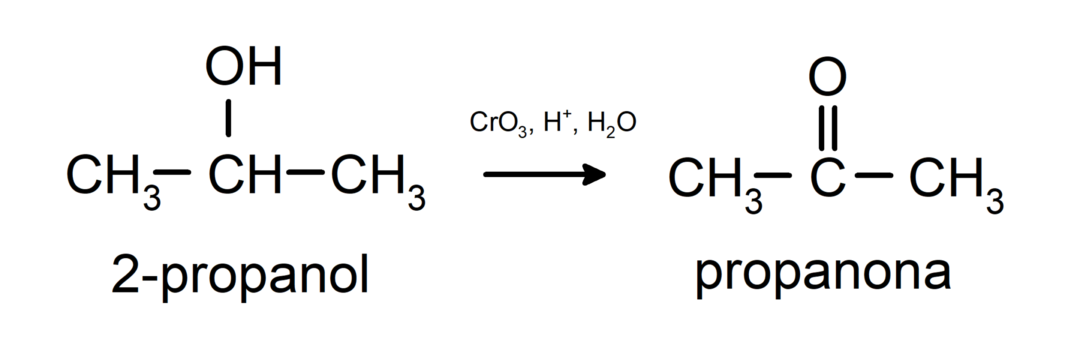
Alcoolii terțiari nu se oxidează cu oxidanți obișnuiți. Cu agenți oxidanți foarte puternici ele pot fi transformate în alchene, care pot fi apoi oxidate.
Alcoolii care au două grupări hidroxil situate pe atomi de carbon adiacente sunt oxidați cu tetraacetat de plumb pentru a forma două cetone.
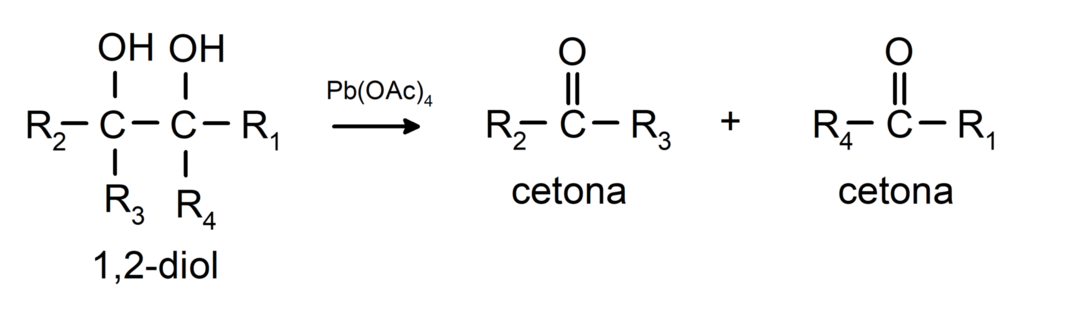
- Alcoolii suferă reacții de dehidrogenare. Aceste reacții apar numai cu alcoolii primari și secundari, care atunci când sunt supuși la temperaturi ridicate în prezența catalizatorilor, eliberează hidrogeni.
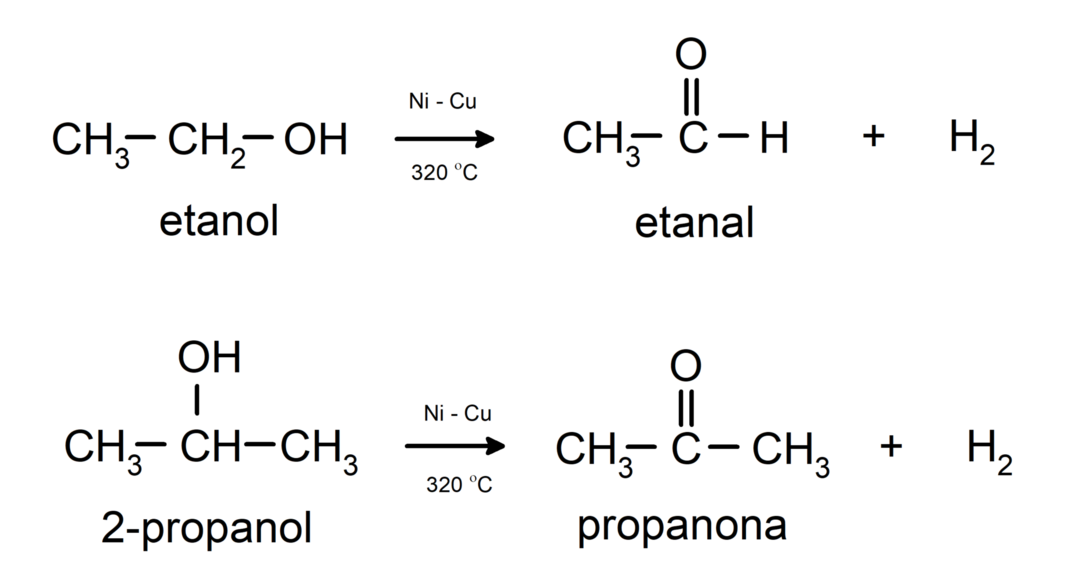
- Alcoolii suferă reacții de deshidratare. Alcoolii se deshidratează pentru a forma alchenele corespunzătoare. Această reacție are loc în prezența temperaturilor acide și intermediare.
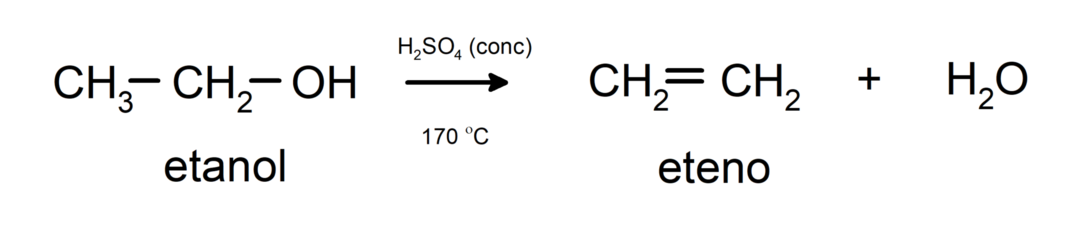
Nomenclatura alcoolului
Conform nomenclatorului stabilit de IUPAC (Uniunea Internațională de Chimie Pură și Aplicată), alcoolii sunt denumiți urmând următoarele reguli:
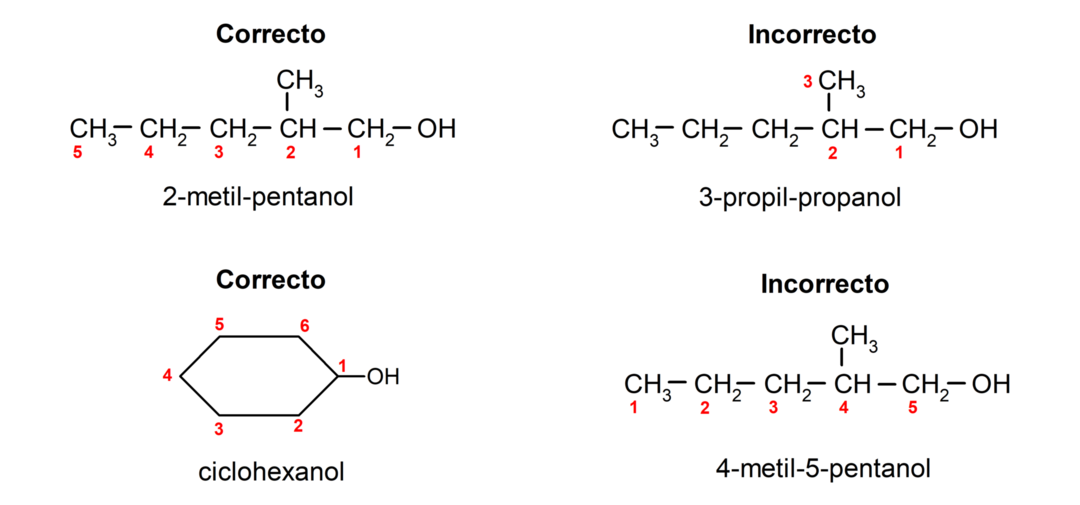
- Poziția grupării hidroxil este aleasă ținând cont de faptul că aceasta ocupă cel mai mic număr posibil în lanțul de carbon. Dacă structura alcoolului este ciclică, se ia în considerare poziția 1 pe carbonul care are atașată gruparea hidroxil și se folosește prefixul ciclo- pentru a-l denumi.
- Numele alcoolului este scris folosind prefixe care indică numărul de atomi din lanțul de carbon și, în plus, este plasat sufixul -ol.
- Dacă structura alcoolului are ramificații, se alege ca lanț principal de carbon cel mai lung lanț care conține și gruparea hidroxil.
Conform nomenclaturii tradiționale, alcoolii sunt denumiți prin scrierea cuvântului „alcool” și apoi scriind numele alcoolului. alcanul corespunzător lanțului de carbon, dar în loc să se folosească terminația -ane a alcanului, terminația -ilic.
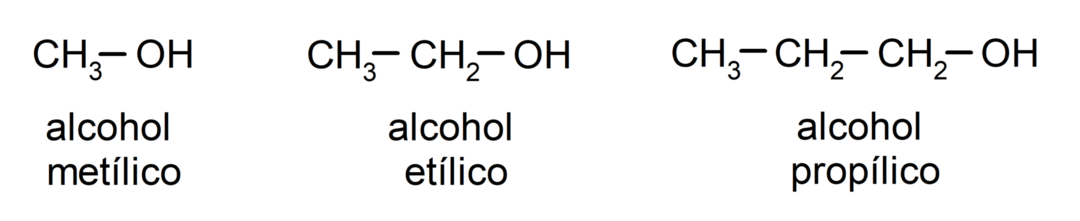
Exemple de alcooli
- metanol
- etanol
- 1-propanol
- 2-propanol
- 1-butanol
- 3-etilhexan-2-ol
- glicerol
- fenol
- 2-metil-2-butanol
- 1,2-etandiol
- 1,5-heptadien-3-ol
- 3-metil-2-butanol
- benzilmetanol
- 3-pentanol
- 2-metilfenol
- 1,2-dihidroxifenol
- cicloheaxnol
- 1-feniletanol


Utilizări ale alcoolilor
Cele mai frecvente utilizări ale alcoolului sunt:
- Sunt folosiți ca dezinfectanți și antiseptice, deoarece opresc creșterea unora microorganisme sau distruge-le. Etanolul și alcoolul izopropilic sunt cele mai utilizate în acest scop.
- Ele sunt utilizate în sinteza diferitelor compuși chimici. Metanolul, de exemplu, este folosit pentru a obține metanal (formaldehidă).
- Sunt folosite pentru a produce antigel. Metanolul este unul dintre cele mai utilizate în acest scop.
- Sunt folosiți ca solvenți în industria farmaceutică. Etanolul este unul dintre cele mai utilizate în acest sens.
- Sunt folosiți ca solvenți pentru lacuri, coloranți și cerneluri. Metanolul este utilizat pe scară largă în acest scop.
- Sunt folosite ca combustibil și există o tendință importantă de a înlocui parțial utilizarea de combustibili fosili prin utilizarea combustibilului bioetanol.
- Sunt folosite pentru a face rășini. Fenolul este folosit în acest sens.
Pericolele consumului de alcool
Deși consumul de alcool este acceptat social astăzi, abuzul de această substanță generează dependență și dependență.
Etanolul este alcoolul prezent în băuturile alcoolice, care atunci când este consumat în exces afectează abilități cognitive și poate provoca boli cardiovasculare, ciroză hepatică și cancer.
Mai mult, atunci când se atinge gradul de intoxicație cu alcool, adică o stare de ebrietate, dacă doza de alcoolul este prea mare, poate apărea o comă alcoolică, care poate duce la paralizie respiratorie și chiar la moarte. moarte.
Referințe
- T. LA. Geissman. (1974) „Principii de chimie organică” Ediția a doua. Editorial Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E. și Valdez-Montero, C. (2017). Consumul de alcool ca problemă de sănătate publică. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T. și Boyd, R. N. (1998). Chimie organica. Educația Pearson.
- Weininger, S. J. și Stermitz, F. R. (1988). Chimie organica. am inversat.
Urmărește cu:
- Alcool etilic
- Combustibili
- Chimie organica
