Exemplu de tensiune la suprafață
Fizică / / July 04, 2021
Tensiunea la suprafață este Forța exercitată pe suprafața unui lichid care este în repaus, pentru a contracara greutatea unui obiect ușor care se sprijină pe el. În plus, tensiunea de suprafață poate fi definită ca Forța exercitată de un lichid pentru a rezista la ruperea suprafeței sale. Este principala proprietate care deține bule de săpun, consistente și ferme.
Lichidele au una dintre principalele lor proprietăți un volum fix, a căror formă va varia în funcție de recipientul care le conține. Lichidele se adaptează la forma recipientului, ocupând întotdeauna cea mai joasă parte a acestuia prin gravitație. În acest fel, lasă o suprafață liberă, nu total plană, sau adoptă forme speciale precum picături, bule sau bule.
Există atunci Forțele de suprafață, apeluri Coeziune și adeziune, care sunt explicate mai jos:
Coeziune: Este atunci când două suprafețe lichide diferite sunt afectate de o forță de atracție una față de cealaltă, care este activată în moleculele cele mai exterioare.
Aderare: Este atunci când un lichid este încorporat prin atracție la suprafața unui solid, difuzând în acea zonă.
Acestea doua Forțele de suprafață sunt responsabile de diverse fenomene biologice, bazat pe conceptele de tensiune superficială și capilaritate.
Tensiune de suprafata
Într-un lichid, fiecare moleculă este înconjurată de mai multe molecule; în acest fel atracția în toate direcțiile este compensată în fiecare punct al lichidului, cu excepția suprafeței, unde nu există molecule deasupra, ci doar aer, forțele sunt direcționate în lichid, generând astfel o atracție netă către acel conținut.
Lichidul, atunci, tinde să facă coeziune, care este la fel ca să nu se disperseze, și să-și minimizeze suprafața, formând picături. Suprafața lichidului va avea comportamentul unui film care oferă rezistență la deformare și, prin urmare, rezistență la rupere.
Pentru a măsura această Forță de Coeziune, se are în vedere o structură de sârmă cu o latură glisantă, în care este plasat un strat de lichid. O comparație simplă a acestei structuri este cu un inel de suflare cu bule de săpun, în care puteți glisa puțin firul pentru a face inelul mai mare.
lichidul va încerca să minimizeze suprafața, desemnată de S, exercitând o forță F pe partea glisantă, care poate fi măsurată. Se concluzionează că calculul Forței rămâne:
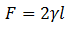
Unde γ este tensiunea de suprafață și l este lungimea cablului care alunecă.
Tensiunea la suprafață γ este o proprietate a lichidului. Forța F va depinde de l, lungimea cablului glisant, dar nu de suprafața S. Factorul 2 este introdus deoarece există două suprafețe, care sunt cea internă și exterioară a firului glisant, care este în contact cu cea a lichidului.
Tensiunea suprafeței γ este Forța pe unitate de lungime exercitată de o suprafață a unui lichid pe orice linie, situată pe ea ca o margine de prindere.
Forța originară din tensiunea superficială este perpendicular pe linia de suprafață și tangentă la aceasta.
Tensiunea de suprafață γ poate fi, de asemenea, definită ca Energie pe unitate de suprafață care este necesar pentru a crește o zonă și este exprimat cu următoarea formulă:
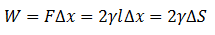
Deoarece energia este necesară pentru a se forma o suprafață, lichidele tind să-și reducă zona expusă în raport cu împrejurimile. În această privință, suprafețele corpurilor de apă, cum ar fi lacurile, mările și oceanele într-o stare calmă, sunt plane.
Tensiune de suprafata se măsoară în Newton fiecare metru (N / m), iar pentru fiecare substanță scade odată cu creșterea temperaturii. Cel al apei este mai mare decât în majoritatea lichidelor și se datorează și faptului că este unul dintre cele mai dense lichide, cu 1 g / cm3 densitate.
Mai jos este un tabel cu valorile unor substanțe, tipice unei serii de temperaturi.
Lichid |
T (° C) |
γ (N / m) |
Heliu |
-270 |
0.0002 |
Hidrogen |
-255 |
0.002 |
Neon |
-247 |
0.005 |
Oxigen |
-193 |
0.016 |
Etanol |
20 |
0.022 |
Apa cu sapun |
20 |
0.025 |
Apă |
100 |
0.059 |
Apă |
60 |
0.062 |
Apă |
20 |
0.073 |
Apă |
0 |
0.076 |
Mercur |
20 |
0.465 |
Argint |
970 |
0.800 |
Surfactanți sau surfactanți
Uneori este necesar să se reducă tensiunea superficială a unui lichid. Este dus la bun sfârșit dizolvând în el substanțele numite Surfactanți sau Surfactanți, care formează un film de suprafață ale cărui molecule sunt abia atrase de moleculele lichidului interior.
Datorită agenților tensioactivi, lichidul în cauză este mai ușor să se ude.
Exemple de tensiune la suprafață
Țânțarul care aterizează pe apă, rămânând suspendat la suprafață.

O placă de polistiren sau polistirol suspendat în apă.

Foaia de apă care se formează pe inel înainte de a sufla o bulă de săpun.

Cele mai ușoare particule de nisip sau praf, dacă nu sunt agitate, rămân suspendate la suprafața apei.

Când există apă și ulei într-un pahar, există tensiune superficială în separarea dintre cele două prin densitate.

Când o băutură aromată este agitată mult, bulele generate rămân la suprafață, fiecare implicată în tensiunea totală a suprafeței.

Spuma de apă cu săpun în funcționarea unei mașini de spălat are bule și bule care se formează înainte de clătire.

Navele profită de această proprietate a apei pentru a rămâne pe linia de plutire, datorită faptului că transportă aer în interior. Sunt ca o bulă plutitoare la suprafața apei.

Plăcile de surf creează tensiune superficială atunci când apa este în repaus, iar atunci când există mișcare, ele se mențin ferm.

Când laptele crud este fiert, începe generarea unei creme, care se consolidează atunci când laptele se răcește. Este un strat gros de grăsime deasupra părții lichide.

Nu uitați să vă lăsați comentariile.

