Пример закона Дальтона
Химия / / July 04, 2021
Английский ученый Джон Далтон (1766-1844) был физиком и химиком, внесшим большой вклад в сжатие и классификацию элементов и химикатов. Среди его основных вкладов - первая модель представления атомов и соединений посредством графического изображения. Он также сформулировал так называемый «закон множественных пропорций», также известный как закон Дальтона.
Что касается химических соединений, Луи Пруст (1754-1826) сформулировал «Закон постоянных пропорций», в котором он собирает наблюдение, что химические вещества всегда соединяются в одинаковой пропорции, чтобы произвести одни и те же соединения. То есть, если объединить водород и кислород, они всегда будут объединяться в одинаковых пропорциях, чтобы получить воду. Однако этот закон не объяснял, как существуют разные соединения, состоящие из одних и тех же веществ.
С помощью своей атомной теории Дальтон понял, что когда некоторые простые вещества объединяются, они могут производятся различные соединения, и что количество одного из веществ изменяется в пропорциональной пропорции просто.
Закон Далтона сформулирован так: Вес одного элемента, который соединяется с одним и тем же количеством другого с образованием различных химических соединений, изменяется в соответствии с очень простой зависимостью..
Это означает, что если мы знаем, как вещества соединяются в простых пропорциях, и количество одного из веществ остается постоянным, а другое вещество, которое мы кладем в простой пропорции, в соотношении 2, 3 или 4 по отношению к исходной пропорции, в каждом случае мы получим вещество разные. Это происходит, например, при соединении фосфора, водорода и кислорода.
Если мы объединим 1 объем фосфора, 3 объема водорода и 2 объема кислорода, мы получим гипофосфорную кислоту:
P + 3H + 2O -> PO2ЧАС3
Если в предыдущей реакции мы изменим только кислород в простой пропорции 2, мы получим фосфорную кислоту:
P + 3H + 4O -> PO4ЧАС3
Следует учитывать, что в то время концепция атомной валентности еще не была известна, поэтому не было точно известно, почему одни вещества могут быть объединены в различных пропорциях, а другие нет.
Пример закона Дальтона
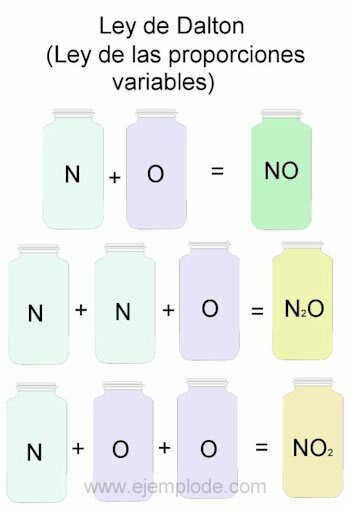
Чтобы проиллюстрировать закон Дальтона, мы возьмем за образец комбинации азота (N) и кислорода (O).
При их соединении в одинаковой пропорции, то есть по одному, мы получим оксид азота:
N + O -> НЕТ
Если мы сохраним объем азота постоянным и изменим содержание кислорода на 2, мы получим перекись азота:
N + 2O -> НЕТ2
Если, исходя из оксида азота, мы теперь сохраним кислород постоянным и изменим объем азота на 2, мы получим закись азота:
2N + O -> N2ИЛИ ЖЕ
Если статья была вам полезна, не забудьте поставить нам +1.



