Пример органической химии
Химия / / July 04, 2021
В Органическая химия Это часть общей химии, отвечающая за изучение и функциональную классификацию химических соединений, структурным элементом которых является Углерод, в изобилии присутствующие в живая материя; Это создает очень дифференцированную вселенную неорганической химии, посвященную химическим соединениям, классифицируемым как минералы.
Атом углерода имеет четыре электрона в последней оболочке своей электронной конфигурации. Эта характеристика, вместе с характеристикой его атомного радиуса, позволяет соединять его ковалентными связями с другими атомы одного и того же элемента в многочисленных цепочках, образующих большое разнообразие химических соединений стабильный.
Вы можете проверить Ковалентные связи.
Такие химические соединения, в дополнение к атомам углерода, которые придают им их изначальную структуру, содержат атомы водорода в качестве основного дополнения валентности углерода. Кроме того, в этом разнообразии соединений есть соединения с участием атомов кислорода, Азот, галогены, сера и даже фосфор, щелочные и щелочноземельные элементы и металлы переход. В зависимости от того, кто участвует в молекуле, это будут физические и химические свойства конечного вещества.
В органические соединения присутствуют повсюду живая материя; продвигать и поддерживать все биологические функциив отличие от неорганических или минеральных веществ, которые люди использовали в коммерческих целях, для экспериментов или для выполнения определенных домашних задач.
История органической химии
До 1828 года различие между органической химией и неорганической химией уже проводилось. Органическое вещество было связано с творением через "жизненная сила", а неорганическое - с неживым, с минералом. Учитывая эти концепции, нельзя было ожидать получения органических соединений из неорганических материалов в лаборатории.
Тем не мение, в 1828 году Фридрих Велер (1800-1882) удалось приготовить органическое вещество, Мочевина CO (NH2)2, важный продукт метаболизма животных, из неорганических соединений. Уход Цианат свинца Pb (CNO)2 с участием Аммиак NH3 получить Цианат аммония NH4CNO; Это соединение действительно образовалось, но когда раствор кипятили для кристаллизации цианата аммония, он превратился в мочевину.
Это химическое изменение является примером Внутренняя перегруппировка, в котором количество или класс атомов в молекуле не изменяется, а изменяется только их порядок в ней. Эти типы превращений очень распространены в органической химии.
Открытие Велера положило начало отказу от теории жизненной силы, позже полностью отвергнуты, за ними последовало получение многих других органических соединений в лаборатория. Несмотря на это, квалификаторы неорганических и органических остаются, поскольку неорганические соединения относятся к минеральным продуктам. а органические соединения, которые на самом деле являются соединениями углерода и водорода и их производными, относятся к тому типу, который вырабатывается живыми организмами.
Хотя законы общей химии в равной степени применимы к обоим соединениям, разные причины оправдывают и делают это разделение необходимым. Таким образом, органические и неорганические соединения различаются разными свойствами, такими как: Растворимость предпочтительны в органических растворителях (эфир, спирт, хлороформ и т. д.) и в воде, соответственно, его Стабильность (органические соединения разлагаются при относительно низких температурах), а Природа реакций; для неорганических соединений они ионные, простые и практически мгновенные, а для органических соединений - ковалентные, сложные и медленные.
Органические соединения
Известны углеродные соединения с цепями до девяноста атомов. В цепи Атомы углерода могут быть линейные и разветвленные и имеют одинарные ковалентные связи или двойные или тройные связи. Известно, что более 2500 соединений содержат только углерод и водород (Углеводороды).
Изомерия органических соединений
В неорганических соединениях формула обычно представляет собой одно соединение; таким образом, существует только одно вещество формулы H2ЮЗ4. Молекула серной кислоты содержит два атома водорода, один серы и четыре атома кислорода, в определенном и уникальном расположении. В органических соединениях это редко такое случается. Так, например, есть два соединения, которые отвечают формуле C2ЧАС6Или этиловый спирт или этанол и диметиловый эфир.

Чем сложнее молекула, то есть чем больше количество атомов углерода, тем больше количество возможных изомеров.
Анализ органических соединений
Анализ органического соединения включает качественный анализ, то количественный анализ и Функциональный анализ. В случае предположения, что соединение находится в неочищенном состоянии, его предварительно очищают с помощью Кристаллизация, Дистилляция, Сублимация, Добыча, так далее. О критерии чистоты можно судить по его физическим константам, таким как точка плавления, точка кипения, плотность, растворимость, кристаллическая форма, показатель преломления и т. Д.
В качественный анализ Это подтверждается исследованием присутствия элементов, входящих в состав соединения, особенно углерода, водорода и азота, а иногда и галогенов, серы и фосфора.
В количественный анализ Он проводится на основе методов, используемых для качественного анализа. Отправной точкой является определенное количество вещества, которое подвергается сгоранию, а углекислый газ собирается и взвешивается. углерода и водяного пара, чтобы рассчитать процентное содержание углерода и водорода в сложный. Результаты количественного анализа облегчают расчет эмпирическая формула, хотя молекулярную формулу можно узнать только после определения молекулярной массы вещества. Но проблема еще не решена, потому что одна и та же молекулярная формула может соответствовать разным изомерам.
Классификация органических соединений
По своему строению органические соединения делятся на соединения. алифатический, ароматный Y гетероциклический. Алифатические соединения относятся к метану CH4, представляют собой открытые цепи, за исключением циклопарафинов, и обязаны своим названием тому факту, что животные и растительные жиры принадлежат к этой группе.
В ароматические соединения, замкнутая цепь, близкородственная бензолу, C6ЧАС6, и своим названием они обязаны тому факту, что многие из них имеют приятный ароматный запах.
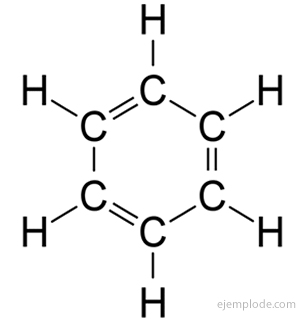
Бензольное кольцо
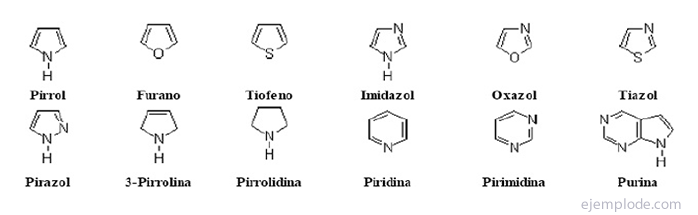
В гетероциклические соединения Это соединения с замкнутой цепью, в кольце которых есть элемент, отличный от углерода.
По своему строению они:
Углеводороды, который, в свою очередь, из-за типа имеющихся ссылок классифицируется как Алканы, Алкенес Y Алкины. Кроме того, в эту категорию входят циклоалканы, бензол и их производные, состоящие только из углерода и водорода.
Гетероциклические соединения
Галогенированные производные:R-X
Нитросоединения:Р-НЕТ2
Сульфоновые кислоты:R-SO3ЧАС
Нитрилы (OR алкилцианиды) и изонитрилы:R-CN и R-NC. Они различаются тем, как атом азота связан в молекуле.
Спирты:R-OH
Фенолы: Соединения на основе основной цепи, состоящей из бензольного кольца с добавленной гидроксильной группой.

Эфиры:R-O-R
Меркаптаны: R-SH
Тиоэфиры:R-S-R
Тиокислоты:R-COSH
Альдегиды:R-CHO
Кетоны:R-CO-R
Карбоновые кислоты:R-COOH
Вы выходите:R-COOM (M для металла)
Сложные эфиры: R-COO-R
Ангидриды: R-CO-O-OC-R
Амины:R-NH2, R-NH-R, 2R-N-R
Углеводы типа альдоса:-CHOH-CHOH-CHO
Углеводы кетозного типа:-CHOH-CO-CH2ой
Металлоорганические соединения:R-M-R
Металл-алкилгалогениды:R-MX (также известные как реактивы Гриньяра)

