10 Príklady plynných zmesí
Rôzne / / July 04, 2021
Zmesi plynné látky Sú jedny z najľahšie dosiahnuteľných, pretože je veľmi možné, že sa látky, ktoré sú v tomto stave agregácie, zmiešajú. Napríklad: Neónové, argónové a xenónové zmesi, aerosólové insekticídy, vzduch a hélium.
Prakticky všetky plyny je možné kombinovať neobmedzene, samozrejme niektorými podmienkami chemické, fyzikálne a zásadne súvisiace s aspektmi bezpečnosti používateľa, ktoré manipuluje. Rovnako ako rôzne typy zmesí, ktoré sa vytvárajú medzi látkami, aj zmesi plyny majú tiež vlastnosti, ktoré sú pre ne jedinečné.
Štúdia bublinkové zmesi je zvyčajne rovnako užitočné ako plyny v ich čistom stave: rovnaké vedomosti o vzduchu, ktorý je prítomný v atmosféra by bola nemožná, nebyť znalostí o proporciách a správaní sa zmiešaných plynov.
Týmto spôsobom je nevyhnutné niektoré poznať Vlastnosti plynných zmesí, ako napríklad vlastnosť parciálneho tlaku (vyvíjaného každým z plynov v zmesi) a molárnej frakcie (pomer medzi počtom mólov plynnej zložky a počtom mólov celkovej zmesi sóda). Mole vyjadrujú množstvo plynu v zmesi.
The Daltonov zákon uvádza, že celkový tlak plynnej zmesi sa rovná súčtu parciálnych tlakov každého z nich jeden z jednotlivých plynov, ktoré sa na ňom podieľajú (to je predmetom plynov, ktoré medzi nimi nereagujú Áno). Parciálny tlak sa tu chápe ako tlak, ktorý by vyvíjal každý z plynov, keby sa nachádzal iba v tej istej nádobe a za rovnakých podmienok teplota. A) Áno:
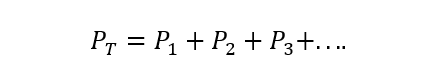
Kde PT je celkový tlak a P1, P2 A p3 sú parciálne tlaky hypotetických plynov 1, 2 a 3 v zmesi plynov.
Pomocou Daltonovho zákona bol vyvinutý výraz na výpočet čiastočný tlak plynu v plynnej zmesi, ak poznáme jeho celkový tlak a jeho molárny zlomok.
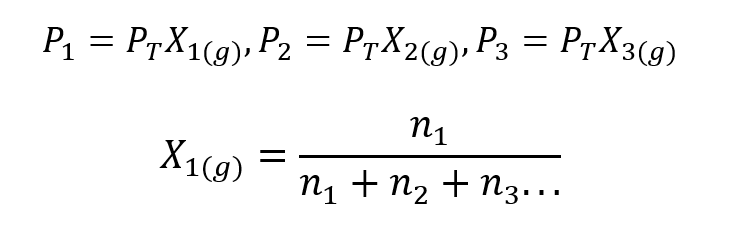
Kde X1, X2 Y. X3 sú molárne frakcie hypotetických plynov 1, 2 a 3 v plynovej zmesi a n1, n2 Y. n3 sú množstvá látky každého z týchto plynov v tej istej zmesi.
Jeden z hlavné vlastnosti zložiek v zmesiach je koncentrácia, ktorú je možné vyjadriť v rôznych jednotkách. V prípade plynných zmesí možno koncentráciu ich zložiek vyjadriť v ppm (ppm), jednotke vzťahujúcej sa na jej objem. To znamená, že určité množstvo ppm zložky v zmesi plynov je pomer objemu tohto určitého množstva k objemu každého milióna jednotiek zmesi.
Je dôležité si to uvedomiť ppm plynu závisí od teploty a tlaku plynu. Z tohto dôvodu sa na výpočet ppm plynu zvyčajne používajú bežné podmienky tlaku a teploty. (CNPT), ktoré poskytujú normálny stav na teplotu 0 stupňov Celzia a 1013 hektopascalov (1 bar) Tlak. Ak sa tieto podmienky nepoužívajú, musíte určiť, ktoré sa použijú.
Môže vám slúžiť:
Príklady plynných zmesí
Nasledujúci zoznam obsahuje zmesi plynov s uvedením prvkov, ktoré sa v zmesi nachádzajú:
- Vzduch (zmes 21% kyslíka a 79% dusíka a ďalšie plyny v malom množstve)
- Cronigón (zmes 99% argónu a 1% kyslíka)
- Trimix (zmes kyslíka, dusíka a hélia)
- Neónové, argónové a xenónové zmesi
- Zmes 85% metánu, 9% etánu, 4% propánu a 2% butánu.
- Hexafluorid sírový a vzduch
- Aerosólový insekticíd
- Vzduch a hélium
- Nitrox (zmes vzduchu, obohatená o kyslík a dusík)
Postupujte podľa:



