Pojem v definícii ABC
Rôzne / / December 09, 2021
Koncepčné vymedzenie
Hydrolýzou sa rozumie akákoľvek reakcia vody s látkou, ktorá spôsobí vytesnenie ionizačnej rovnováhy vody.

Chemický inžinier
K javu dochádza napríklad vtedy, keď sa soľ rozpustí Voda, kde je soľ, ktorá je elektrolytom, úplne ionizovaná a pri reakcii s vodou môže vytvárať hydroxyl alebo hydrónium. Z disociácie soli sa pH a rozpustenie s vedomím, že čím vyšší je charakter kyselina alebo bázickej zlúčeniny, tým nižší je hydrolytický účinok.
Silné a slabé kyseliny
Zoberme si typický príklad, akým je HCl, je to silná kyselina, ktorá sa pri ionizácii správa nasledovne:
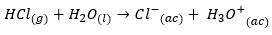
Na štúdium účinku hydrolýzy sa zameriame na konjugovanú bázu: C {l ^ -} {(ac)}, tento anión je slabá konjugovaná báza, to znamená, že má slabú tendenciu odoberať protón z vody za vzniku a hydroxid. Zatiaľ čo, ak uvažujeme o slabej kyseline, napr.
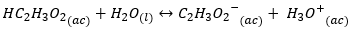
Jeho konjugovaná báza C_2 {{H_3O_2} ^ -} _ {(ac)} \ bude mať silne zásaditý charakter, čo povedie k tvorbe hydroxidu:
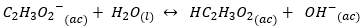
východ Zostatok je posunutý smerom k priamemu smeru reakcie doprava a v dôsledku toho má tento anión vysokú schopnosť ovplyvňovať pH prostredníctvom
výroby hydroxyl. Zatiaľ čo v prípade Cl- neexistuje žiadny vplyv na pH roztoku.Ak je konjugovaná báza, anión, a druhov schopný zachytávať protóny z vody, potom sa pH roztoku zvyšuje v dôsledku tvorby OH-.
Silné a slabé základy
Pozrime sa teraz na prípad silných alebo slabých zásad, ktoré čiastočne alebo úplne ionizujú vo vode a môžu, ale nemusia ovplyvniť pH roztoku.
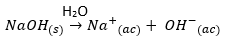
Ak vezmeme {{Na} ^ +} {(ac)}, malý katión, slabú kyselinu, neovplyvní to pH roztoku, pretože nie je schopný darovať protóny vode. Pokiaľ:
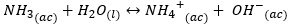
Katión {{NH_4} ^ +} {(ac)} je silná kyselina, ktorá pochádza zo slabej zásady (amoniak). Preto má schopnosť darovať protón vode (hydrolyzovať) nasledovne:
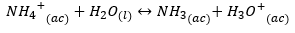
To vysvetľuje, prečo rozpúšťanie amoniaku vo vode znižuje pH, vzhľadom na tvorbu hydronií. V tomto prípade, posunutie rovnováha je vpravo.
Rozpúšťanie solí
Rovnako ako sme videli účinok katiónov a aniónov oddelene, keď sa rozpúšťajú Choď von vo vode sa oba účinky kombinujú a v závislosti od relatívnej schopnosti iónov reagovať s vodou bude prevládať tvorba hydroxylových hydroxylov nad hydróniami alebo naopak.
Aby sme to lepšie pochopili, budeme pracovať s niekoľkými prípadmi:
- Ak kuchynskú soľ rozpustíme vo vode, v Riešenie Budeme mať Na + katióny a Cl- anióny. Ako sme videli predtým, oba druhy majú malú schopnosť reagovať s vodou, a preto ani jeden z nich nebude schopný upraviť pH základnej vody. Potom sa očakáva, že pH je 7. V tomto prípade sa rozpustí silný zásaditý konjugovaný katión, bude to slabá kyselina, ktorá neovplyvňuje pH. A konjugovaný anión silnej kyseliny, slabá zásada, tiež nemení pH.
- Na druhej strane, ak je soľ, ktorej konjugovaný katión slabej zásady je rozpustený, ide o silnú kyselinu. Zatiaľ čo ak je anión konjugovaný so silnou kyselinou, bude to slabá zásada neschopná reagovať s vodou. Čo bude prevládať, bude reakcia silnej konjugovanej kyseliny s vodou darujúcimi protóny a znížením pH.
- Opak nastane, ak je katión konjugátom silnej zásady (slabá kyselina) a aniónom je konjugát slabej kyseliny (silná zásada). Prevládať bude reakcia silnej zásady s vodou, zvýšenie produkcie OH- a následne zvýšenie pH.
- Nakoniec môže nastať prípad, keď anión a katión sú silné zásady a kyseliny, ktoré môžu ovplyvniť pH. V tomto prípade treba sledovať, ktorá reakcia prevažuje nad druhou, či vzniká OH- alebo H3O+. Aby sme to dosiahli, musíme sa uchýliť ku konštantám kyslosti a zásaditosti: ak je konštanta kyslosti väčšia ako konštanta zásaditosti, pH bude menšie ako 7. Naopak, ak konštanta zásaditosti prevažuje nad konštantou kyslosti, pH bude vyššie ako 7. Stručne povedané, keď sú obe konštanty rovnaké, pH = 7 a je podobné ako v prvom študovanom prípade.
Témy v hydrolýze