20 Primeri idealnega plina in pravega plina
Miscellanea / / July 04, 2021
The kemije ali je znanosti ki preučuje sestavo in preobrazbe, ki se lahko pojavijo v snovi v kateri koli njeni obliki. Eno najpomembnejših področij študija kemije je plini.
The koncept plina Ustanovil ga je belgijski kemik Jan van Helmont. Za razlago vedenja plinov so z uporabo statističnih orodij razvili različne matematične enačbe. Vendar je bilo treba te enačbe poenostaviti in spremeniti, ker niso delovale pri vseh vrstah plinov, zato so bili opredeljeni različni modeli plinov (idealen plin Y. pravi plin, med drugimi vmesnimi pristopi). Na primer: dušik, helij, metan.
V tem smislu so bili vzpostavljeni trije zakoni, ki na splošno povezujejo obseg, temperatura in tlak plinov:
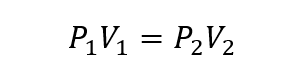
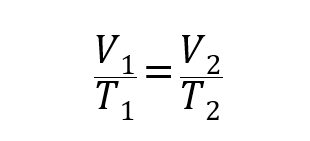
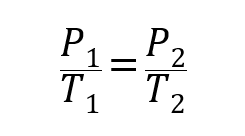
Kje P1, V1 Y. T1so začetni tlak, prostornina in temperatura plina, in P2, V2 Y. T2 so finale.
Tako v povezavi s tremi zakoni dobimo Splošni zakon o plinu,
PV / T = C kje C je konstanta, ki je odvisna od količine plina.
Primeri idealnih plinov
The idealen plin gre za teoretični model, ki predstavlja plin, ki v resnici ne obstaja. Je orodje za lažje število matematičnih izračunov, saj močno poenostavi zapleteno vedenje plina. Šteje se, da je ta plin sestavljen iz delcev, ki se niti ne privlačijo niti ne odbijajo in katerih trki so popolnoma elastični. Gre za model, ki ne uspe, če je plin izpostavljen visokim pritiskom in nizkim temperaturam.
The splošna enačba idealen plin je rezultat kombinacije zakonov Boyle-Mariotteja, Charlesa in Gaya Lussca z Avogadrovim zakonom. Avogadrov zakon določa, da če imajo različne plinaste snovi enake količine in so pod enakim tlakom in temperaturo, imajo enake številko delcev. Tako je enačba stanja idealnega plina: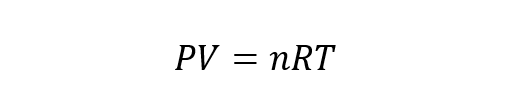
Kje n je število molov plina in R je plinska konstanta enaka 8.314 J / Kmol.
Natančnega seznama idealnih plinov ni mogoče sestaviti, ker je hipotetični plin. Lahko naštejemo niz plinov (vključno s plemenitimi plini), katerih obdelava se lahko približa obdelavi plinov idealno, ker so lastnosti podobne, če so tlačni in temperaturni pogoji normalno.
- Dušik (N2)
- Kisik (O2)
- Vodik (H2)
- Ogljikov dioksid (CO2)
- Helij (He)
- Neon (Ne)
- Argon (Ar)
- Kripton (kr)
- Ksenon (Xe)
- Radon (Rn)
Primeri pravih plinov
The pravi plini So tisti, ki imajo termodinamično vedenje in zato ne sledijo enaki enačbi stanja kot idealni plini. Pri visokem tlaku in nizki temperaturi je treba pline neizogibno šteti za resnične, saj se v tem primeru povečujejo interakcije med njihovimi delci.
The bistvena razlika med idealnim in realnim plinom je, da slednjega ni mogoče stisniti v nedogled, vendar je njegova kompresijska sposobnost odvisna od ravni tlaka in temperature.
Za razlago vedenja realnih plinov so bile razvite različne enačbe. Ena najpomembnejših je tista, ki jo je leta 1873 zagotovil Van der Waals in jo je treba uporabljati v pogojih visokega tlaka. The Van der Waalsova enačba je predstavljen kot:
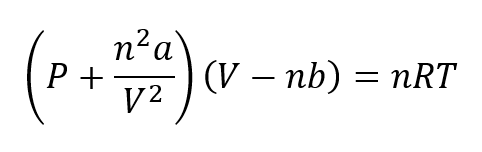
Kje doY. bso konstante glede na naravo vsakega plina.
Naslednji seznam prikazuje nekaj primerov pravih plinov, lahko pa dodate tudi tiste, ki že obstajajo so bili navedeni kot idealni plini, tokrat pa v kontekstu visokega in / ali nizkega tlaka temperatura.
- Amoniak (NH3)
- Metan (CH4)
- Etan (CH3CH3)
- Ethene (CH2CH2)
- Propan (CH3CH2CH3)
- Butan (CH3CH2CH2CH3)
Sledite z:

