Primer volumetrične analize
Kemija / / July 04, 2021
Vklopljeno Analitična kemija, Volumetrija je metoda analize, ki je sestavljena iz Merjenje prostornine reagenta, potrebnega za stehiometrično reakcijo z analitom, ki je snov, ki jo je treba določiti.
Reagirajte stehiometrično se nanaša na snovi, ki kemično medsebojno delujejo, v skladu s delež, ki označuje kemijsko enačbo že uravnoteženo.
Snov, ki jo je treba raziskati, se imenuje Analit. Iz te snovi se za vzorec vzame znana in natančno izmerjena prostornina, ki jo bomo imenovali Alikvot, ki je vsebovana v erlenmeyerjevi bučki za začetek analize.
Pojmi volumetrične analize
Volumetrična analiza kot vrsta Kemijska analiza, nositi vključena kemična reakcija. Ta kemična reakcija bo izvedena med vzorcem z neznano količino preiskovane snovi in znano količino druge snovi, ki lahko reagira s prvo.
The Reakcijske snovi bodo v vodni raztopini, izmerjene pa bodo količine raztopin, ki so medsebojno vplivale do konca reakcije, kar bo vidno zahvaljujoč indikatorju, ki bo dal barvo v bučki.
V volumetrični analizi je vodna raztopina
Znana koncentracija se imenuje standardna raztopina, Standard ali Titrantin bo služil kot referenca za zaključek reakcije za izračun, ki bo razkril količino preiskane snovi.Ta postopek za sprožitev reakcij obeh rešitev se imenuje Kemijska stopnja o Vrednotenje, ki je temeljni del volumetrične analize. Sestavljen je iz iti postopoma vlijemo standardno raztopino (Titrant) v alikvotu (Vzorec), dokler indikator ne prikaže spremembe z barvno razliko.
A Kazalnik To je kemična snov, ki se doda Aliquotu in pokaže obarvanost in da bo po koncu reakcije spremenila barvo.
Volumetrična analiza je sestavljena iz preprostega niza korakov:
1. - Priprava standardne raztopine
2. - Priprava vzorca ali alikvota
3. - kemijska stopnja
4. - Merjenje prostornine
5. - Izračun preiskane snovi.
Do točke, ko so že popolnoma reagiral dve snovi, se imenuje Točka enakovrednosti.
Kot pri vseh kemičnih metodah analize tudi pri volumetrični analizi obstajajo zahteve za dobre rezultate:
-Kemična reakcija mora biti SelektivnoTo pomeni, da bo standardna raztopina reagirala le z vzorcem.
-Kemična reakcija mora biti Stehiometrična, to je, upoštevajte razmerja, označena v uravnoteženi kemijski enačbi.
-Kemična reakcija mora biti Kvantitativni; se nanaša na 99,9% dokončanost na točki enakovrednosti.
-Mora biti zaznavna končna točka v reakciji, kar bo bolje potrdil kazalnik.
Primarni vzorec
The Primarni vzorci So snovi visoke čistosti, katerih koncentracija v raztopini se izračuna neposredno na podlagi tehtane količine in porabljene količine vode.
A) Da, lahko reagiramo z delujočimi rešitvami, da poznamo koncentracije slednjih in jih pretvorimo v standardne raztopine.
Primeri primarnih vzorcev so:
-Natrijev karbonat (Na2CO3): Uporablja se za standardizacijo kislin, kot je žveplova kislina.
-Kalijev biftalat: Primarni standard je priprava standardnih raztopin baz, kot je natrijev hidroksid.
-Natrijev klorid (NaCl): Uporablja se za standardizacijo raztopin srebrovega nitrata.
-Kalcijev karbonat (CaCO3): Primarni standard za EDTA (etilen diamin tetraocetna kislina).
Primarni vzorec mora izpolnjevati več bistvenih značilnosti:
Mora imeti Visoka čistost, Atmosferska stabilnost, Odsotnost hidracijske vode, Nizki stroški in enostaven dostop, Y Velika ekvivalentna teža.
Klasifikacija volumetrične analize
Glede na vrsto kemikalij, s katerimi sodelujete pri analizi, bo to vrsta volumetrije:
Kislinsko-bazična volumetrija: Deluje bodisi s kislino bodisi z bazo za analizo vzorcev, ki vsebujejo kisline ali baze.
Volumetrija padavin: Imenuje se tudi Argentometrija in s standardno raztopino srebrovega nitrata ugotovi, koliko kloridov je v vzorcu.
Volumetrija kompleksnosti: Za merjenje koncentracije trdote, to je kalcijevih in magnezijevih karbonatov, v vodi se uporablja standardna raztopina kompleksa, kot je EDTA.
Volumetrija REDOX: Reakcija poteka med oksidacijsko snovjo in reducirajočo snovjo.
Kazalniki
Med številnimi kazalniki, uporabljenimi v Volumetrics, izstopajo trije:
1.- Metil oranžna: V alikvotu je oranžno obarvan, ki bo titriran s kislino. Ko je točka enakovrednosti dosežena, indikator zasveti rumeno.
2.- Fenolftalein: Na začetku je prozoren v alikvotu, ki bo naslovljen z osnovo. Ko je točka enakovrednosti dosežena, indikator postane roza.
3.- Eriochrome Black: To je indikator, ki se uporablja za določanje trdote v vodi. Na začetku je v alikvotu vijoličen, dokler ga ne titriramo s kompleksirnim sredstvom. Na koncu reakcije postane modra.

Instrumenti v volumetrični analizi
V volumetrični analizi bo uporabljena vrsta instrumentov, ki jih, če niso na voljo, ni mogoče ustrezno razviti:
1. - Volumetrična bučka: Je posoda, kot je žarnica v spodnjem delu, sploščeno na dnu in ima tanek stolpec, v katerega se doda tekočina. Oznaka označuje, kje naj bo meniskus tekočine, tako da pokrije natančen volumen. Uporablja se za vsebovanje standardnih rešitev; zahvaljujoč natančnosti njegove prostornine je zagotovljena znana koncentracija.

2.- pipete: To so graduirane tanke cevi, ki omogočajo zanesljivo merjenje natančnih količin tekočine. Na voljo so do 25 mililitrov in omogočajo natančno vzorčenje.
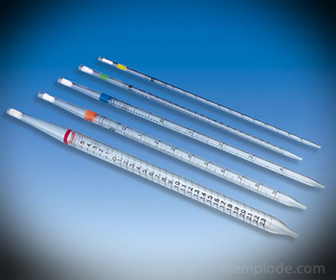
3.- Bireta: To je podolgovata cev s prostornino 50 mililitrov, ki bo vsebovala standardno raztopino. Na enem od njegovih koncev ima ventil za uravnavanje pretoka, ki bo odtekel raztopino v Aliquot.
4. - Erlenmeyerjeve bučke: So posode z ravnim dnom, stožčaste oblike, ki se konča v valjastem robu. Zaradi te zasnove so primerni za kemijske titracije, saj ne dovoljujejo, da bi jih raztresanje prelilo. Za izvedbo ponavljajočih se preskusov bodo potrebni najmanj trije, da se zagotovi zanesljiv rezultat.

Izračuni v volumetrični analizi
Med obdelavo vodnih raztopin sta za volumetrično analizo pomembni koncentraciji in prostornini.
Glavna enačba volumetrije temelji na štirih glavnih podatkih:
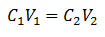
C1= Koncentracija vzorca (neznano)
V1= Prostornina alikvota, s katerim je bila opravljena analiza
C2= Koncentracija standardne raztopine, ki se uporablja za doseganje točke enakovrednosti
V2= Volumen Standardna raztopina, potrebna za konec reakcije
Podatki so nadomeščeni v enačbi, tako da je neznana le iskana koncentracija. Seveda morajo biti vsi podatki na istih pogonih.
Primeri volumetrične analize
Določanje kloridov (Cl-) z argentometrijo s srebrovim nitratom.
Določanje bromidov (Br-) z argentometrijo s srebrovim nitratom.
Določanje cianidov (CN-) z argentometrijo s srebrovim nitratom.
Določanje magnezijevega karbonata (MgCO3), s Kompleksometrijo, z EDTA.
Določanje kalcijevega karbonata (CaCO3), s Kompleksometrijo, z EDTA.
Analiza žveplove kisline (H2SW4) z natrijevim hidroksidom (NaOH).
Analiza natrijevega hidroksida (NaOH) s klorovodikovo kislino (HCl).
Določanje antimona (III) s kalijevim permanganatom (KMnO4).
Določanje arzena (III) s kalijevim permanganatom (KMnO4).
Določanje titana (III) s kalijevim permanganatom (KMnO4).
Določanje molibdena (III) s kalijevim permanganatom (KMnO4).
Določanje železa (II) s kalijevim permanganatom (KMnO4).
Določanje oksalatnega iona s kalijevim permanganatom (KMnO4).