Пример пептидне везе
Хемија / / July 04, 2021
Тхе Пептидна веза је онај у коме два молекула аминокиселина се спајају кондензацијом.
Да би се боље разумеле пептидне везе, прво се морају дефинисати аминокиселине:
Тхе Аминокиселине су органски молекули кратко садржи најмање амино група (-НХ2), алкалне природе, и карбоксилна група (-ЦООХ), киселог карактера.
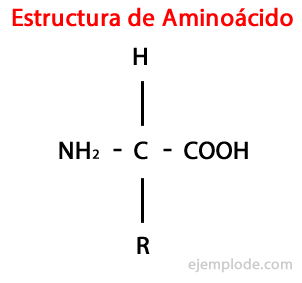
Иако жива бића синтетишу, у различите сврхе, врло разнолике врсте аминокиселина, најважније су оне које су део протеина, који сви припадају класи α-аминокиселине.
За α-аминокиселине је карактеристично да имају киселину и амино групе везане за исти атом угљеника, назван α угљеник. Даље, овај α угљеник веже као трећи супституент атом водоника и као четврти супституент, додатна група различитих величина и карактеристика, која разликује сваку аминокиселину од други.
Четврти супституент се зове Бочни ланац Аминокиселина и често је представљен у поједностављеном облику словом Р.
Како су четири супституента α-угљеника различита и усвајају тетраедарски распоред око себе, присутне су α-аминокиселине
оптичка изомерија, а то је када молекул има алтернативни облик то изгледа као одраз његов, који на крају није једнак молекул. Ова два изомерна облика молекула имају слова Д или Л, у зависности од тога како су супституенти распоређени у простору. Све аминокиселине које се налазе у протеинима су Л.Аминокиселине су класификоване према хемијском карактеру у Полар и Аполар. Полари су пак подељени на Неутрално и наплаћено (која може бити кисела или базична). Тхе Неполарни могу бити алифатски или ароматични.
Пептиди и пептидна веза
Пептиди су производ ковалентне уније аминокиселина кроз амидне везе, формирајући кондензација карбоксилног краја једног и амино краја другог, ослобађање молекула воде у реакција. Овај спој се назива Пептидна веза.
Механизам ове реакције представљен је у наставку, у којем Амино и карбоксилне групе, а долази до кондензације молекула аминокиселине да би се створио пептид.
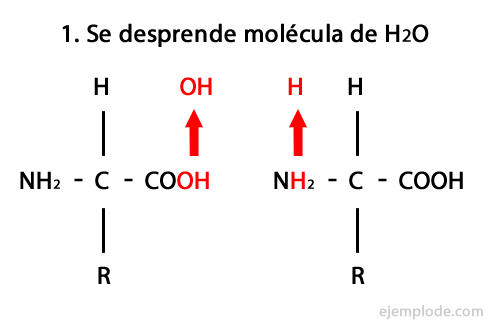
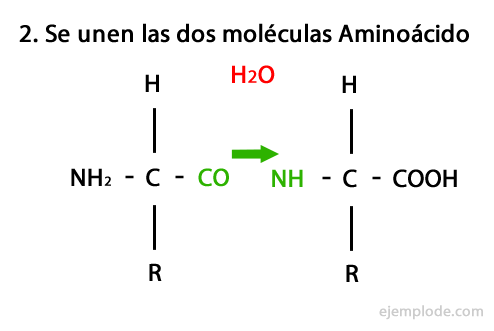

Пептиди, попут аминокиселина и протеина, имају амино групу и карбоксилну групу на својим крајевима а да не реагује.
Да бисте одредили формулу једноставног пептида, па чак и протеина, довољно је навести аминокиселине које га чине, почев од оне са бесплатном Амино групом, а завршава оним са слободном карбоксилном групом.
Неки пептиди који се налазе у телу су Вазопресин, који подиже крвни притисак и повећава реапсорпцију воде у бубрезима; тхе Енкефалин, што смањује осећај бола; и Окситоцин, што доводи до контракције материце.
Карактеристике пептидне везе
Кондензација амино групе једне аминокиселине са карбоксилом друге, одвија се у воденом растварачу, тако да није спонтано, те стога синтеза протеина захтева снабдевање енергијом.
Пептидна веза, као у било којој амидној вези, представља резонанцу између два екстремна облика: неутрални облик, са једноструком везом која спаја карбонилни угљеник прве аминокиселине и амино азот друге (Ц-Н), и облик са одвајањем набоја у којој су два атома повезана двоструком везом (Ц = Н). У стварности, пептидна веза не усваја ниједну од две екстремне ситуације, али је резонантни хибрид обе.
Ево позива Пептид Плане, који се састоји од сви атоми укључени у пептидну везу, који се придружују двема почетним аминокиселинама. С једне стране, атоми азота и водоника, са њиховим угљеником α у првој аминокиселини. С друге стране, угљеник α друге аминокиселине, са кисеоником и угљеником карбонилне групе.
Разлике између пептида и протеина
Тхе пептиди имају мали број аминокиселина, која се креће од два до неколико десетина, и њихова конформација у решењу постаје флексибилна.
Тхе мали протеини, структурно блиски великим пептидима, имају а дефинисане конформације и много мање флексибилне.
Постоје протеини који, попут пептида, имају неуређену и флексибилну конформацију, али такав поредак имају у интеракцији са другим макромолекулима у ћелији.
20 примера аминокиселина које учествују у везивању пептида
- Глицинија
- Девојци
- Валине
- Леуцин
- Изолеуцин
- Пролине
- Метионин
- Фенилаланин
- Тирозин
- Триптофан
- Серине
- Треонин
- Цистеин
- Аспарагин
- Глутамин
- Аспарагинска киселина
- Глутаминска киселина
- Лизин
- Аргинин
- Хистидин

