50 Exempel på syror och baser
Miscellanea / / July 04, 2021
Inom området för kemi, kallas baser (eller hydroxider) till ämnen som, när de är upplösta i vatten, frigör hydroxyljoner (OH–) och kallas syror ämnen som kan frigöra protoner (H+i vattenlösning. Till exempel: svavelsyra, salpetersyra, kalciumhydroxid, kaliumhydroxid.
Klassificering av syror och baser
Enligt deras tendens att dissociera till joner klassificeras syror och baser i:
Syror minskarpH i lösningar, baser eller alkalier höjer den. Starka syror är ofta frätande, vissa ämnen löses bättre i media som har försurats eller alkaliserats något.
Exempel på syror
Några kända syror är:
- Svavelsyra (H2SW4). Det är en stark syra med många användningsområden, särskilt i tung industri, mycket frätande och irriterande. När det späds släpper det ut mycket värme, så det måste hanteras (som andra starka syror) med stor försiktighet. Det oxiderar intensivt.
- Saltsyra (HCl). Även om det är en stark syra, är den närvarande i människokroppen, särskilt i magen, där den spelar en viktig roll i matsmältningsprocessen. Dess överskott genererar halsbränna.
- Fosforsyra (H3PO4). Denna syra är en vanlig ingrediens i kolsyrade drycker. Regelbunden konsumtion av sådana drycker avskräcks på grund av denna syras negativa inverkan på kalciummetabolismen, vilket påverkar ben och tänder särskilt.
- Salpetersyra (HNO3). Det är en erkänd stark syra, som bland annat används för att tillverka sprängämnen och kvävegödselmedel.
- Perklorsyra (HClO4). Det är en stark syra, flytande a temperatur miljö. Det är en av de mest oxiderande.
- Vätesulfid (H2S). Det är ett gasformigt ämne med en stark och obehaglig lukt, giftig i höga koncentrationer. Den har många industriella applikationer.
- Ribonukleinsyra. Det är en central komponent i ribosomer, som är nödvändig för att den globala processen för proteinsyntes ska kunna fullbordas från deoxiribonukleinsyra.
- Acetylsalicylsyra. Det är en mycket viktig organisk syra, med smärtstillande och antiinflammatoriska egenskaper. Det är basen för aspirin.
- Mjölksyra. Det kommer från nedbrytningen av glukos under anaerob träning med hög intensitet och kort varaktighet. Under normala förhållanden återanvänds denna mjölksyra, men om den ackumuleras orsakar den skador på muskelfibrerna, vilket framför allt orsakar kramper.
- Allylsyra. Det är en syra som finns i grönsaker såsom vitlök eller lök, härledd från en föregångare som också finns i sådana arter, allicin. Det är bakteriedödande och antioxidant.
- Retinsyra. Appliceras topiskt, det hämmar keratinisering, används i krämer mot akne och hudåldring. Det ska användas under medicinsk övervakning.
- Smörsyra. Det är slutprodukten av jäsning av vissa kolhydrater som utförs av mikroorganismer av vommen. Det är vanligtvis en del av fett djur i små mängder.
- Propionsyra. Det är ett konserveringsmedel för livsmedel, det används för att förhindra svamp och bakteriell förstörelse av bageriprodukter och andra.
- Bensoesyra. Det används som konserveringsmedel tillsatt till olika produkter (majonnäs, konserver), ofta i form av salt (natriumbensoat).
- Ättiksyra (CH3COOH). Det är ett konserveringsmedel som ofta används i hemmet, även som bas för vinägretter och pickles. Det är huvudkomponenten i vinäger.
- Hydrojodsyra (HI(ac)). Det är en stark syra som kan användas för att öka nivåerna av jod i du går ut.
- Bärnstenssyra (C4H6ELLER4). Det är ett kristallint fast ämne som kan erhållas från bärnsten. Det kan genereras i jäsningsprocessen av vin och öl.
- Bromvätesyra (HBr(ac)). Det är en mycket frätande stark syra. Dess reaktion med baser är väldigt våldsam, den är också mycket irriterande. Det används i den kemiska och läkemedelsindustrin.
- Citronsyra (C6H8ELLER7) Det är en organisk syra som är rik på frukt. Det är en naturlig antioxidant.
- Oxalsyra (H2C2ELLER4). Det är en organisk syra som finns naturligt i växter. Det används vid biodling för att kontrollera sjukdomar i bin. Det används också för att tillverka rengöringsprodukter, bland annat inom textilindustrin.
Exempel på baser
Metallbasar är allmänt kända som hydroxider. Några baser är:
- Natriumhydroxid (NaOH, kaustiksoda). Det är en stark bas som används i pappersindustrin och vid tillverkning av tvättmedel. I vardagen används den för att rensa badrums- och köksrör.
- Magnesiumhydroxid (Mg (OH))2, mjölk av magnesia). Det är en stark bas som ibland används som antacida eller laxermedel.
- Kalcium hydroxid (Ca (OH)2, lime). Även känd som hydratiserad kalk, används den i metallurgi och oljeindustrin. Det används också för att göra bekämpningsmedel, bland annat inom socker och mejeri.
- Kaliumhydroxid (KOH). Det är en stark och frätande bas som används ofta i olika branscher. Det används ofta för att göra tvål.
- Bariumhydroxid (Ba (OH)2). På grund av dess toxicitet används den för att göra gifter. Det används också i keramikindustrin, i pappersindustrin och i processen för raffinering av socker.
- Järn II eller III hydroxid (Fe (OH)2 eller Fe (OH)3). Det genereras vanligtvis som en del av den metallurgiska industrin. Det används vid tillverkning av färger bland andra användningsområden.
- Ammoniak (NH3). Det är en gas med en karakteristisk lukt. Det används för att tillverka gödselmedel och många droger. Det är mycket farligt vid inandning i höga doser.
- Tvål. Det är ett natrium- eller kaliumsalt. Det används för personlig och allmän hygien.
- Rengöringsmedel. Det är också en mycket använd produkt för hygien.
- Kinin. Det är en naturlig bas som produceras av vissa växter. Det har febernedsättande och smärtstillande egenskaper. I antiken användes den för att behandla malaria.
- Anilin. Det är en giftig förening vid intag eller inandning. Det används i gummiindustrin, bland annat vid tillverkning av herbicider och sprängämnen.
- Guanine. Det är en av de kvävehaltiga baserna som ingår i nukleinsyror (DNA och RNA).
- Pyrimidin. De kvävehaltiga baserna som utgör nukleinsyror härrör från pyrimidin.
- Cytosin. Det är en av de kvävehaltiga baserna som ingår i nukleinsyror.
- Adenine. Det är en av de kvävebaser som ingår i nukleinsyror.
- Zinkhydroxid (Zn (OH)2). Det är en amfotär substans (den kan fungera både som en syra och som en bas). Det är ett giftigt ämne om det kommer i kontakt med ögonen eller huden. Det används i tillverkningsprocessen för kirurgiska förband.
- Kopparhydroxid (Cu (OH)2). Det används som ett fungicid och för att färglägga keramiska föremål. Det används också som katalysator för vissa kemiska reaktioner.
- Zirkoniumhydroxid IV (Zr (OH))4). Det används inom keramik- och glasindustrin.
- Berylliumhydroxid (Be (OH))2). Det har amfotära egenskaper. Det används i industrin för att erhålla metallisk beryllium. Det är ett ämne med begränsat överflöd.
- Aluminiumhydroxid (Al (OH)3antacida). Det används i medicin som ett antacida och adjuvans mot vacciner.
Teorier om syror och baser
Begreppet baser och syror har förändrats över tiden. Det var Arrhenius som tog fram den första definitionen, som definierar en syra som ett ämne som ger H-joner i vattenlösning+och till en bas såsom ett ämne som i vattenlösning ger upp OH-joner–. Hans teori hade vissa begränsningar, eftersom vissa ämnen (som ammoniak) beter sig som baser utan att ha i sig molekyl till hydroxyljonen.
Dessutom ansåg Arrhenius endast ämnen i vattenhaltiga medier, men syrabasreaktioner förekommer också i andra medier. upplösning inte vattenhaltig. En representation av en syra och en bas enligt Arrhenius-teorin är:
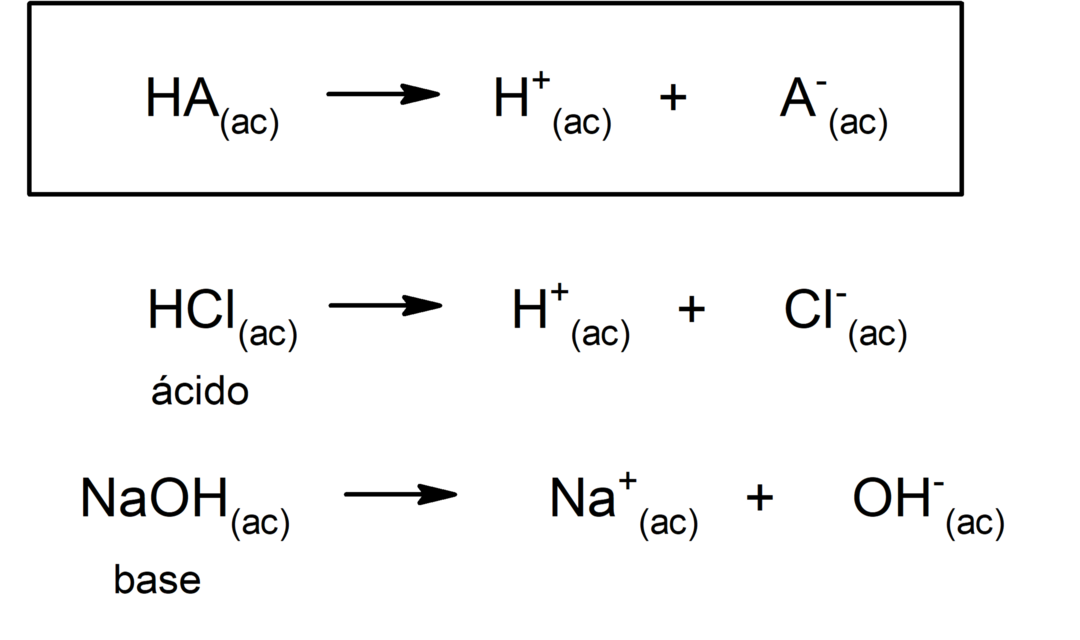
Nästan fyrtio år senare, omkring 1923, formulerade Brönsted och Lowry en annan teori genom att säga att syror och baser fungerar som konjugerade par. Enligt denna teori är syran den substans som kan ge upp protoner (i detta fall hänvisar den inte till atomkärnans protoner utan till katjonerna H+, är H+ en förkortning för katjon H3ELLER+) och basen är den substans som kan acceptera dessa protoner.
Denna teori säger att i en syrabasreaktion är en konjugatbas den kemiska arten som bildas efter en syra donerar en proton, och en konjugerad syra är den kemiska art som bildas efter att basen accepterar en proton. Denna teori är inte helt komplett, eftersom det finns flera ämnen som har sura egenskaper utan att ha atomer vätejoniserbar i sin struktur.
Men å andra sidan är det i denna teori inte obligatoriskt att ämnena finns i vattenlösning. En representation av en syra (och dess konjugatbas) och en bas (och dess konjugatsyra) enligt Brönsted - Lowry-teorin är protonationen av ammoniak, som inte behöver förekomma i vattenhaltigt medium:
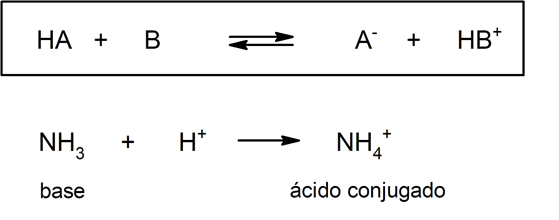
Därför, som en ytterligare del av hans teori om kovalent bindning, Lewis utvecklade en teori där han definierar en syra som allt detta ämne som kan acceptera ett par elektroner, medan en bas är vilken substans som helst som kan ge upp det elektroniska paret.
Enligt Lewisbegreppen syra och bas involverar inte vinst eller förlust av OH-joner– och H+Istället föreslår det att H + själv är syran (den kan acceptera elektroner) och OH- är basen (den kan donera elektroner). En representation av en syrabasreaktion enligt Lewis-teorin är:

Där OH- (som tillhör NaOH) donerar det odelade elektronparet till H + (som tillhör HCl), som ett resultat koordinat- eller dativlänk (kovalent bindning i vilken det delade elektronparet bidrar med endast en av de atomer som är involverade i bindningen) för att bilda vattenmolekylen.