Definition av molekylär geometri
Miscellanea / / January 11, 2022
Begreppsmässig definition
Det är strukturen hos en molekyl som bestämmer det tredimensionella arrangemanget av atomerna som utgör den i rymden.

Kemi ingenjör
Molekylära geometrier definieras för närvarande baserat på Teori of Repulsion of Electronic Pairs of the Valencia Layer (TRPECV). Denna teori gör det möjligt att förutsäga beteendet kemisk av ämnen (särskilt kovalenta) och hjälper till att förstå distribution elektronik, vilket leder till geometri av molekyl. Detta i sin tur gör att vi kan förstå många av de egenskaper som ämnen förvärvar.
Denna teori är baserad på en rad grundläggande pelare som vi kommer att granska och sedan försöka förstå deras Ansökan öva. För det första betraktas bundna och obundna (valens) elektroner som ett hav av elektroner som, genom har samma typ av laddning stöter de bort varandra, så de kommer alltid att vara placerade så långt bort från den centrala atomen i molekyl.
För det andra bildar detta "hav" av elektroner eller "elektroniska moln" områden med hög elektrondensitet, som är uppbyggda i bindningar, där elektronerna är delade eller i par av elektroner som inte delas. I sin tur kan bindningarna som bildas vara enkla, dubbla eller till och med trippel.
Slutligen för besluta molekylär geometri, är det mycket användbart att ha Lewis-strukturen, där mängden elektrondensiteter runt den centrala atomen kommer att räknas och detta kommer att ge indikation från namnet på dess geometri och formen som molekylen tar tredimensionellt.
Det bör noteras att dessa tätheter kommer att placeras så långt ifrån varandra som möjligt, för att anta den mest stabila strukturen och där det finns mindre repulsion. Så här identifieras först den elektroniska geometrin och sedan den molekylära geometrin.
Sex nivåer av densitet
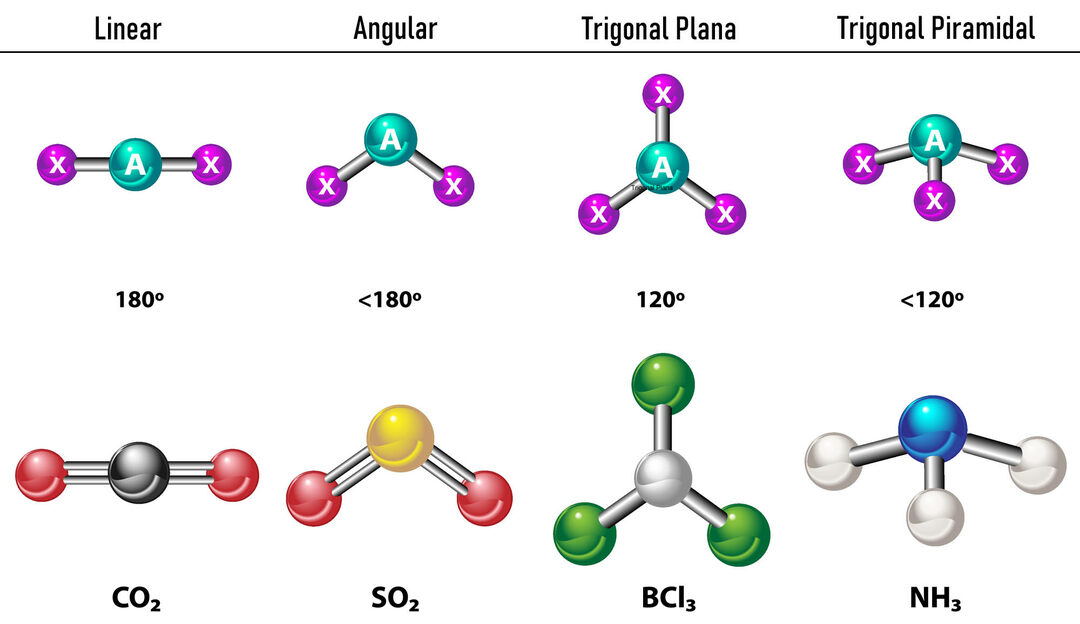
Om det finns två elektrondensiteter runt den centrala atomen, kommer bindningarna att ligga så långt ifrån varandra mellan dem, det vill säga 180º från varandra och därför är deras elektroniska geometri linjär och molekylärt är den också linjär.
I fallet att det finns tre elektrondensiteter runt den centrala atomen, finns det två alternativ: tre bindningar eller två bindningar och ett obundet par. Om det finns tre bindningar är den elektroniska geometrin det Trigonal platt, med 120º vinklar mellan bindningar och molekylär geometri tar samma namn. Nu, om det finns ett obundet par, stöter de bort varandra med mer intensitet att bundna laddningar därför tenderar att komprimera bindningsvinklar. Vinkeln mellan det fria paret och varje bindning är 120º och den elektroniska geometrin är Trigonal Plane medan den molekylära geometrin är Angular.
I det fall det finns fyra elektrondensiteter runt den centrala atomen är den elektroniska geometrin tetraedrisk. Om alla fyra elektronpar är bundna sammanfaller deras molekylära geometri i namn med deras elektroniska geometri och bindningsvinkeln är 109,5º. Nu, om ett av paren är fritt, blir bindningsvinkeln mindre (107º) och molekylgeometrin är typ Trigonal pyramid. Slutligen, om två är fria par och två är bundna, är bindningsvinkeln 104,5º medan molekylgeometrin kallas Vinkel.
När elektrontätheten runt den centrala atomen uppgår till fem kallas det a Trigonal bipyramid dess elektroniska geometri. Om alla laster är sammanlänkade, finns det vinklar på 120ºC mellan de ekvatorialt placerade länkarna och 90º mellan de axiella med de ekviatoriska. Nu kallas molekylär geometri också Trigonal Bipyramid medan, med fyra länkade par och ett fritt par, är den molekylära geometrin förvrängd och bildar den välkända "rocker”, Där är namnet den får Förvrängd tetraeder. Om två av de fem elektronparen är fria och tre av dem är bundna, har den en "T"-formad geometri och dess namn beror just på dess struktur. Slutligen, om det är omvänt, tre fria par och två bundna laddningar, är molekylgeometrin linjär.
Slutligen finns det sex elektrondensiteter runt den centrala atomen och en oktaeder bildas, därav dess namn i elektronisk geometri. På liknande sätt namnges molekylgeometrin om alla dess par är länkade. Om du har fem länkade par och ett fritt par, är molekylgeometrin Square Base Pyramid. Om du har fyra bundna par och två fria par, är molekylgeometrin Fyrkantig lägenhet.
Figur: Sweet Nature
Ämnen i molekylär geometri