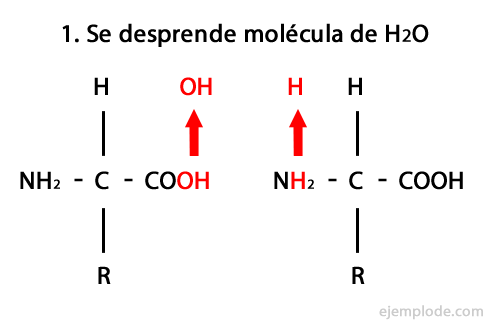
30 Exempel på alkoholer
Exempel / / November 06, 2023
De alkoholer är organiska kemiska föreningar som i sin struktur innehåller den funktionella hydroxylgruppen (-OH) bunden till ett kol (- C). Gruppen (- C – OH) kallas "karbinol". Några exempel på alkoholer är: metanol, etanol och 1-propanol.
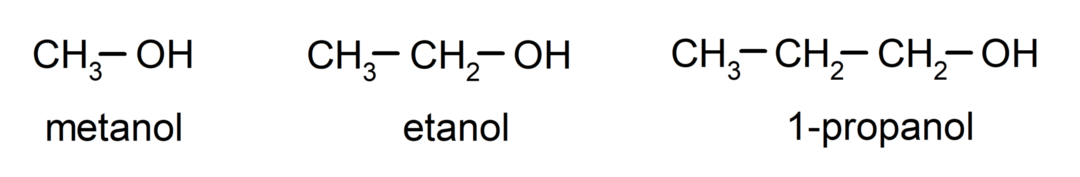
Alkoholer är kemiska föreningar med olika användningsområden i vardagen, eftersom de har antibakteriella och antiseptiska egenskaper. Å andra sidan kan de vara farliga för människors hälsa när de intas okontrollerat.
Likaså kan inte alla alkoholer intas av människor.
- Se även: Aminer och ketoner
Typer av alkoholer
Beroende på antalet kolatomer till vilka kolatomen som har hydroxylgruppen bunden är fäst, kan en alkohol vara:
- Primär alkohol. Kolatomen som har hydroxylgruppen fäst är också bunden till en enda kolatom. Till exempel:
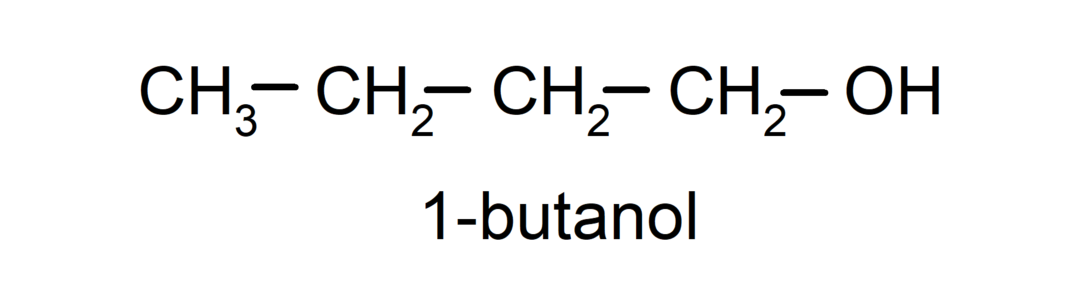
- Sekundär alkohol. Kolatomen som har hydroxylgruppen fäst är också bunden till två andra kolatomer. Till exempel:
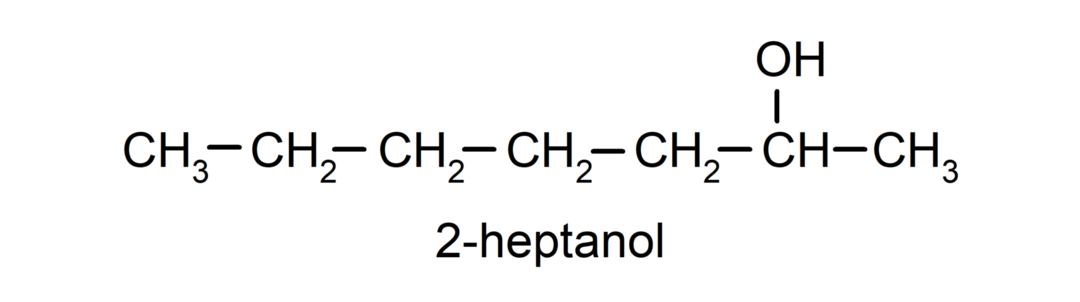
- Tertiär alkohol. Kolatomen som har hydroxylgruppen fäst är också bunden till tre kolatomer. Till exempel:
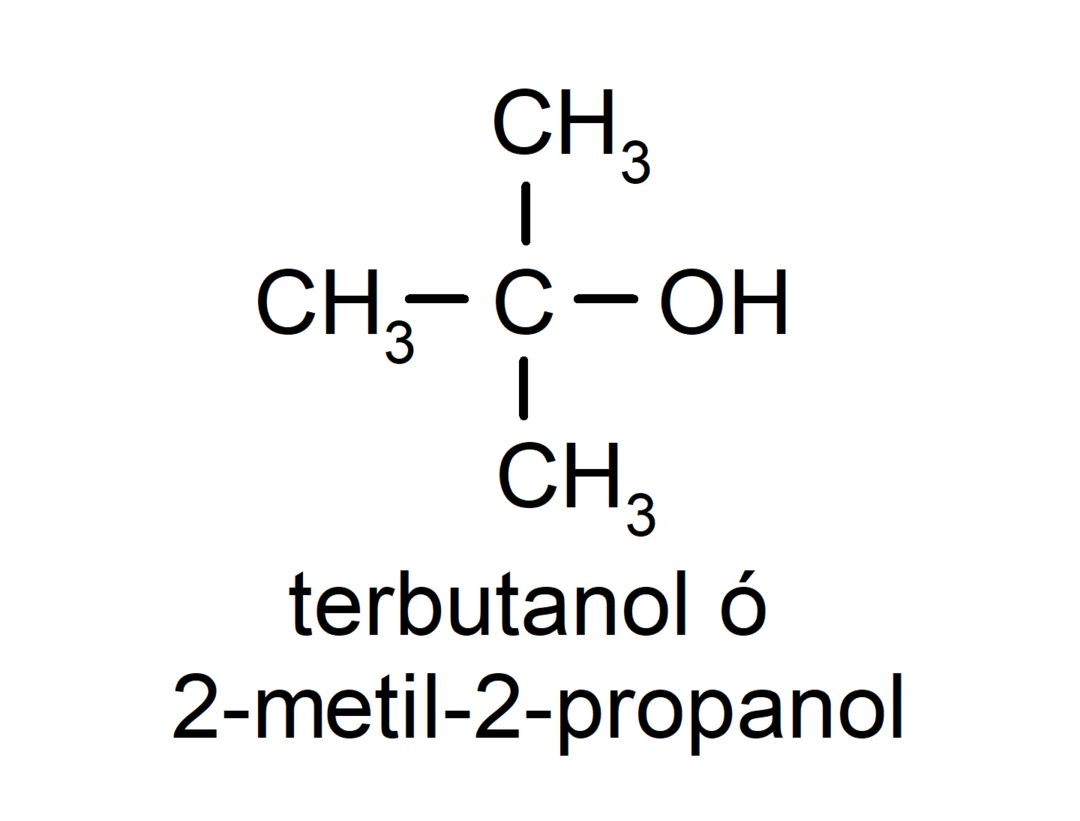
Beroende på antalet hydroxylgrupper den har, kan en alkohol vara:
- Diol. Den har två hydroxylgrupper i sin struktur. Till exempel:
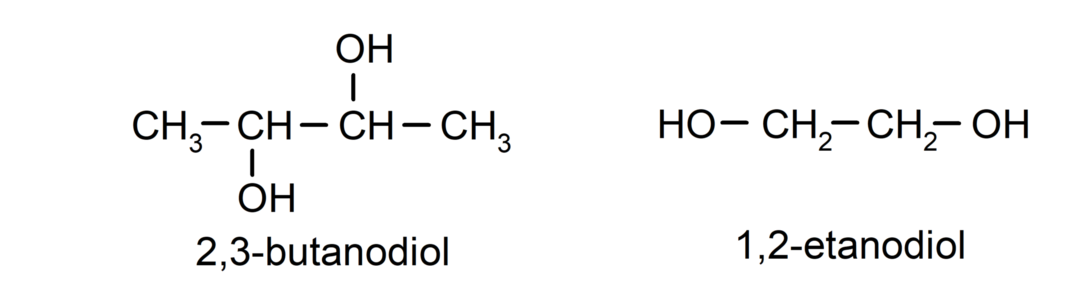
- Triol. Den har tre hydroxylgrupper i sin struktur. Till exempel:
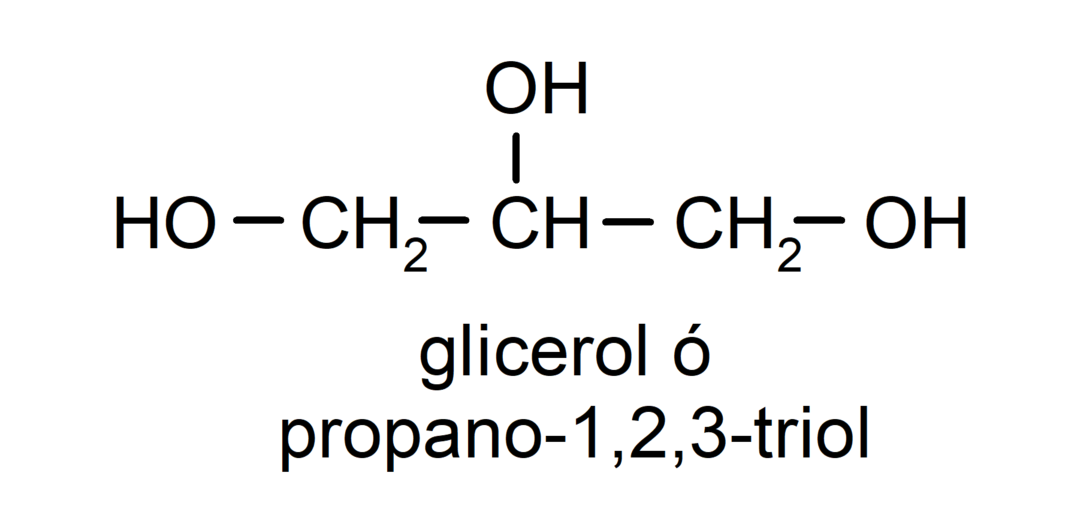
- Polyalkohol. Den har många hydroxylgrupper i sin struktur. Till exempel:
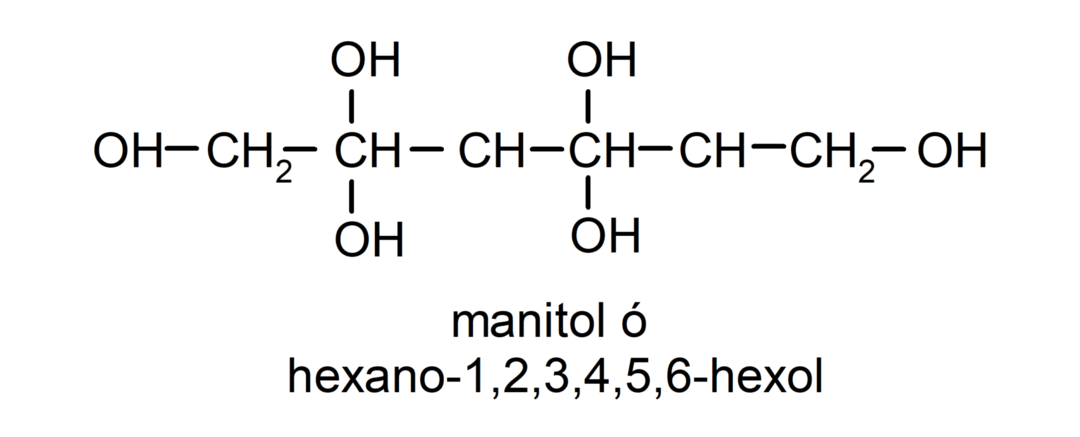
Fysikaliska egenskaper hos alkoholer
Några av de fysiska egenskaperna hos alkoholer är:
- Kokpunkt. Kokpunkten i alkoholer är ganska hög på grund av närvaron av hydroxylgruppen, vilket möjliggör bildandet av vätebindningar. Dessutom, ju fler hydroxylfunktionella grupper som finns i kolkedjan, desto högre är Kokpunkt av alkoholer.
- Polaritet. Alkoholer är ganska polära föreningar.
- Löslighet. Alkoholer med låg molekylvikt är lösliga i vatten. Å andra sidan, ju större kolkedjan av alkoholer är, desto lägre är deras löslighet i vatten. Dessutom, ju fler hydroxylgrupper alkoholer har, desto större är deras löslighet i vatten.
- Aggregeringstillstånd. De flesta alkoholer är flytande vid rumstemperatur (25ºC) och har karakteristiska lukter.
Kemiska egenskaper hos alkoholer
Några av de kemiska egenskaperna hos alkoholer är:
- Alkoholer beter sig som syror och baser.. Deras beteende som syror kan ses i reaktioner med aktiva metaller för att frigöra vätgas och bilda alkoxider.

Deras beteende som baser kan ses i reaktioner som reaktionen av metanol med vätebromid för att bilda metyloxoniumbromid.
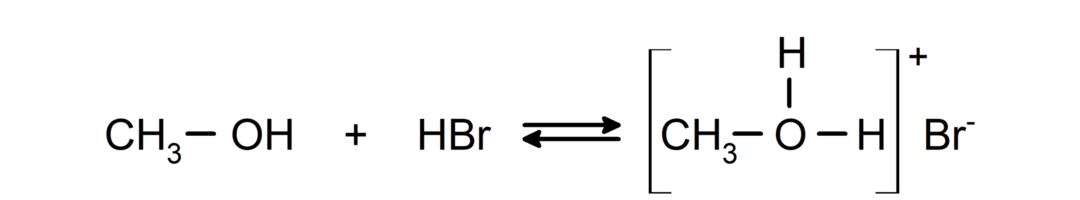
- Alkoholer genomgår halogeneringsreaktioner. De reagerar med vätehalogenider för att bilda alkylhalider.
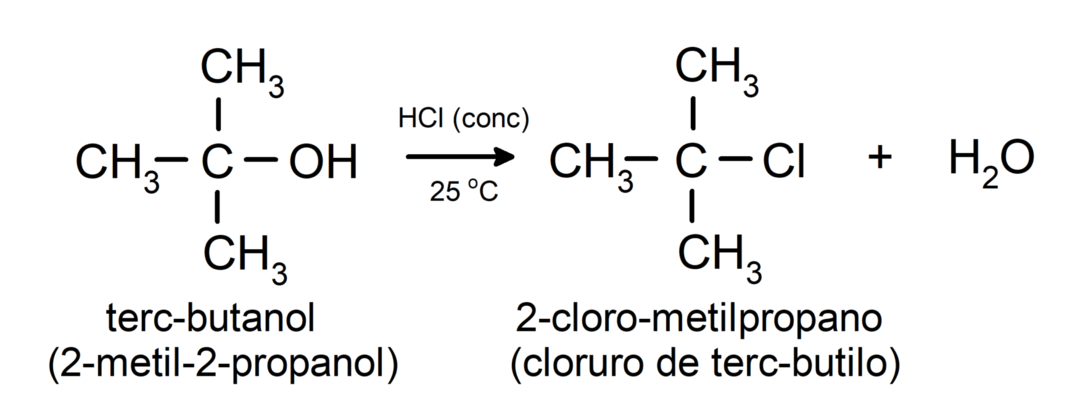
-
Alkoholer genomgår oxidationsreaktioner när de reagerar med vissa oxiderande föreningar. Produkterna av oxidationsreaktioner beror på vilken typ av alkohol som reagerar, det vill säga om den är primär, sekundär eller tertiär.
Oxidation av primär alkohol för att bilda aldehyd eller karboxylsyra.
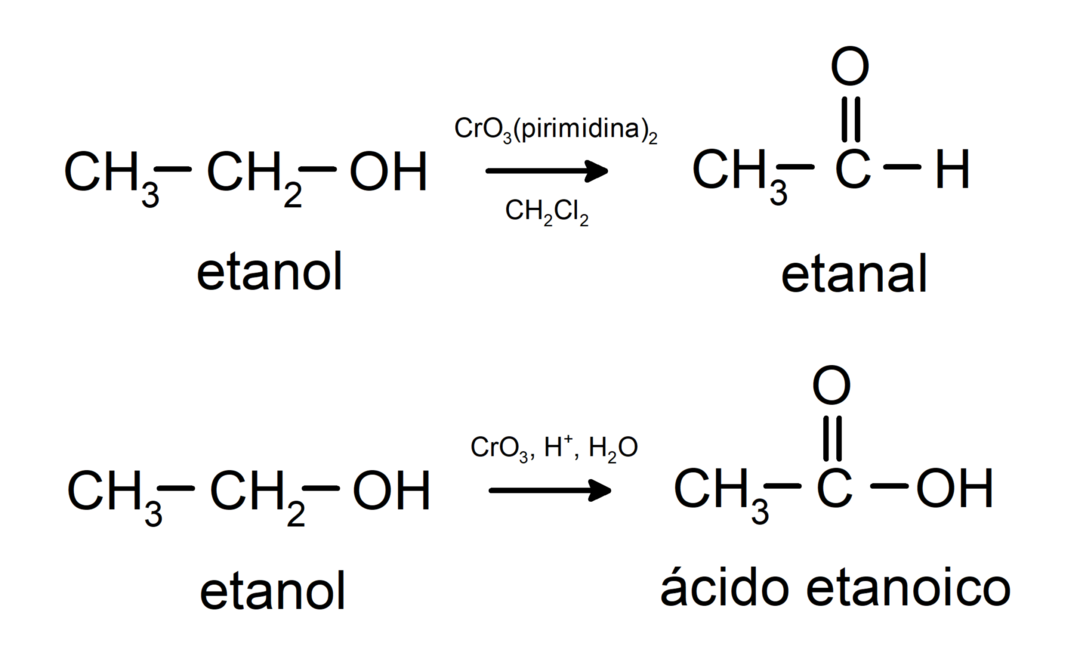
Oxidation av sekundär alkohol för att bilda keton.
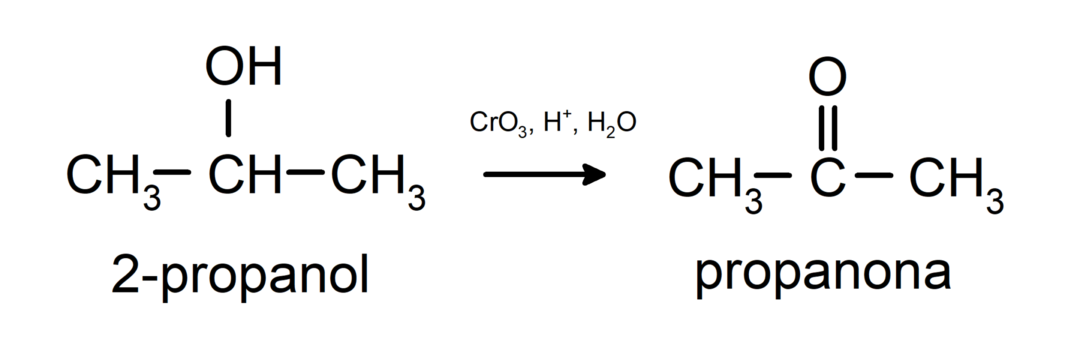
Tertiära alkoholer oxiderar inte med vanliga oxidanter. Med mycket starka oxidationsmedel kan de omvandlas till alkener, som sedan kan oxideras.
Alkoholer som har två hydroxylgrupper på intilliggande kol oxideras med blytetraacetat för att bilda två ketoner.
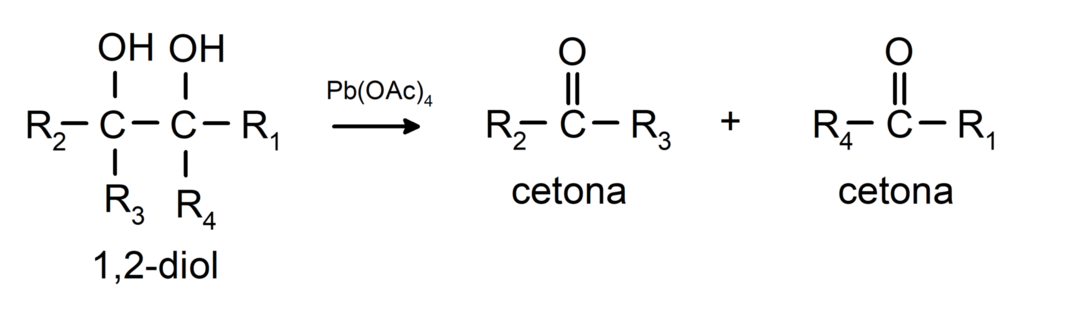
- Alkoholer genomgår dehydreringsreaktioner. Dessa reaktioner inträffar endast med primära och sekundära alkoholer, som när de utsätts för höga temperaturer i närvaro av katalysatorer frigör väte.
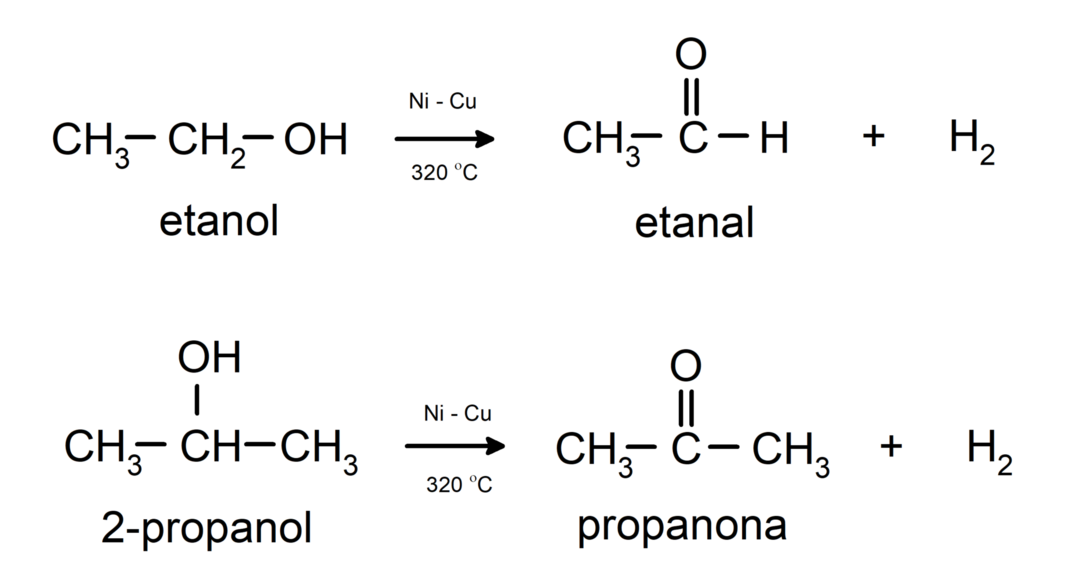
- Alkoholer genomgår uttorkningsreaktioner. Alkoholer dehydrerar för att bilda motsvarande alkener. Denna reaktion sker i närvaro av sura och mellanliggande temperaturer.
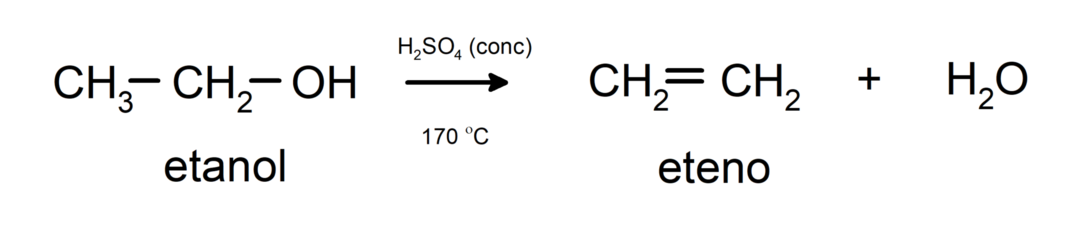
Alkoholnomenklatur
Enligt nomenklaturen som fastställts av IUPAC (International Union of Pure and Applied Chemistry) namnges alkoholer enligt följande regler:
- Hydroxylgruppens position väljs med hänsyn till att den upptar lägsta möjliga antal i kolkedjan. Om alkoholens struktur är cyklisk, beaktas 1-positionen på kolet som har hydroxylgruppen fäst och prefixet cyklo- används för att namnge det.
- Namnet på alkoholen skrivs med hjälp av prefix som anger antalet atomer i kolkedjan, och dessutom placeras suffixet -ol.
- Om alkoholens struktur har grenar väljs den längsta kedjan som också innehåller hydroxylgruppen som huvudkolkedja.
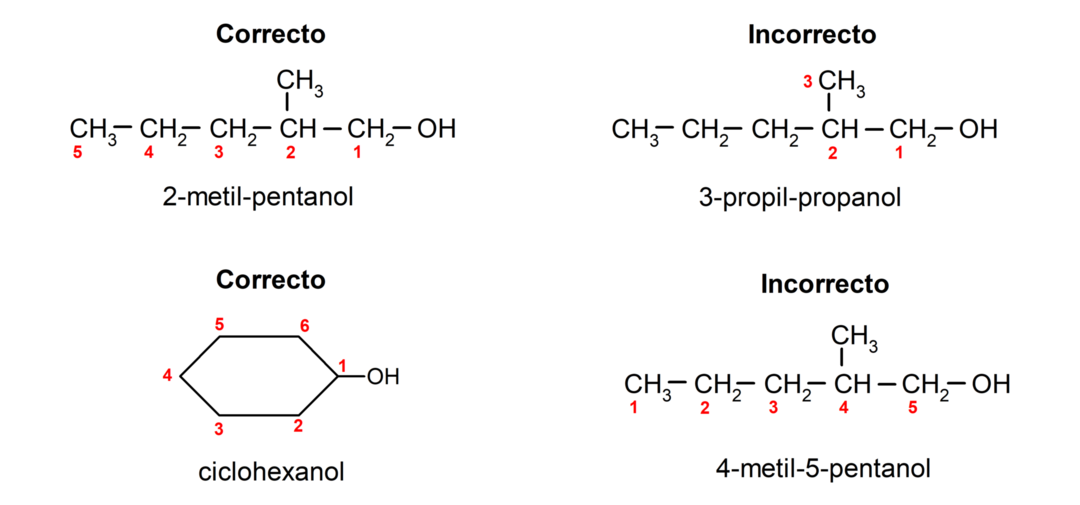
Enligt traditionell nomenklatur namnges alkoholer genom att skriva ordet "alkohol" och sedan skriva namnet på alkoholen. alkan som motsvarar kolkedjan, men istället för att använda -an-änden av alkanen, ändelsen -yllisk.
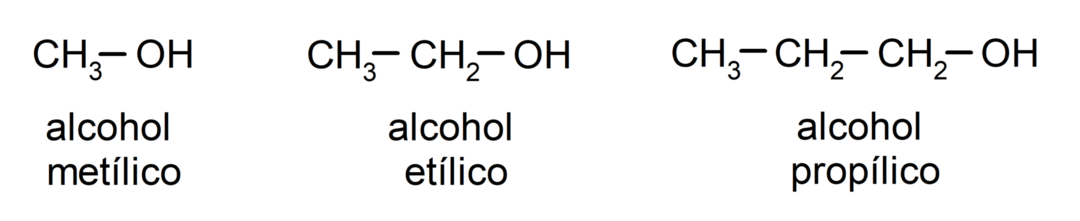
Exempel på alkoholer
- metanol
- etanol
- 1-propanol
- 2-propanol
- 1-butanol
- 3-etylhexan-2-ol
- glycerol
- fenol
- 2-metyl-2-butanol
- 1,2-etandiol
- 1,5-heptadien-3-ol
- 3-metyl-2-butanol
- bensylmetanol
- 3-pentanol
- 2-metylfenol
- 1,2-dihydroxifenol
- cykloheaxnol
- 1-fenyletanol


Användning av alkoholer
De vanligaste användningsområdena för alkoholer är:
- De används som desinfektionsmedel och antiseptika eftersom de stoppar tillväxten av vissa mikroorganismer eller förstöra dem. Etanol och isopropylalkohol är de mest använda för detta ändamål.
- De används i syntesen av olika kemiska föreningar. Metanol används till exempel för att erhålla metanal (formaldehyd).
- De används för att tillverka frostskyddsmedel. Metanol är en av de mest använda för detta ändamål.
- De används som lösningsmedel inom läkemedelsindustrin. Etanol är en av de mest använda i denna mening.
- De används som lösningsmedel för lacker, färgämnen och bläck. Metanol används i stor utsträckning för detta ändamål.
- De används som bränsle och det finns en viktig tendens att delvis ersätta användningen av fossila bränslen genom användning av bioetanolbränsle.
- De används för att göra hartser. Fenol används i denna mening.
Faror med alkoholkonsumtion
Även om alkoholkonsumtion är socialt accepterad idag, skapar missbruk av detta ämne beroende och beroende.
Etanol är alkoholen som finns i alkoholhaltiga drycker, som när den konsumeras i överskott påverkar kognitiva förmågor, och kan orsaka hjärt-kärlsjukdomar, levercirros och cancer.
Dessutom, när graden av alkoholförgiftning uppnås, det vill säga ett tillstånd av berusning, om dosen av alkoholen är för hög kan en alkoholiserad koma uppstå, vilket kan leda till andningsförlamning och till och med dödsfall. död.
Referenser
- T. TILL. Geissman. (1974) "Principles of Organic Chemistry" Andra upplagan. Redaktionell Reverté, S.A. ISBN: 8429171800
- Ahumada-Cortez, J. G., Gámez-Medina, M. E., & Valdez-Montero, C. (2017). Alkoholkonsumtion som ett folkhälsoproblem. Ra Ximhai, 13(2), 13-24.
- Morrison, R. T. & Boyd, R. N. (1998). Organisk kemi. Pearson utbildning.
- Weininger, S. J. & Stermitz, F. R. (1988). Organisk kemi. Jag backade.
Följ med:
- Etanol
- Bränsle
- organisk kemi