50 ตัวอย่างของอัลดีไฮด์และคีโตน
ตัวอย่าง / / November 06, 2023
ที่ อัลดีไฮด์ เป็น สารประกอบอินทรีย์ ที่มีโครงสร้างเป็นหมู่ฟังก์ชันคาร์บอนิล (= C = O) ซึ่งเชื่อมโยงกับโซ่คาร์บอนและอะตอมไฮโดรเจน ตัวอย่างเช่น: เมทานอล (เรียกอีกอย่างว่าฟอร์มาลดีไฮด์), เอทานอล (เรียกอีกอย่างว่าอะซีตัลดีไฮด์) และโพรพานัล (เรียกอีกอย่างว่าโพรพัลดีไฮด์)
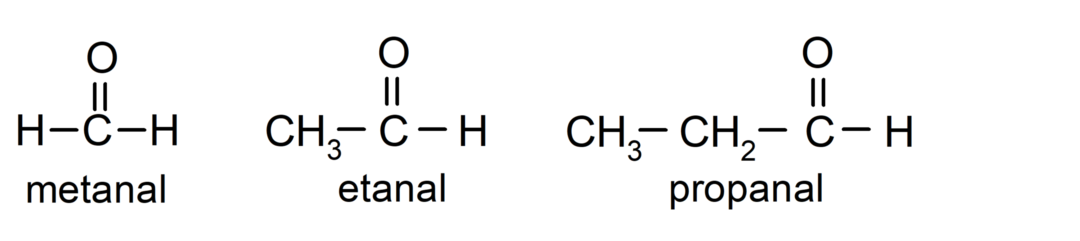
ที่ คีโตน เป็นสารประกอบอินทรีย์ที่มีกลุ่มคาร์บอนิลในโครงสร้างเชื่อมโยงกับอะตอมคาร์บอนสองอะตอม ตัวอย่างเช่น: โพรพาโนน (เรียกอีกอย่างว่าอะซิโตน) บิวทาโนน และ 2-เพนตาโนน
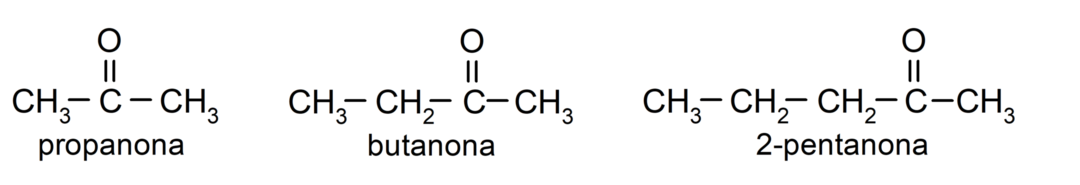
ความแตกต่างระหว่างอัลดีไฮด์และคีโตน
ความแตกต่างที่สำคัญระหว่างอัลดีไฮด์และคีโตนคือ:
- อัลดีไฮด์มีหมู่ฟังก์ชันคาร์บอนิลในโครงสร้างซึ่งอยู่ที่ปลายขั้วด้านหนึ่ง ในขณะที่คีโตนมีหมู่คาร์บอนิลอยู่ในตำแหน่งที่ไม่ใช่ขั้วของมัน โครงสร้าง.
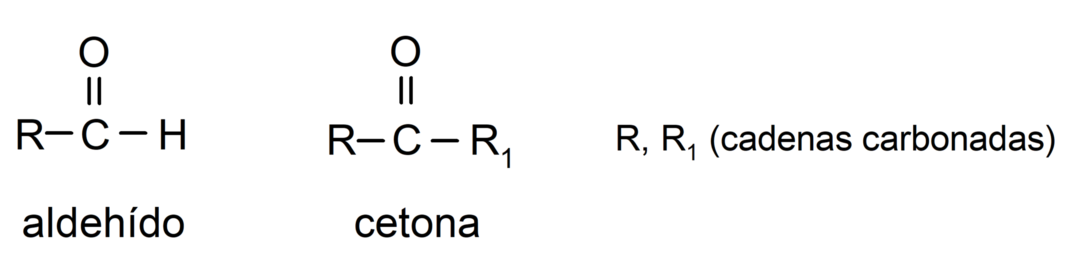
- อัลดีไฮด์จะถูกออกซิไดซ์โดยปฏิกิริยากับรีเอเจนต์ของโทลเลนทำให้เกิดเป็นโลหะเงิน พวกมันยังออกซิไดซ์กับรีเอเจนต์ของเบเนดิกต์ด้วย เกิดเป็นคิวรัสออกไซด์ คีโตนไม่ถูกออกซิไดซ์โดยรีเอเจนต์ตัวใดตัวหนึ่ง
- อัลดีไฮด์จะถูกรีดิวซ์เป็นแอลกอฮอล์ปฐมภูมิ ในขณะที่คีโตนจะถูกรีดิวซ์เป็นแอลกอฮอล์ทุติยภูมิ
คุณสมบัติทางกายภาพ
คุณสมบัติทางกายภาพของอัลดีไฮด์
คุณสมบัติทางกายภาพของอัลดีไฮด์มีความหลากหลายมากเนื่องจากขึ้นอยู่กับโครงสร้างของโซ่คาร์บอนที่เชื่อมโยงกับหมู่คาร์บอนิล
บางสิ่งเป็น:
- อัลดีไฮด์ที่ละลายน้ำได้มากที่สุดคืออัลดีไฮด์ที่มีขนาดเล็กกว่า เช่น มีธานอลและเอทานอล
- อัลดีไฮด์ระเหยมีกลิ่นฉุนและระคายเคืองได้
- หมู่คาร์บอนิลทำให้เกิดขั้ว
- มักจะมีจุดเดือดสูงกว่าสารประกอบเคมีที่มีขนาดโมเลกุลใกล้เคียงกัน
คุณสมบัติทางกายภาพของคีโตน
คุณสมบัติทางกายภาพของคีโตนขึ้นอยู่กับว่าห่วงโซ่คาร์บอนที่เชื่อมโยงกับกลุ่มคาร์บอนิลเกิดขึ้นได้อย่างไร
- คีโตนหลายชนิดมีกลิ่นที่น่าพึงพอใจ
- ความสามารถในการละลายในน้ำขึ้นอยู่กับขนาดของโซ่คาร์บอนที่ติดอยู่กับหมู่คาร์บอนิล ยิ่งโซ่คาร์บอนมีขนาดเล็ก คีโตนก็จะละลายในน้ำได้มากขึ้นเท่านั้น
- หมู่คาร์บอนิลทำให้เกิดขั้วที่ชัดเจน
- มีจุดเดือดค่อนข้างสูงเมื่อเปรียบเทียบกับสารประกอบเคมีที่มีขนาดโมเลกุลใกล้เคียงกัน
คุณสมบัติทางเคมี
คุณสมบัติทางเคมีของอัลดีไฮด์
ในบรรดาคุณสมบัติทางเคมีของอัลดีไฮด์เราสามารถพบ:
พวกมันถูกออกซิไดซ์เพื่อสร้างกรดคาร์บอกซิลิกที่สอดคล้องกันกล่าวคือกรดที่เกิดขึ้นจะมีจำนวนคาร์บอนในห่วงโซ่คาร์บอนเท่ากันกับ อัลดีไฮด์ ที่ทำให้เกิดสิ่งนั้นขึ้นมา ตัวอย่างเช่น:
- ออกซิเดชันด้วยรีเอเจนต์โทลเลน (คอมเพล็กซ์ซิลเวอร์แอมโมเนียในสารละลายพื้นฐาน [Ag (NH3)2]+) จากเอทานอลทำให้เกิดกรดเอทาโนอิกและเงินโลหะ
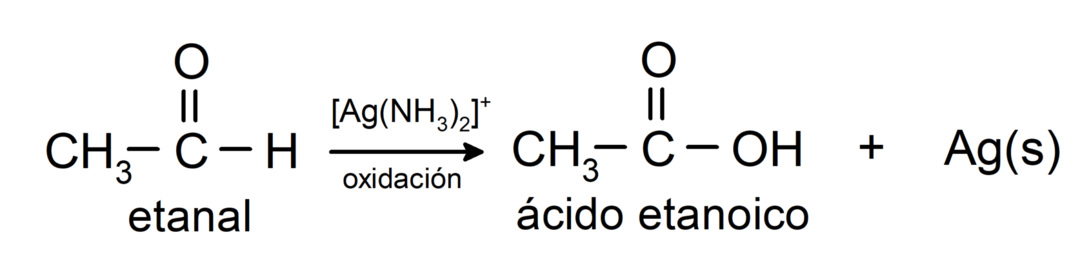
- ออกซิเดชันด้วยรีเอเจนต์ของเบเนดิกต์ (สารละลายอัลคาไลน์ของคอปเปอร์ซัลเฟต) ของเอทานอลทำให้เกิดกรดเอทาโนอิกและคิวรัสออกไซด์
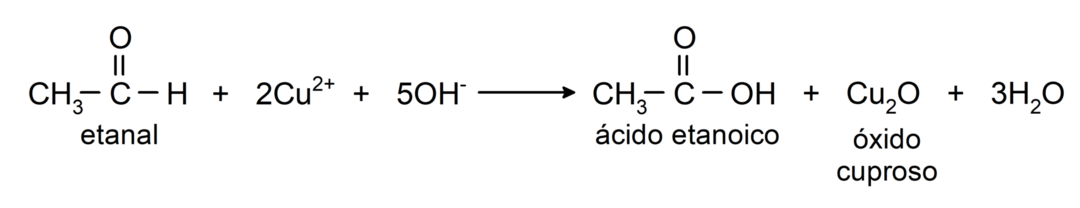
พวกมันได้รับปฏิกิริยาการเติมนิวคลีโอฟิลิกนั่นคือการเติมนิวคลีโอไทล์ให้กับหมู่คาร์บอนิล ตัวอย่างเช่น:
- การเติมกรดไฮโดรไซยานิกเพื่อสร้างไซยาโนไฮดรินหรือไซยาโนไฮดริน
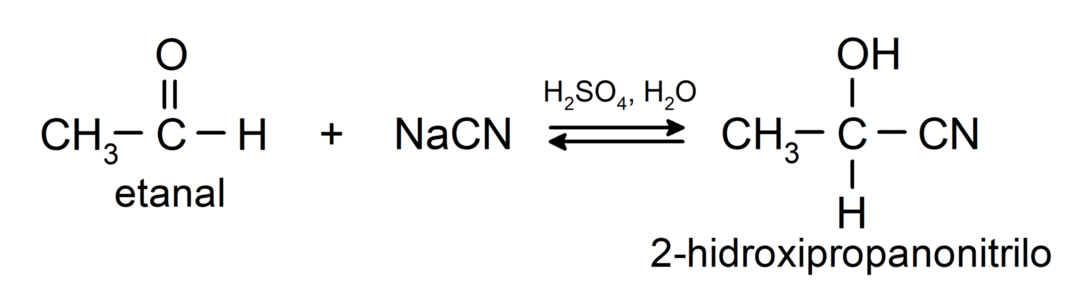
- ในกรณีที่มีกรดแอนไฮดรัส แอลกอฮอล์จะถูกเติมลงในกลุ่มคาร์บอนิลของอัลดีไฮด์เพื่อสร้างอะซีตัลและเฮมิอะซีทัล
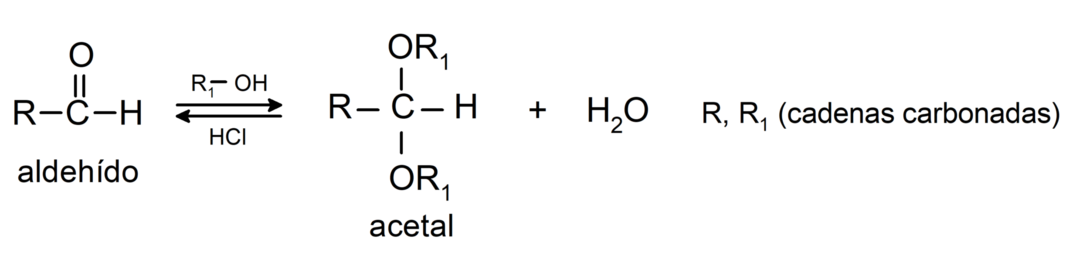
พวกมันเกิดปฏิกิริยาควบแน่นอัลโดล. ในปฏิกิริยาเหล่านี้ อัลดีไฮด์สองตัวจะรวมตัวกันเมื่อมีโซเดียมไฮดรอกไซด์ (NaOH) และ สารประกอบเคมี ผลลัพธ์ที่ได้จึงเรียกว่าอัลโดล ตัวอย่างเช่น:
- ปฏิกิริยาการควบแน่นของเอทานอลเมื่อมี NaOH เจือจาง
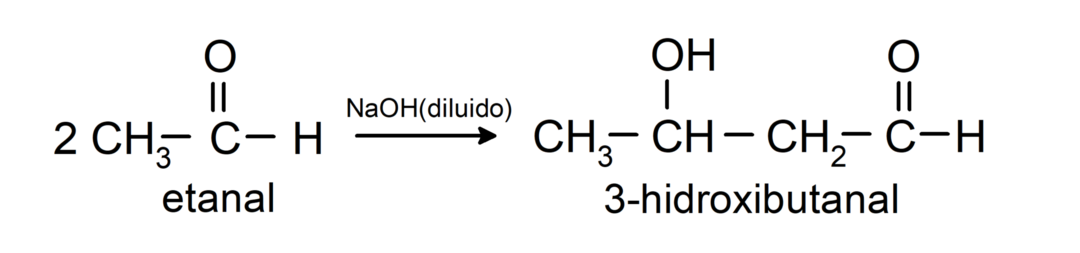
พวกมันจะถูกลดเหลือเป็นแอลกอฮอล์ปฐมภูมิ. อัลดีไฮด์สามารถถูกรีดิวซ์เป็นแอลกอฮอล์ปฐมภูมิได้โดยการเร่งปฏิกิริยาไฮโดรจิเนชันหรือโดยรีดิวซ์ด้วยโซเดียมโบโรไฮไดรด์ (NaBH)4) และลิเธียมอะลูมิเนียมไฮไดรด์ (LiAlH4).
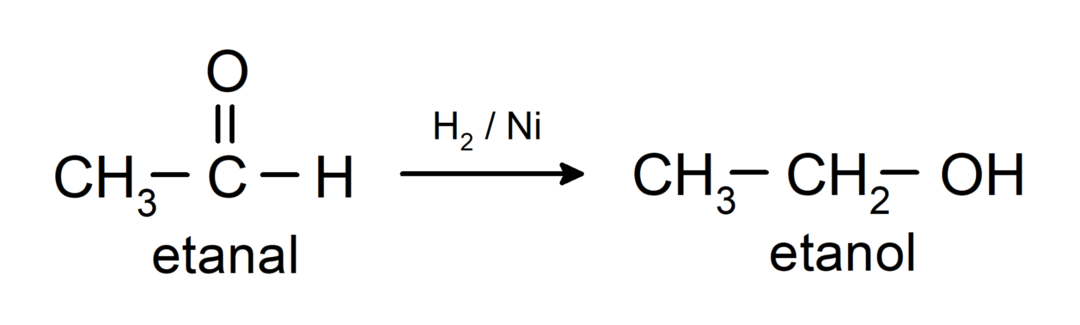
คุณสมบัติทางเคมีของคีโตน
ในบรรดาคุณสมบัติทางเคมีของคีโตนเราสามารถพบ:
พวกมันได้รับปฏิกิริยาการเติมนิวคลีโอฟิลิก. ตัวอย่างเช่น:
- การเติมกรดไฮโดรไซยานิกเพื่อสร้างไซยาโนไฮดรินหรือไซยาโนไฮดริน
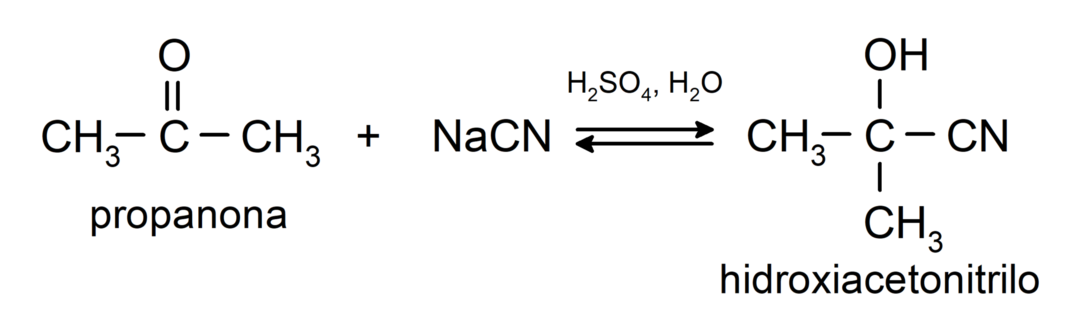
พวกเขาเพิ่มแอลกอฮอล์ (เมื่อมีกรดแอนไฮดรัส) ไปยังกลุ่มคาร์บอนิลของคีโตนเพื่อสร้างคีทัลและเฮมิเคทัล ตัวอย่างเช่น:
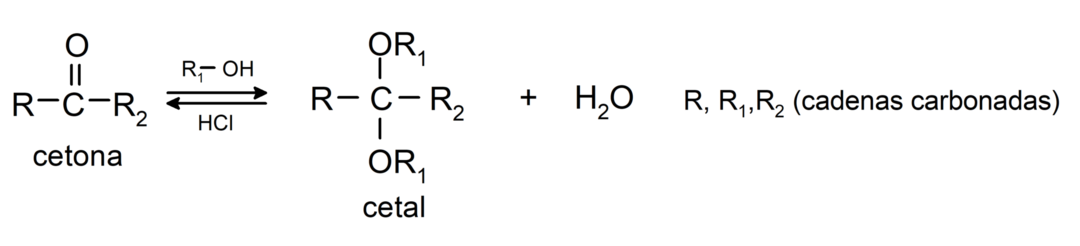
พวกมันเกิดปฏิกิริยาฮาโลเจน. คีโตนที่มีอัลฟ่าไฮโดรเจน (α) ทำปฏิกิริยาโดยการแทนที่ไฮโดรเจนด้วยฮาโลเจน (คลอรีน (Cl), โบรมีน (Br), ไอโอดีน (I), ฟลูออรีน (F)) ต่อหน้ากรดหรือตัวเร่งปฏิกิริยาพื้นฐาน การทดแทนเกิดขึ้นเกือบทั้งหมดในคาร์บอน αนั่นคือคาร์บอนที่เกิดพันธะกับไฮโดรเจน α. ตัวอย่างเช่น:
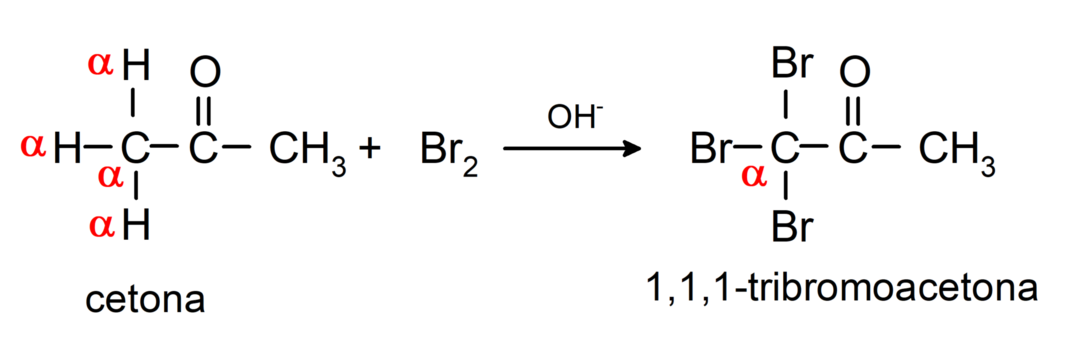
พวกมันจะถูกรีดิวซ์เป็นแอลกอฮอล์ทุติยภูมิ โดยตัวเร่งปฏิกิริยาไฮโดรจิเนชันหรือโดยการรีดักชันด้วยโซเดียมโบโรไฮไดรด์ (NaBH4) และลิเธียมอะลูมิเนียมไฮไดรด์ (LiAlH4). ตัวอย่างเช่น:
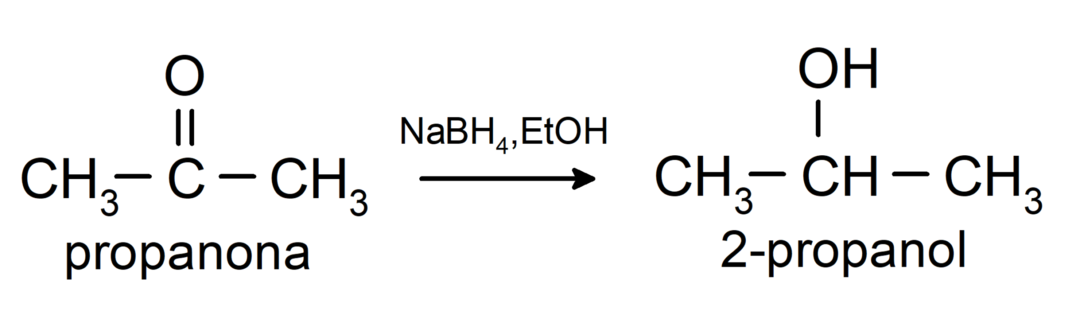
คีโตนไม่ถูกออกซิไดซ์โดยสาร Tollens และ Benedict
ศัพท์เฉพาะของอัลดีไฮด์
ตามกฎที่กำหนดโดยสหภาพเคมีบริสุทธิ์และเคมีประยุกต์นานาชาติ (IUPAC) อัลดีไฮด์ตั้งชื่อโดยใช้คำนำหน้าที่ระบุจำนวนคาร์บอนในสายโซ่ อัดลม. ไม่จำเป็นต้องระบุตำแหน่งของหมู่คาร์บอนิล เนื่องจากจะอยู่ในตำแหน่งที่หนึ่งเสมอที่ปลายด้านหนึ่งของโมเลกุล นอกจากนี้ คำต่อท้าย -al ยังเขียนไว้ท้ายชื่ออัลดีไฮด์อีกด้วย ตัวอย่างเช่น:
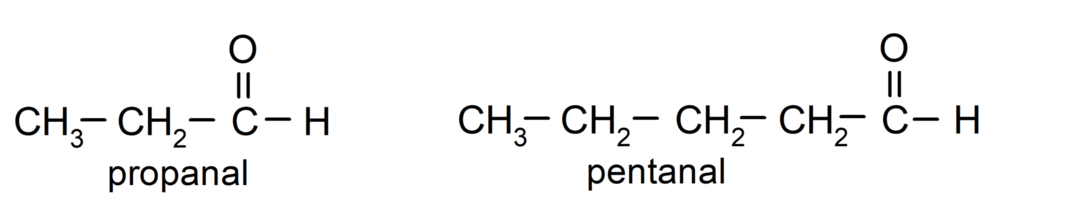
หากอัลดีไฮด์ประกอบด้วยโซ่คาร์บอนหลายสาย กล่าวคือ มีกิ่งก้าน โซ่คาร์บอนที่มีจำนวนอะตอมของคาร์บอนมากที่สุดจะถูกเลือกเป็นโซ่หลัก สายโซ่อื่นๆ ได้รับการตั้งชื่อเป็นกลุ่มองค์ประกอบย่อย และเลือกตำแหน่งของแต่ละองค์ประกอบย่อยเพื่อให้มีจำนวนน้อยที่สุดที่เป็นไปได้ในสายโซ่ นอกจากนี้จะเริ่มนับอะตอมของคาร์บอนตั้งแต่ปลายที่มีหมู่คาร์บอนิล ตัวอย่างเช่น:
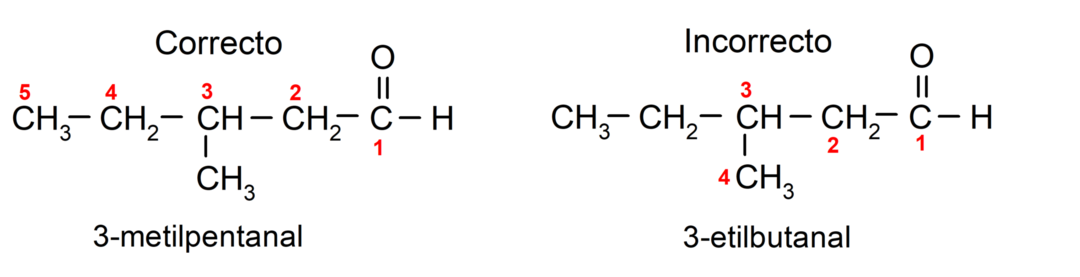
อัลดีไฮด์ที่มีหมู่คาร์บอนิล 2 หมู่ ตั้งชื่อโดยใช้คำต่อท้าย -dial ตัวอย่างเช่น:
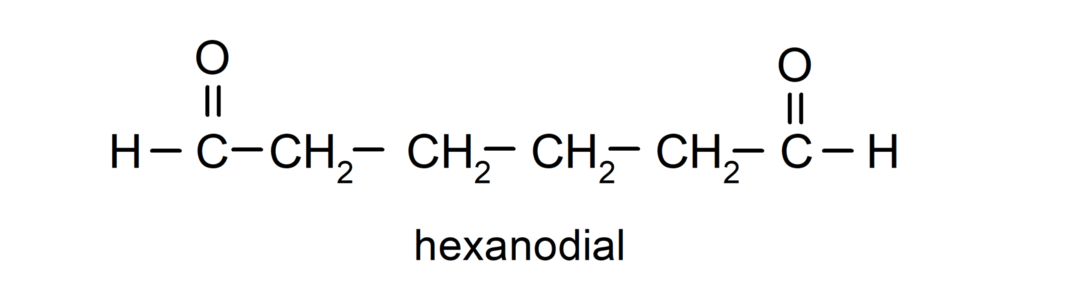
การตั้งชื่อคีโตน
ตามที่สหภาพเคมีบริสุทธิ์และเคมีประยุกต์นานาชาติ (IUPAC) ระบุว่าคีโตนได้รับการตั้งชื่อโดยใช้คำนำหน้าที่ระบุจำนวนคาร์บอนในห่วงโซ่คาร์บอน
ในทางกลับกัน ชื่อของอะซิโตนเขียนโดยใช้คำต่อท้าย -1 นำหน้าด้วยตัวเลขที่ระบุตำแหน่งของหมู่คาร์บอนิลในห่วงโซ่คาร์บอน ควรเลือกตำแหน่งของหมู่คาร์บอนิลในลักษณะที่สอดคล้องกับหมายเลขที่ต่ำที่สุดเท่าที่จะเป็นไปได้ ตัวอย่างเช่น:
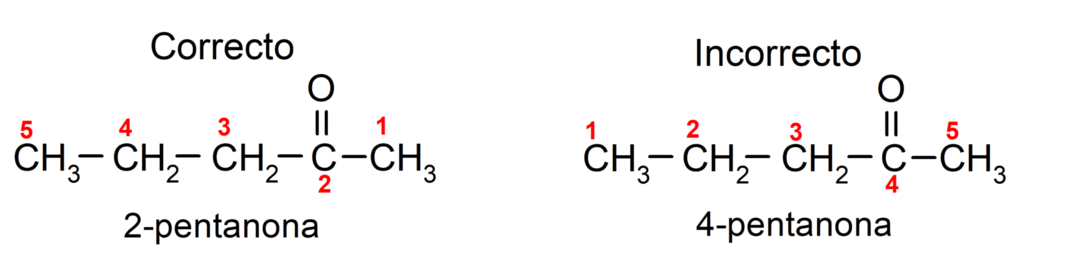
ในการตั้งชื่อคีโตนที่ประกอบด้วยโซ่คาร์บอนหลายสาย เราเลือกเป็นกิ่งก้าน เป็นสายโซ่หลัก คือ สายโซ่คาร์บอนที่มีอะตอมของคาร์บอนมากที่สุดและประกอบด้วยหมู่ คาร์บอนิล โซ่ที่เหลือจะถูกตั้งชื่อเป็นกลุ่มย่อย ตัวอย่างเช่น:
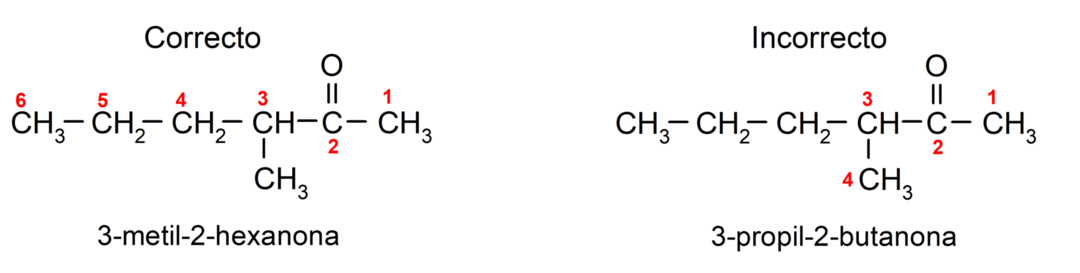
มีคีโตนที่มีหมู่คาร์บอนิล 2 หมู่ เรียกว่าไดโอน ตัวอย่างเช่น:
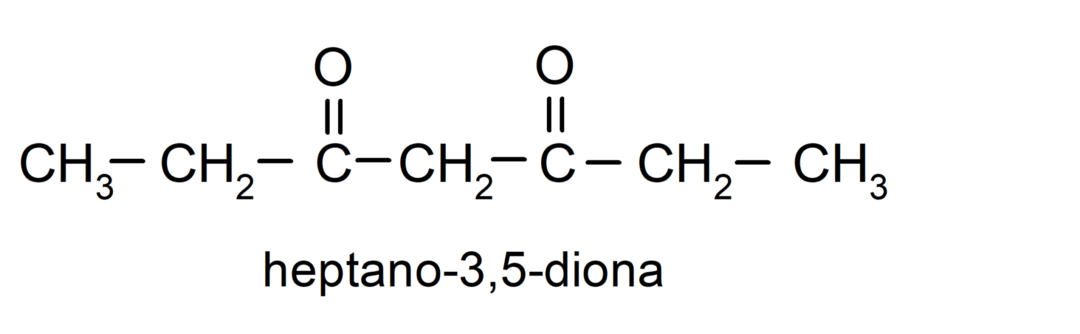
ตัวอย่างของอัลดีไฮด์
- มีทานอล (ฟอร์มาลดีไฮด์)
- เอทานอล (อะซีตัลดีไฮด์)
- โพรพานัล (โพรพัลดีไฮด์)
- บิวทานอล
- เพนทานัล
- เลขฐานสิบหก
- 3-โบรโมไซโคลเพนเทนคาร์บาลดีไฮด์
- ไซโคลเฮกเซนคาร์บาลดีไฮด์
- เบนซาลดีไฮด์
- 4,4-ไดเมทิลเพนทานอล
- 2-ไฮดรอกซี-บิวทานอล
- 2-ไฮดรอกซี-2-เมทิล-บิวทานอล
- 2,3-ไดเมทิลเพนทานอล
- เพนทานีเดียล
- 4-ไฮดรอกซี-3-เมทอกซีเบนซาลดีไฮด์
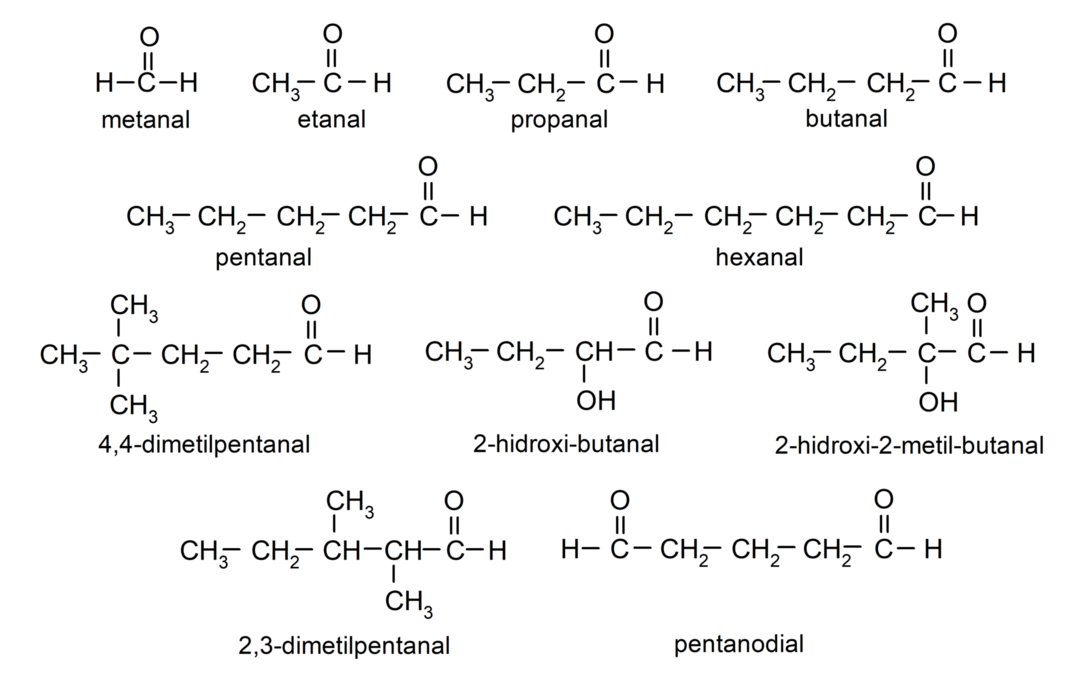
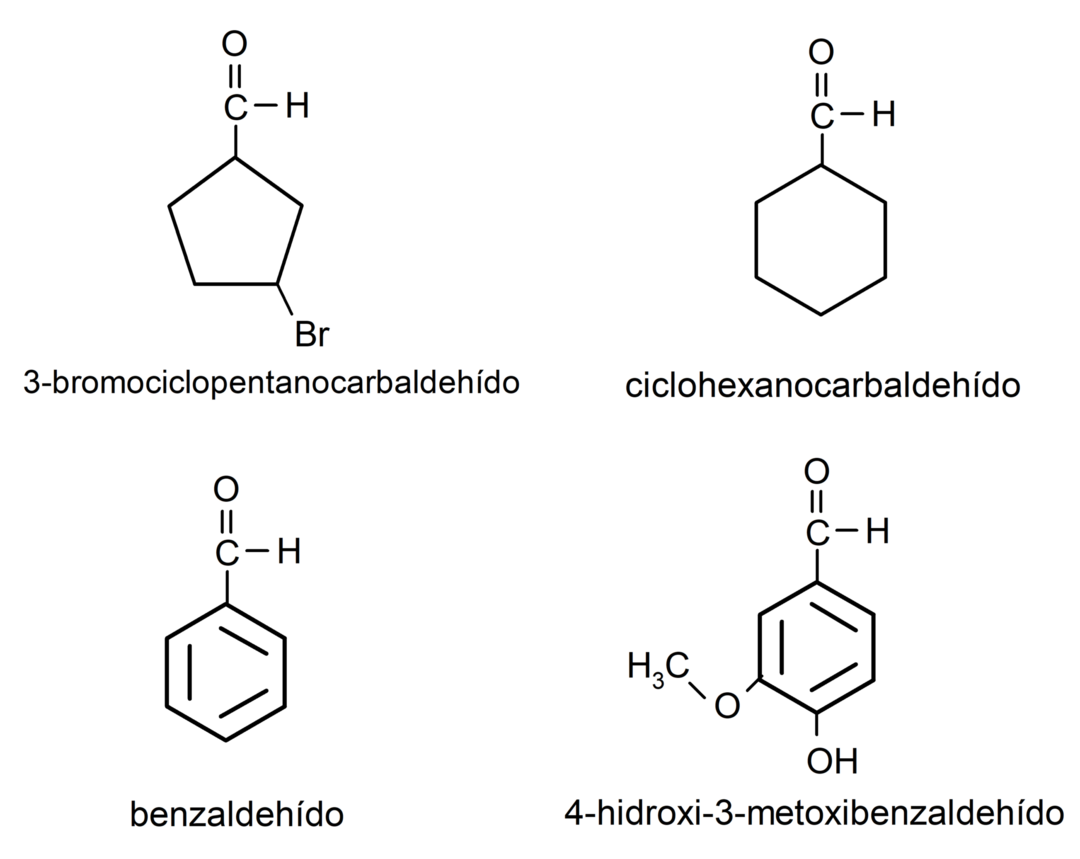
ตัวอย่างของคีโตน
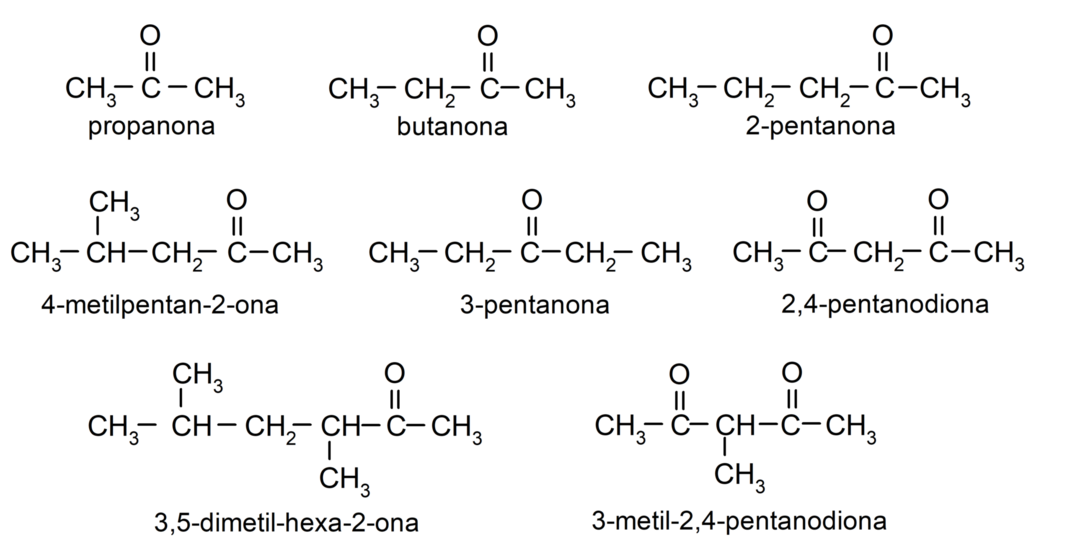
- โพรพาโนน (อะซิโตน)
- บิวทาโนน
- 2-เพนทาโนน
- 4-เมทิลเพนแทน-2-วัน
- 3-เมทิลไซโคลเฮกซาโนน
- ไซโคลเฮกซิลเมทิลคีโตน
- 3,4 ไดเมทิล-เฮกซัน-2-โอน
- เอทิลฟีนิลคีโตน
- 2,4-เพนทาไดโอน
- ไซโคลเฮกซาโนน
- 3-เพนทาโนน
- 3-เมทิล-2,4-เพนทาไดโอน
- 1-ฟีนิลโพรพาโนน
- ไซโคลเพนทาโนน
- ไดฟีนิล คีโตน
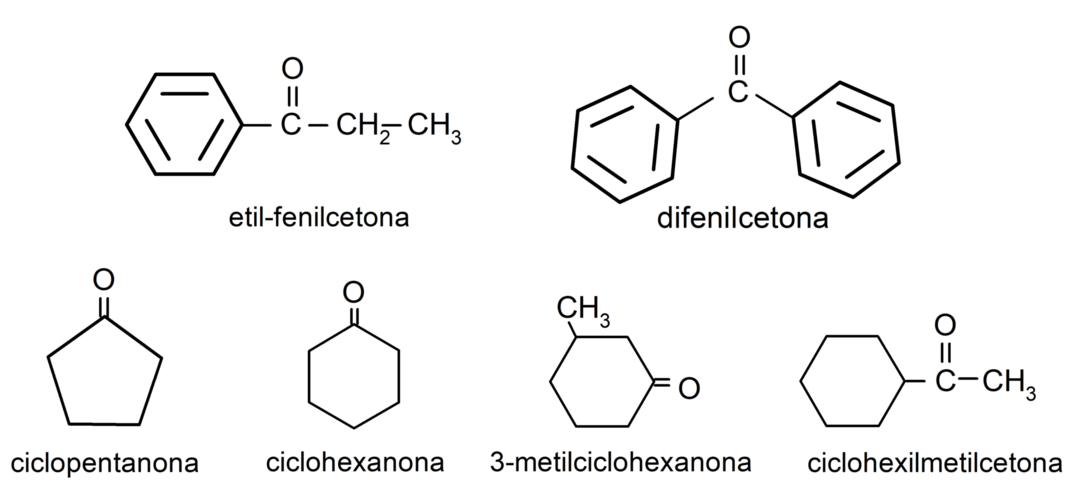
การใช้อัลดีไฮด์ในชีวิตประจำวัน
การใช้อัลดีไฮด์บางประการคือ:
- ใช้ในการผลิตตัวทำละลาย สี น้ำหอม เรซิน และสาระสำคัญ
- ใช้เป็นสารกันบูดในผลิตภัณฑ์เครื่องสำอาง ตัวอย่างทางชีวภาพ และศพ ฟอร์มาลดีไฮด์ถูกใช้มากที่สุดเพื่อจุดประสงค์เหล่านี้
- ใช้ในการผลิตพลาสติกซึ่งสามารถทดแทนชิ้นส่วนโลหะในอุตสาหกรรมยานยนต์ได้
- ใช้เป็นเครื่องปรุงสำหรับอาหารบางชนิด
- พวกมันถูกใช้เป็นสารฆ่าเชื้อ
- พวกมันถูกใช้เพื่อผลิตวัตถุระเบิดบางชนิด เช่น เพนตะเอริทริทอล เตตราไนเตรต (TNPE)
การใช้คีโตนในชีวิตประจำวัน
การใช้คีโตนบางประการคือ:
- ใช้ในการผลิตตัวทำละลาย โดยเฉพาะอะซิโตนมีการใช้กันอย่างแพร่หลายในการขจัดสีและแลคเกอร์
- ใช้ในการผลิตยางและน้ำมันหล่อลื่นบางชนิด
- ใช้ในการผลิตสี แลคเกอร์ และวาร์นิช
- ใช้ในการผลิตยาและเครื่องสำอาง
ความเป็นพิษของอัลดีไฮด์และคีโตน
- พวกอัลดีไฮด์. การสัมผัสกับอัลดีไฮด์ทำให้เกิดการระคายเคืองต่อผิวหนัง ดวงตา และทางเดินหายใจ นอกจากนี้ การสัมผัสกับอัลดีไฮด์ยังเชื่อมโยงกับโรคต่างๆ เช่น มะเร็ง ผิวหนังอักเสบจากการสัมผัส และโรคตับและระบบประสาทเสื่อม ตัวอย่างเช่น ฟอร์มาลดีไฮด์ได้รับการพิจารณาโดย WHO (องค์การอนามัยโลก) ให้เป็นสารประกอบก่อมะเร็ง
- คีโตน. การได้รับคีโตนซ้ำๆ อาจทำให้เกิดความเสียหายต่อระบบประสาทส่วนกลางได้ สิ่งนี้สามารถนำไปสู่การสูญเสียความทรงจำ ความอ่อนแอ ปวดกล้ามเนื้อ และตะคริว นอกจากนี้หากผิวหนังสัมผัสกับคีโตน จะเกิดความแห้งและแตกร้าว ในทางกลับกัน หากสูดดมคีโตน จะเกิดการระคายเคืองต่อทางเดินหายใจและไอ
อ้างอิง
- ลอเรนส์ โมลินา, เจ.เอ. (2018). “อัลดีไฮด์และคีโตน: ตัวอย่างบางส่วน” http://hdl.handle.net/
- Gabriel Pinto Cañón, Manuela Martín Sánchez, José María Hernández Hernández, María Teresa Martín Sánchez (2015) “สาร Tollens: ตั้งแต่การระบุอัลดีไฮด์ไปจนถึงการใช้นาโนเทคโนโลยี แง่มุมทางประวัติศาสตร์และการประยุกต์การสอน”ฉบับที่ 111 เลขที่ 3. ราชสมาคมเคมีแห่งสเปน
- วิลเลียม บาวเออร์ จูเนียร์ (2000) «กรดเมทาอะคริลิกและอนุพันธ์» ใน Ullmann’s Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim ดอย: 10.1002/14356007.a16_441.
- “พวกมันเปิดเผยกลไกใหม่ของความเป็นพิษในกลุ่มสารประกอบก่อมะเร็งที่ได้มาจากอาหารและสิ่งแวดล้อม” (2022) ใน: www.conicet.gov.ar มีจำหน่ายใน: https://www.conicet.gov.ar/ เข้าถึงได้: 20 มิถุนายน 2023.
ติดตามด้วย:
- แอลกอฮอล์
- น้ำตาล
- อัลเคน


