50 Çözüm örnekleri
Çeşitli / / July 04, 2021
çözümler türlerinden biridir karışımlar bulunmakta. Bir çözeltiyi oluşturan bileşenler, kimyasal olarak reaksiyona girmezler, ancak bu bileşenlerin fiziksel özellikleri, çözeltinin bir parçası olduklarında değiştirilebilir. Örneğin: duman, amalgam, sütlü kahve.
Bir karışımın çözelti olabilmesi için homojen Y üniformayani, karışık bileşenlerin çıplak gözle ayırt edilememesi ve buna ek olarak, çözünen (daha az miktarda görünen bir madde) ile madde arasındaki orantı. çözücü (daha fazla miktarda görünen madde), çözeltiden alınan hacim ne olursa olsun yaklaşık olarak değişmeden kalır. Çözeltideki veya çözücüdeki çözünenin oranı "konsantrasyon" olarak adlandırılır ve genellikle aynı çözelti, çeşitli çözünen konsantrasyonları kullanılarak hazırlanabilir.
Çözeltiler, karıştırılmadan önce farklı maddelerden herhangi birinde bulunan maddeler arasında oluşabilir. toplama durumları. Hemen hemen tüm toplama durumlarında çözümler vardır. Genel olarak, çözeltinin kümelenme durumu, çözücünün kümelenme durumu ile belirlenir. Örneğin:
için yaygın moleküllerin varlığı Çözücü içindeki çözünenin miktarı, çözücünün kendisinin özelliklerini değiştirir. Örneğin, iki bileşiğin erime ve kaynama noktaları, bu bileşikler karıştırıldığında, bileşimleri gibi değişir. yoğunluklar ve renkler.
Fransız Bilim Adamı Rol Çözümlerdeki bileşenlerin bu davranışını inceledi ve ayrıca ana yasasını önerdi (Roult Yasası), ideal bir çözeltiyi çevreleyen buhar karışımındaki her bir bileşenin kısmi buhar basıncını ifade eder. itibaren sıvılar her bir saf bileşenin kısmi basıncı ile çözeltideki mol kesrinin çarpımına eşittir. İdeal bir çözüm, kimyasal türlerin çok benzer olduğu bir çözüm olarak kabul edilir, bu nedenle aralarındaki etkileşimlerin enerjisinde herhangi bir değişiklik göz önüne alınmaz. Roult Yasasının temel denklemi:
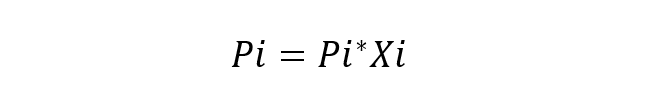
Nerede:
- Pi bileşenin kısmi basıncıdır ben Çözeltiyi çevreleyen gaz halindeki karışımda.
- Pi* bileşenin basıncıdır ben
- Xi bileşenin mol kesridir ben çözülme içinde.
Açıkçası, insanlar kalıcı olarak çözümlerle temas halindedir. hava elementlerin çözünmesidir gaz hali: çoğunluk bileşimi tarafından verilir azot (%78) ve geri kalanı %21'i tarafından işgal edilmiştir. oksijen ve diğer bileşenlerin %1'i, ancak bu oranlar biraz değişebilir.
Çözüm örnekleri
Aşağıdaki liste, her birinin bulunduğu kümelenme durumunu, ilgili bir çözücüde bir çözünen maddeyi vurgulayan kırk çözelti örneği içerir.
- Hava (gaz içinde gaz). Azotun en bol olduğu bir gaz bileşimi.
- Sigara içmek (gazda katı). Yangından çıkan duman nedeniyle hava bayatlamış. Havanın çözücü görevi gördüğü bir çözeltidir.
- metaller arasındaki alaşımlar (katı içinde katı). Duralumin, alüminyum, bakır, manganez, magnezyum ve silikondan oluşan bir alaşımdır.
- Atmosferik hava tozu (gazda katı). Gazda katıların (neredeyse bölünmez bir birime ayrışmış ama sonunda katı) varlığı bu anlamda bir çözünme örneğidir.
- Çelik (katı içinde katı). alaşım demir ve karbon arasında, öncekinden çok daha yüksek oranda.
- Karbonatlı içecekler (sıvı içinde gaz). Gazlı içecekler bir sıvı içinde gazların çözünmesine sahiptir.
- amalgam (katı içinde sıvı). Belirli bir ortamda çözünmüş cıva alaşımlarıdır. metaller altın veya gümüş gibi.
- rafine petrol (sıvı içinde sıvı). Onu oluşturan elementlerin kombinasyonu (çoğu karbondur), sıvılar arasında bir çözünmeye yol açar.
- havada bütan (gaz içinde gaz). Bütan bir kimyasal bileşik tüplerde depolanabilen, yakıt olarak kullanılmaya hazır gaz halindedir.
- Okyanus suyundaki oksijen (sıvı içinde gaz). Deniz suyunun oksijenlenmesi, su yaşamının gelişmesine izin verir.
- Alkol içeriği olan içecekler (sıvı içinde sıvı). Kutlamalarda insanlar tarafından çok tüketilirler. Genellikle kontrollü konsantrasyonlarda etanol ve meyve sularının çözeltileridir. alkol.
- Sütlü kahve (sıvı içinde sıvı). Daha yüksek içeriğe sahip bir sıvı, diğerinden biraz alır, bu da renginin ve aromasının dönüşümünü temsil eder.
- duman (gazlar gazlara dönüşür). Atmosfere özgü olmayan gazların girişi, havanın dönüşümüne neden olur. onu soluyan toplumlar üzerinde olumsuz etkileri vardır: ne kadar konsantre olursa o kadar zararlı olur.
- suda tuz (sıvı içinde katı). Yemek pişirmek için yaygın olarak kullanılır.
- Kan (sıvı içinde sıvı). Çoğunluk bileşeni plazmadır (sıvı) ve içinde kırmızı kan hücrelerinin öne çıktığı diğer elementler ortaya çıkar.
- sudaki amonyak (sıvı içinde sıvı). Bu çözüm (gazdan sıvıya da yapılabilir), birçok temizlik malzemesi için işlevseldir.
- Nem izleri olan hava (gaz içinde sıvı). artması nedeniyle havada su buharı bulunur. sıcaklık.
- Toz meyve suları (sıvı içinde katı). Toz suda çözünür ve toz meyve suyu renginde bir çözelti üretir.
- paladyumdaki hidrojen (katıda gaz). Hidrojen bazı metallerde çok iyi çözünür.
- Havadaki Virüsler (gazda katı). Atmosferik toz gibi, bir gaz tarafından taşınan çok küçük katı birimlerdir.
- gümüş cıva (katı içinde sıvı). Sözde "amalgam"lardan biridir.
- Çay (sıvı içinde katı). Çok küçük boyutlardaki bir katı (zarfın granitleri) suda çözünür.
- Kraliyet suyu (sıvı içinde sıvı). Bu bir kompozisyon asitler Bu, aralarında altının göründüğü farklı metallerin çözülmesini sağlar.
- Bronz (katı içinde katı). Bakır ve kalay arasındaki alaşımdır.
- Limonata (sıvı içinde sıvı. Çoğu zaman karışım katı ve sıvı arasında olmasına rağmen, aslında limon suyu gibi o katıda bulunan bir sıvıdır.
- Peroksit (sıvı içinde sıvı). Bu bir hidrojen peroksit çözeltisidir (H2VEYA2) Suda. Yaraları dezenfekte etmek için ve kozmetik endüstrisinde kullanılır.
- Pirinç (katı içinde katı). Katı bakır ve çinko arasındaki alaşımdır.
- buz soğutma (sıvı içinde katı). Buz sıvıya girer ve çözülürken soğutur. Suya girmişse, aynı madde olduğu özel durumdur.
- fizyolojik çözüm (sıvı içinde sıvı). Su bir çözücü görevi görür ve birçok sıvı madde bir çözünen olarak işlev görür.
- Smoothie'ler (sıvılardaki katılar). Öğütme işlemi ile katılardan sıvılara bir kombinasyon indüklenir.
Şununla takip edin: