Aromatik Bileşikler Örneği
Kimya / / July 04, 2021
Kimyacılar, tüm organik bileşikleri iki geniş sınıfa ayırmayı faydalı bulmuşlardır: bileşikler alifatik ve bileşikler aromatikler. Aromatik bileşikler Benzen ve benzer kimyasal davranışa sahip bileşiklerdir. Benzen'i Alifatik Hidrokarbonlardan ayıran şey aromatik özelliklerdir. Benzen molekülü, belirli bir tipte bir halkadır. Yapısal olarak benzenden farklı gibi görünen ve yine de benzer şekilde davranan halka şeklinde başka bileşikler de vardır.
Bu diğer bileşiklerin temel elektronik yapılarında benzene benzediği ortaya çıktı, bu yüzden aromatik olarak da davranıyorlar.
Alifatik hidrokarbonlar (alkanlar, alkenler, alkinler ve bunların döngüsel analogları) esas olarak ilave, birden çok bağlantıda ve serbest radikal ikamesi, alifatik zincirin diğer noktalarında.
Öte yandan, aromatik hidrokarbonların, mayalanma eğilimine sahip oldukları vurgulanmaktadır. heterolitik ikame. Ayrıca, bu aynı ikame reaksiyonları, molekülün başka hangi fonksiyonel grupları içerebileceğinden bağımsız olarak, göründükleri her yerde aromatik halkaların karakteristiğidir. Bu son gruplar aromatik halkaların reaktivitesini etkiler ve bunun tersi de geçerlidir.
benzen molekülü
Benzen 1825'ten beri bilinmektedir ve kimyasal ve fiziksel özellikleri diğer organik bileşiklerden daha iyi bilinmektedir. Buna rağmen, 1931 yılına kadar bunun için tatmin edici bir yapı önerilmemiştir. Kimyasallar arasında genel kullanıma girmesi 15 yılı bulmaktadır. organik. Zorluk, yapısal teorinin o zamana kadar ulaştığı gelişimin sınırlamalarında yatıyordu. Birkaç önemli gerçeğin varsayımı sayesinde nihai yapıya ulaşılmıştır:
Benzen moleküler formül C'ye sahiptir.6H6. Elementel bileşimi ve moleküler ağırlığı nedeniyle benzenin altı Karbon ve altı Hidrojen atomuna sahip olduğu biliniyordu. Sorun, bu tür atomların düzenini bilmekti.
1858'de August Kekulé, Karbon atomlarının zincirler oluşturmak için birbirine bağlanabileceğini öne sürdü. Daha sonra 1865'te benzen sorununa bir cevap önerdi: Bu karbonat zincirleri bazen halkalar oluşturmak üzere kapanabilir.
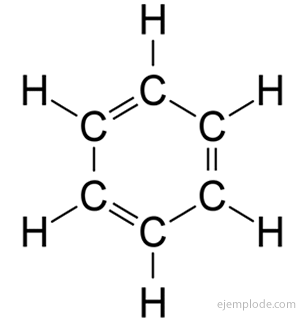
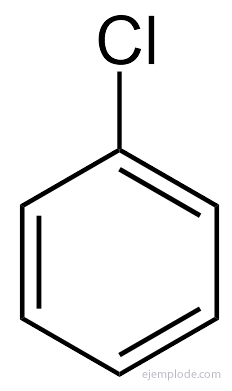
Benzen sadece tek ikameli bir ürün C verir6H5Y. Örneğin, bir hidrojen atomu Bromin ile değiştirildiğinde, BromoBenzene C'nin yalnızca tek bir konfigürasyonu elde edilir.6H5Br; benzer şekilde, bir KloroBenzen C de elde edilir6H5Cl veya bir NitroBenzen C6H5DEĞİL2, vb. Bu gerçek, Benzen'in yapısına ciddi bir sınırlama getirir: tüm Hidrojeni olmalıdır. tam olarak eşdeğerdir, yani hepsi sırayla hepsi eşit olan Karbonlara birleştirilmelidir. bağlantılı. CH'de hidrojen olamaz3, ve diğerleri CH'de2, ve diğerleri CH'de. Tekli ikamenin nihai yapısı, Benzen içindeki herhangi bir Hidrojenin ikamesi için aynı olmalıdır.
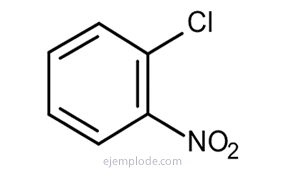
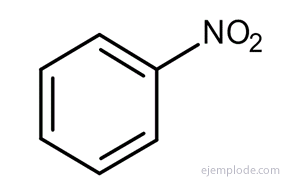
Benzen, üç izomerik ikamesiz ürün verir, C6H4Y2 veya C6H4VE Z. Yalnızca üç izomerik DiBromoBenzenes vardır, C6H4Br2, üç KloroNitroBenzen C6H4CINO2, vb. Bu gerçek, yapısal olasılıkları daha da sınırlandırmaktadır.
Benzen, ekleme reaksiyonlarından ziyade ikame reaksiyonlarına girer. Kekulé'nin benzen yapısı, Sikloheksatrien diyeceğimiz yapıya karşılık gelir. Bu nedenle, alkenlerin yapısının bir özelliği olan benzer bileşikler, sikloheksadien ve sikloheksen gibi ilave edilerek kolayca reaksiyona girmelidir. Ama durum böyle değil; alkenlerin hızlı reaksiyona girdiği koşullar altında benzen reaksiyona girmez veya çok yavaş reaksiyona girer. Benzen, ekleme reaksiyonları yerine kolaylıkla bir dizi reaksiyona girer; ikame, olarak nitrasyon, sülfonasyon, halojenasyon, Friedel-Crafts alkilasyonu, asilasyon itibaren Friedel-El Sanatları. Bu reaksiyonların her birinde, bir atom veya grup, Benzenin Hidrojen atomlarından biri ile değiştirilmiştir.
Benzenin kararlılığı, alternatif çift bağlardan ve ayrıca rezonans enerjisinden kaynaklanmaktadır. çift bağların aynı değişimi koruyarak karbonlar arasındaki konumlarını değiştirdiği bağ yapısal. Dır-dir rezonans stabilizasyon enerjisi olarak adlandırılan özellikler kümesinden sorumludur. Aromatik Özellikler.
Bir Ekleme reaksiyonu, bir alkeni daha kararlı bir doymuş bileşiğe dönüştürür. Ancak Benzen durumunda, bir Ekleme, rezonansla sürdürülen ve stabilize edilen halka sistemini yok ederek onu daha az kararlı hale getirir. Son molekül Sikloheksadien olacaktır. Bu nedenle, Benzenin kararlılığı onu yalnızca Yer Değiştirme reaksiyonlarına yol açar.
Aromatik Bileşiklerin Özellikleri
Benzen halkaları içeren maddelere ek olarak, aromatik olarak kabul edilen başka maddeler de vardır, ancak yüzeyde benzen ile neredeyse hiç benzerlik göstermezler.
Deneysel bir bakış açısından, aromatik bileşikler, moleküler formülleri bir yüksek derecede doymamışlık, bunlara rağmen ekleme reaksiyonlarına dirençli doymamış bileşiklerin karakteristiğidir.
Bunun yerine, bu aromatik bileşikler bir genellikle elektrofilik yer değiştirme reaksiyonlarına girer Benzen'e benzer. Eklemeye karşı bu direncin yanı sıra ve muhtemelen bundan dolayı, olağandışı kararlılıkdüşük hidrojenasyon ve yanma ısıları gibi.
Aromatik maddeler döngüseldir, genellikle beş, altı ve yedi atomlu halkalar sunar ve fiziksel incelemeleri, sahip olduklarını gösterir. düz veya neredeyse düz moleküller. Protonları, Nükleer Manyetik Rezonans spektrumlarında Benzen ve Türevlerinde olduğu gibi aynı tip kimyasal kaymaya sahiptir.
Teorik bir bakış açısından, bir maddenin aromatik olması için molekülü, molekül düzleminin üstünde ve altında delokalize π elektronlarından oluşan döngüsel bulutlara sahip olmalıdır; Ayrıca, bu π bulutları toplam (4n + 2) π elektronu içermelidir; bu, aromatik bir bileşiği karakterize eden belirli stabilitenin sonuçlanması için delokalizasyonun yeterli olmadığı anlamına gelir.
Benzen Türevlerinin (Aromatik Bileşikler) Adlandırılması
Bu türevlerin birçoğunda, özellikle tek ikameli türevlerde, Benzen kelimesi için ikame grubu, örneğin, ChloroBenzene, BromoBenzene, IodoBenzene, nitrobenzen.
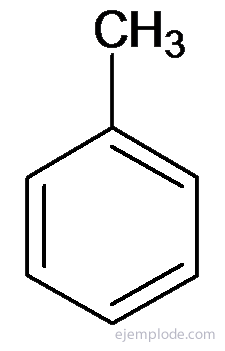
Diğer türevler, ikame grubunun adıyla benzerlik göstermeyen özel adlara sahiptir. Örneğin Metil Benzen sadece Toluen olarak bilinir; Anilin olarak AminoBenzen; Fenol olarak hidroksibenzen, vb.
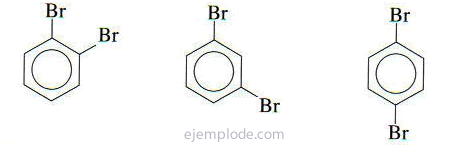
Benzen halkasına bağlı iki grup varsa, sadece ne olduklarını değil, aynı zamanda göreceli konumlarını da belirtmek gerekir. Disübstitüe edilmiş benzenler için olası üç izomer, orto, meta ve para önekleriyle, kısaltılmış o-, m-, p- ile karakterize edilir. Örneğin: o-DiBromoBenzene, m-DiBromoBenzene, p-DiBromoBenzene.
İki gruptan biri moleküle özel isim veren türden ise bileşik o özel maddenin türevi olarak adlandırılır. Örneğin: NitroToluen, Bromophenol, vb.
Aromatik Bileşiklere Örnekler
Toluen veya Metilbenzen
etilbenzen
izopropilbenzen
TriNitroToluen veya TNT
Anilin veya Aminobenzen
Benzoik asit
Glutamik Asit veya ParaAminoBenzoik Asit
Toluen Sülfonik Asit
Fenol veya Hidroksibenzen
bromofenol
trikloro benzen
Benzen Fenil Eter
iyot benzen
bromo benzen

