20 Приклади ідеального та реального газу
Різне / / July 04, 2021
хімія є наук що вивчає склад та перетворення, які можуть відбуватися з речовиною в будь-якій її формі. Однією з найважливіших галузей хімії є тематика гази.
газова концепція Його заснував бельгійський хімік Ян ван Гельмонт. Для пояснення поведінки газів були розроблені різні математичні рівняння із використанням статистичних інструментів. Однак необхідно було спростити та модифікувати ці рівняння, оскільки вони працювали не для всіх типів газів, тому були визначені різні моделі газу (ідеальний газ Y справжній газ, серед інших проміжних підходів). Наприклад: азот, гелій, метан.
У цьому сенсі було встановлено три закони, які загальним чином співвідносять обсяг, температури і тиск газів:
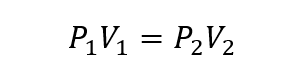
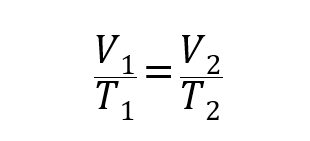
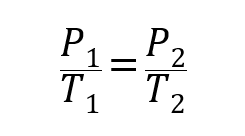
Де P1, V1 Y Т1- початковий тиск, об'єм і температура газу відповідно, і P2, V2 Y Т2 є фінали.
Таким чином, пов'язуючи три закони, ми отримуємо Загальне газове законодавство,
PV / T = C де C. є константою, яка залежить від кількості газу.
Ідеальні приклади газу
ідеальний газ це теоретична модель, яка представляє газ, якого насправді не існує. Це інструмент для полегшення великої кількості математичних розрахунків, оскільки значно спрощує складну поведінку газу. Вважається, що цей газ складається з частинок, які ні притягують, ні відштовхують одна одну і зіткнення яких є абсолютно пружними. Це модель, яка виходить з ладу, якщо на газ діє високий тиск і низькі температури.
загальне рівняння ідеальний газ є результатом поєднання законів Бойля-Маріотта, Чарльза та Гей-Люссака із законом Авогадро. Закон Авогадро стверджує, що якщо різні газоподібні речовини містяться в однакових обсягах і піддаються однаковому тиску і температурі, то вони мають однакові номер частинок. Таким чином, рівняння стану ідеального газу є: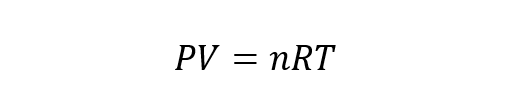
Де п - кількість молей газу і Р. - газова константа, що дорівнює 8,314 Дж / Кмоль.
Неможливо скласти конкретний список ідеальних газів, оскільки це гіпотетичний газ. Можна перелічити групу газів (включаючи благородні гази), обробка яких може бути наближена до обробки газів ідеально, оскільки характеристики схожі, якщо тиск і температурні умови є нормальний.
- Азот (N2)
- Кисень (O2)
- Гідроген (H2)
- Вуглекислий газ (CO2)
- Гелій (He)
- Неон (Ne)
- Аргон (Ar)
- Криптон (Кр)
- Ксенон (Xe)
- Радон (Rn)
Приклади реальних газів
реальні гази Вони мають термодинамічну поведінку, і тому вони не дотримуються того самого рівняння стану, що і ідеальні гази. При високому тиску та низькій температурі гази неминуче слід вважати реальними, оскільки в такому випадку взаємодія між їх частинками посилюється.
істотна різниця між ідеальним газом і реальним газом є те, що останній не можна стискати безкінечно, але його здатність до стиснення залежить від рівня тиску та температури.
Для пояснення поведінки реальних газів були розроблені різні рівняння. Одним з найважливіших є той, який був запропонований Ван дер Ваальсом у 1873 році, і який повинен застосовуватися в умовах високого тиску. Рівняння Ван дер Ваальса представляється як:
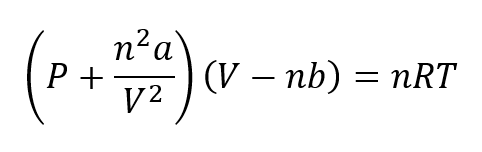
Де доY bвони є постійними, що відносяться до природи кожного газу.
У наведеному нижче списку показано кілька прикладів реальних газів, хоча ви також можете додати такі, що вже є були перераховані як ідеальні гази, але цього разу в контексті високого тиску та / або низького температури.
- Аміак (NH3)
- Метан (СН4)
- Етан (СН3СН3)
- Ефін (СН2СН2)
- Пропан (СН3СН2СН3)
- Бутан (СН3СН2СН2СН3)
Слідуйте за:


