20 Приклади алканів
Різне / / July 04, 2021
алкани вони свого роду вуглеводні в яких змінна кількість атомів вуглецю з'єднана між собою одинарними зв'язками, як скелет, і кожен атом вуглецю в свою чергу приєднаний до атомів водню, які з часом можуть бути замінені іншими атоми або функціональні групи. Наприклад: хлороформ, метан, октан.
молекулярна формула алканів з відкритим лінійним ланцюгом становить CnH2n + 2, де C являє собою вуглець, H являє собою водень і n являє собою кількість атомів вуглецю. Алкани - це насичені вуглеводні, що означає, що вони не мають подвійних або потрійних зв’язків. Щоб назвати їх, ви використовуєте суфікс "-Ano" після називання вуглецевого ланцюга за допомогою префікс що відповідає кількості атомів вуглецю (et- (2), pro- (3), but- (4), pen- (5), hex- (6), hep- (7) тощо).
Це може послужити вам:
Класифікація алканів
У алканах їх зазвичай розпізнають дві великі групи: відкритий ланцюг (також званий ациклічним) та закритий ланцюг (або циклічний).
Коли сполуки з відкритим ланцюгом Вони не містять заміщення водню, що супроводжує кожен атом вуглецю, їх називають лінійними алканами: це найпростіші алкани. Коли вони представляють заміщення будь-якого з їх воднів одним або кількома вуглецевими ланцюгами, їх називають розгалуженими алканами. Найбільш поширеними заступниками є етилові групи (СН
3СН2-) і метил (СН3-).Зі свого боку в молекулі є сполуки з одним циклом (моноциклічні) та інші з кількома (поліциклічні). циклічні алкани вони можуть бути гомоциклічними (вони утворюються з виключним втручанням атомів вуглецю) або гетероциклічними (в яких беруть участь інші атоми, наприклад, кисень або сірка).
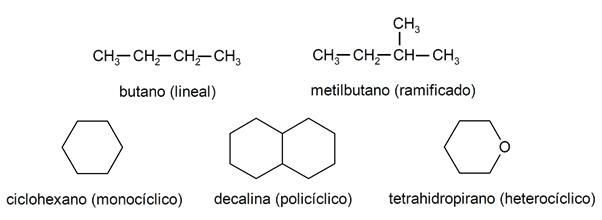
Фізичні властивості алканів
Загалом, фізичні властивості алканів обумовлені молекулярною масою (в свою чергу пов'язаною з довжиною вуглецевого ланцюга). Ті, у кого вуглець найменший газоподібний до температури навколишнього середовища, це від 5 до 18 атомів вуглецю рідини, і вище цього числа твердий (схожий на віск).
Будучи менш щільними, ніж вода, вони, як правило, плавають на ній. Загалом, алкани нерозчинні у воді та розчинні в органічних розчинниках.
Суть кипіння та з синтез алканів залежить від їх молекулярна маса, тобто від довжини вуглецевого ланцюга, хоча вони також багаторазово залежать від просторового розташування атомів. Лінійні та циклічні алкани мають вищі температури кипіння, ніж розгалужені.
Хімічні властивості алканів
Алкани характеризуються буттям хімічні сполуки дуже погана реакційна здатність, тому вони також відомі як "парафіни" (латиною, parum affinis означає "низька спорідненість"). Вони є сполуками, які мають дуже високу енергію активації, коли в них беруть участь хімічні реакції. Найважливішою реакцією, яку можуть зазнати алкани, є горіння утворюючи, у присутності кисню, тепла, вуглекислого газу та води.
Алкани є основою для важливого різноманіття реакцій, пов'язаних з промислові процеси дуже важливо, будучи найбільш традиційним видом палива. Вони також виступають кінцевими продуктами біологічних процесів, таких як метаногенне бродіння, яке проводять деякі мікроорганізми.
Приклади алканів
Деякі приклади алканів (включаючи деякі добре відомі лінійні та розгалужені):
- Хлороформ (химерна назва трихлорметан; CHCl3). Раніше пари цієї речовини використовувались як анестетики. З цією метою його припинено, оскільки було встановлено, що він пошкоджений органів такі, як печінка або нирки. Сьогодні його використання в основному застосовується як розчинник або охолоджуюча рідина.
- Метан (СН4). Це найпростіший алкан з усіх: він складається лише з одного атома вуглецю та чотирьох атомів водню. Це газ, який природним чином відбувається при розкладанні різних органічних субстратів і є основною складовою природного газу. Останнім часом він був визнаний одним із газів, який найбільше сприяє так званому парниковому ефекту.
- Октан (C8H18). Це восьмивуглецевий алкан і має велике значення, оскільки він визначає остаточну якість нафти, яка є суміш різних вуглеводнів. Ця якість вимірюється октановим чи октановим числом палива, яке приймає за еталон низькодетонуючу (індекс 100) та сильно детонуючу (індекс 0).
- Гексан (C6H14). Це важливий розчинник, слід уникати його вдихання, оскільки він дуже токсичний.
- Бутан (C4H10). Поряд з пропаном (C3H8), складають так звані скраплені нафтові гази (LPG), які утворюються в газових мішках в процесі видобутку нафти. В даний час заохочується заміна бензину або дизельного палива на зріджений газ як паливо, оскільки він є більш екологічно чистого вуглеводню (при його згорянні він виділяє лише вуглекислий газ та воду).
- Ікозано (C20H42). Це двадцятивуглецевий алкан (префікс ico означає двадцять)
- Циклопропан (C3H6). Раніше він використовувався як знеболюючий засіб
- н-гептан (C7H16). Це той, який береться за еталон нульової точки октанової шкали бензину, що було б найменш бажаним, оскільки він горить вибухонебезпечно. Його отримують з певної смоли рослини.
- 3-етил-2,3-диметилпентан (C9H20)
- 2-метилбутан (C5H12)
- 3-хлор-4-н-пропілгептан (C10H21Cl)
- 3,4,6-триметилгептан (C10H22)
- 1-бром-2-фенілетан (C8H9Br)
- 3-етил-4-метилгексан (C9H18)
- 5-ізопропіл-3-метилнонан (C13H28)
- Кубинський (C8H8)
- 1-бромопропан (C3H7Br)
- 3-метил-5-н-пропілоктан (C12H26)
- 5-н-бутил-4,7-діетилдекан (C18H28)
- 3,3-диметилдекан (C12H26)
