Eksempel på volumetrisk analyse
Kemi / / July 04, 2021
På Analytisk kemi, det Volumetri er en analysemetode, der består af Måling af det reagensvolumen, der er nødvendigt for at reagere støkiometrisk med analytten, hvilket er det stof, der skal bestemmes.
Reager støkiometrisk refererer til de stoffer, der interagerer kemisk, ifølge andel, der markerer den kemiske ligning allerede afbalanceret.
Det stof, der skal undersøges, kaldes Analyt. Et kendt og nøjagtigt målt volumen tages som en prøve af dette stof, som vi kalder Alikvot, indeholdt i en Erlenmeyer-kolbe for at starte analysen.
Begreber om volumetrisk analyse
Volumetrisk analyse, der er en type Kemisk analyse, bære involveret en kemisk reaktion. Denne kemiske reaktion vil blive udført mellem prøven med en ukendt mængde af det undersøgte stof og en kendt mængde af et andet stof, der er i stand til at reagere med den førstnævnte.
Det reaktionsstoffer vil være i vandig opløsning, og mængderne af opløsninger, der interagerede for at nå slutningen af reaktionen, måles, hvilket vil være synligt takket være en indikator, der giver farve inde i kolben.
I volumetrisk analyse er den vandige opløsning af Kendt koncentration kaldes standardløsning, Standard eller Titrantog vil tjene som en reference til, når reaktionen afsluttes, til at foretage den beregning, der afslører mængden af det undersøgte stof.
Denne procedure til at få begge opløsninger til at reagere kaldes Kemisk grad o Værdiansættelse, som er den grundlæggende del af volumetrisk analyse. Består af at gå gradvist hælde standardløsningen (Titrant) i alikvoten (Prøve), indtil indikatoren viser ændringen med en farveforskel.
EN Indikator Det er et kemisk stof, der tilsættes alikvoten, der viser en farve, og at når reaktionen slutter, vil den ændre farve.
En volumetrisk analyse består af en simpel række trin:
1. - Forberedelse af standardopløsning
2.- Forberedelse af prøven eller alikvoten
3.- Kemisk grad
4.- Volumenmåling
5.- Beregning af det undersøgte stof.
Til det punkt, hvor de allerede har gjort reagerede fuldt ud de to stoffer, kaldes det Ækvivalenspunkt.
Som i enhver kemisk analysemetode er der i volumetrisk analyse krav til gode resultater:
-Den kemiske reaktion skal være Selektivdet vil sige, at standardopløsningen kun reagerer med prøven.
-Den kemiske reaktion skal være Støkiometriskdet vil sige adlyde proportionerne markeret i den afbalancerede kemiske ligning.
-Den kemiske reaktion skal være Kvantitativ; henviser til 99,9% afslutning ved ækvivalenspunktet.
-Der skal være en detekterbart slutpunkt i reaktion, hvilket bedre vil blive bekræftet af indikatoren.
Primært mønster
Det Primære mønstre De er stoffer med høj renhed, hvis koncentration i opløsning beregnes direkte ud fra den vejede mængde og det anvendte volumen vand.
A) Ja, kan reageres med arbejdsløsninger, at kende koncentrationerne af sidstnævnte og konvertere dem til standardløsninger.
Eksempler på primære mønstre er:
-Natriumcarbonat (Na2CO3): Bruges til at standardisere syrer, såsom svovlsyre.
-Kaliumbifthalat: Det er den primære standard at fremstille standardopløsninger af baser, såsom natriumhydroxid.
-Natriumchlorid (NaCl): Det bruges til at standardisere sølvnitratopløsninger.
-Calciumcarbonat (CaCO3): Primær standard for EDTA (ethylendiamintetraeddikesyre).
Et primært mønster skal opfylde flere væsentlige egenskaber:
Skal have en Høj renhed, Atmosfærisk stabilitet, Fravær af hydratiseringsvand, Lave omkostninger og nemme at få, Y Høj ækvivalent vægt.
Klassificering af volumetrisk analyse
Afhængigt af den kemiske art, som du arbejder med at foretage en analyse med, vil det være typen af volumetri:
Syrebasevolumetri: Det fungerer, enten med en syre eller med en base, til at analysere prøver, der indeholder syrer eller baser.
Nedbørsmængde: Også kaldet Argentometry, det bruger en standardopløsning af sølvnitrat til at bestemme, hvor mange klorider der er i en prøve.
Kompleksitetsvolumetri: En standardopløsning af et kompleksdannende middel, såsom EDTA, bruges til at måle koncentrationen af hårdhed, dvs. calcium og magnesiumcarbonater, i vandet.
REDOX-volumetri: Reaktionen finder sted mellem et oxiderende stof og et reducerende stof.
Indikatorer
Af de mange indikatorer, der bruges i volumetriske markeringer, skiller tre sig ud:
1.- Methylorange: Det tager en orange farve i alikvoten, som titreres med en syre. Når ækvivalenspunktet er nået, bliver indikatoren gul.
2.- Phenolphthalein: Det er gennemsigtigt i starten i alikvoten, der vil blive titlen med en base. Når ækvivalenspunktet er nået, bliver indikatoren lyserød.
3.- Eriokrom sort: Det er den indikator, der bruges til at bestemme hårdheden i vand. I begyndelsen er den lilla i alikvoten, indtil den titreres med et kompleksdannende middel. I slutningen af reaktionen bliver den blå.

Instrumenter i en volumetrisk analyse
I en volumetrisk analyse vil en række instrumenter blive brugt, som, hvis de ikke er tilgængelige, ikke kan udvikles tilstrækkeligt:
1.- Volumetrisk kolbe: Det er en beholder som en pære i sin nedre del, fladt i bunden, som har en tynd søjle, hvori væsken tilsættes. Det har et mærke, der angiver, hvor væskens menisk skal være, så den dækker det nøjagtige volumen. Det bruges til at indeholde standardløsninger; takket være nøjagtigheden af dets volumen sikres en kendt koncentration.

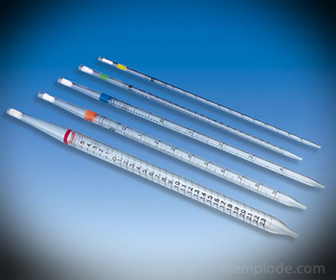
2. - Pipetter: De er graduerede tynde rør, der gør det muligt at måle pålideligt nøjagtige mængder væske. De fås op til 25 ml og muliggør nøjagtig prøvetagning.
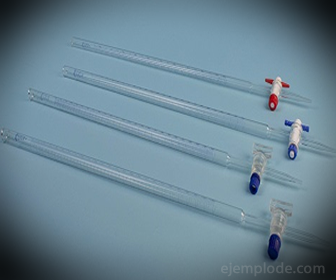
3.- Burette: Det er et langstrakt rør med en kapacitet på 50 ml, der indeholder standardopløsningen. I den ene ende har den en strømningsregulerende ventil, der dræner opløsningen i alikvoten.
4.- Erlenmeyer-kolber: De er beholdere med en flad base, konisk form, der ender i en cylindrisk kant. Dette design gør dem egnede til kemiske titreringer, da de ikke tillader, at løsningen ryster op. Der kræves mindst tre, hvis gentagne test skal udføres for at sikre et pålideligt resultat.

Beregninger i en volumetrisk analyse
Når vandige opløsninger håndteres, er mængderne af betydning for en volumetrisk analyse koncentration og volumen.
Hovedligningen af Volumetry er baseret på fire hoveddata:
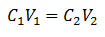
C1= Prøvekoncentration (ukendt)
V1= Volumen af alikvoten, som analysen blev arbejdet med
C2= Koncentration af standardopløsning brugt til at nå ækvivalenspunktet
V2= Volume Standard Solution nødvendig for at nå slutningen af reaktionen
Data erstattes i ligningen, hvilket kun efterlader den koncentration, der søges, som ukendt. Naturligvis skal alle data være på de samme drev.
Eksempler på volumetriske analyser
Bestemmelse af chlorider (Cl-) ved Argentometry med sølvnitrat.
Bestemmelse af bromider (Br-) ved Argentometry med sølvnitrat.
Bestemmelse af cyanider (CN-) ved Argentometry med sølvnitrat.
Bestemmelse af magnesiumcarbonat (MgCO3) ved kompleksmetri med EDTA.
Bestemmelse af calciumcarbonat (CaCO3) ved kompleksmetri med EDTA.
Svovlsyre-analyse (H2SW4) med natriumhydroxid (NaOH).
Analyse af natriumhydroxid (NaOH) med saltsyre (HCI).
Bestemmelse af antimon (III) med kaliumpermanganat (KMnO4).
Bestemmelse af arsen (III) med kaliumpermanganat (KMnO4).
Bestemmelse af titanium (III) med kaliumpermanganat (KMnO4).
Bestemmelse af molybdæn (III) med kaliumpermanganat (KMnO4).
Bestemmelse af jern (II) med kaliumpermanganat (KMnO4).
Bestemmelse af oxalation med kaliumpermanganat (KMnO4).