Peptiidsideme näide
Keemia / / July 04, 2021
The Peptiidvõlakiri on see, milles kaks aminohappemolekuli on ühendatud kondenseerumisega.
Peptiidsidemete paremaks mõistmiseks tuleb kõigepealt määratleda aminohapped:
The Aminohapped on orgaanilised molekulid lühike sisaldab vähemalt aminorühm (-NH2), leeliseline, ja karboksüülrühm (-COOH), happelise iseloomuga.
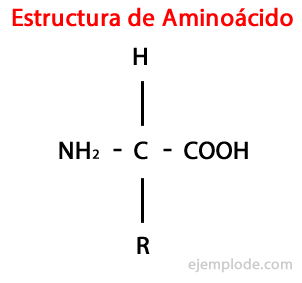
Kuigi elusolendid sünteesivad erinevatel eesmärkidel väga erinevaid aminohappetüüpe, on kõige olulisemad need on osa valkudest, mis kõik kuuluvad klassi a-aminohapped.
Α-aminohappeid iseloomustab see, et happe- ja aminorühmad on kinnitatud samale süsinikuaatomile, mida nimetatakse süsinikuaatomiks. Lisaks seob see a-süsinik kolmanda asendajana vesiniku aatomit ja neljandana asendaja, erineva suuruse ja omadustega täiendav rühm, mis eristab kõiki aminohappeid teised.
Neljandat asendajat nimetatakse Külgkett aminohappe ja on sageli lihtsustatud kujul tähega R tähistatud.
Kuna a-süsiniku neli asendajat on erinevad ja nende ümber on tetraeedriline paigutus, esinevad a-aminohapped optiline isomeeria
, mis on siis, kui molekulil on a asendusvorm mis näeb välja nagu a peegelpilt tema, mis lõpuks pole võrdne molekul. Neile kahele molekuli isomeersele vormile omistatakse tähed D või L, sõltuvalt sellest, kuidas asendajad ruumis paiknevad. Kõik aminohapped, mis on valkudes, on L.Aminohapped klassifitseeritakse vastavalt keemilisele omadusele Polaar ja Apolar. Polaarid jagunevad omakorda Neutraalne ja laetud (mis võib olla happeline või aluseline). The Mittepolaarne võib olla alifaatne või aromaatne.
Peptiidid ja peptiidside
Peptiidid on aminohapete kovalentse liitumise tulemusena amiidsidemed, mis moodustuvad ühe ja teise amino karboksüüli otsa kondenseerumine, vabastades vees molekuli reaktsioon. Seda liitu nimetatakse peptiidsideks.
Selle reaktsiooni mehhanism on esitatud allpool, milles Amino- ja karboksüülrühmad, ja peptiidi moodustamiseks toimub aminohappe molekulide kondenseerumine.
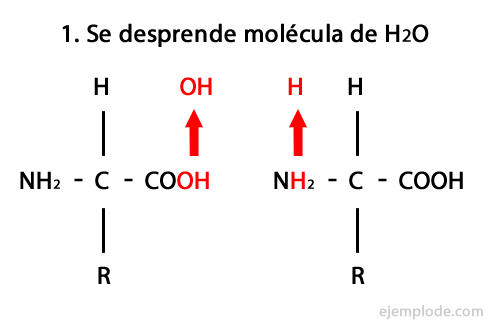
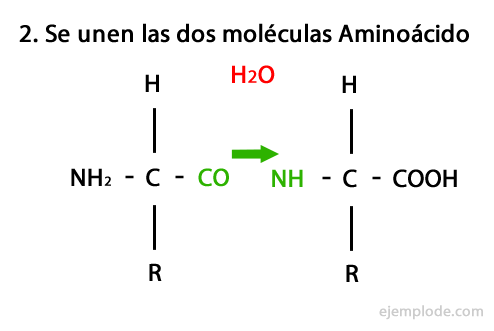

Peptiidid, nagu aminohapped ja valgud, nende otstes on aminorühm ja karboksüülrühm reageerimata.
Lihtsa peptiidi ja isegi valgu valemi täpsustamiseks piisab selle koostamise aminohapete loetlemisest, alustades tasuta Amino grupigaja lõpetades selle vaba karboksüülrühmaga.
Mõned kehas leiduvad peptiidid on Vasopressiin, mis tõstab vererõhku ja suurendab vee neeldumist; Entsefaliin, mis vähendab valuaistingut; ja Oksütotsiin, mis põhjustab emaka kokkutõmbumist.
Peptiidsideme omadused
Ühe aminohappe aminorühma kondenseerumine teise aminohappe karboksüülrühmaga, toimub vesilahustis, nii et see pole spontaanneja seetõttu vajab valgusüntees energiavarustust.
Nagu iga amiidsidemega, peptiidside esitab resonantsi kahe äärmusliku vormi vahel: neutraalne vorm, kusjuures üksikside ühendab esimese aminohappe karbonüülsüsiniku ja teise (C-N) aminolämmastiku ning vorm koos laengute eraldamisega milles kaks aatomit on ühendatud kaksiksidemega (C = N). Tegelikkuses ei omanda peptiidside kumbagi äärmuslikku olukorda, vaid on mõlema resonants hübriid.
On kõne Peptiidlennuk, koosnevad kõik peptiidsidemega seotud aatomid, mis ühinevad kahe algse aminohappega. Ühelt poolt lämmastiku ja vesiniku aatomid koos vastava süsinikuaatomiga esimeses aminohappes. Teiselt poolt teise aminohappe süsinik a koos karbonüülrühma hapniku ja süsinikuga.
Erinevused peptiidide ja valkude vahel
The peptiidides on vähe aminohappeid, mis ulatub kahest kuni mõnekümneni ja nende vorm lahuses muutub paindlikuks.
The väikesed valgud, struktuuriliselt suurtele peptiididele lähedased, on a määratletud konformatsioon ja palju vähem paindlik.
On valke, millel on sarnaselt peptiididele häiritud ja paindlik konformatsioon, kuid mis on järjestuses, kui nad suhtlevad rakus teiste makromolekulidega.
20 näidet aminohapetest, mis osalevad peptiidide sidumisel
- Wisteria
- Tüdrukule
- Valine
- Leutsiin
- Isoleutsiin
- Proline
- Metioniin
- Fenüülalaniin
- Türosiin
- Trüptofaan
- Serine
- Treoniin
- Tsüsteiin
- Asparagiin
- Glutamiin
- Asparagiinhape
- Glutamiinhape
- Lüsiin
- Arginiin
- Histidiin

