იდეალური გაზისა და რეალური გაზის 20 მაგალითი
Miscellanea / / July 04, 2021
ქიმია არის მეცნიერება რომ შეისწავლის კომპოზიციასა და გარდაქმნებს, რომლებიც შეიძლება მოხდეს მატერიაში, მისი ნებისმიერი ფორმით. ქიმიის შესწავლის ერთ-ერთი ყველაზე მნიშვნელოვანი სფეროა ის გაზები.
გაზის კონცეფცია იგი დააარსა ბელგიელმა ქიმიკოსმა იან ვან ჰელმონტმა. გაზების ქცევის ასახსნელად შეიქმნა სხვადასხვა მათემატიკური განტოლებები სტატისტიკური საშუალებების გამოყენებით. ამასთან, საჭირო იყო ამ განტოლებების გამარტივება და შეცვლა, რადგან ისინი არ მუშაობდნენ ყველა ტიპის გაზზე, ამიტომ განისაზღვრა გაზის სხვადასხვა მოდელი (იდეალური გაზი ი ნამდვილი გაზისხვა შუალედურ მიდგომებთან ერთად). Მაგალითად: აზოტი, ჰელიუმი, მეთანი.
ამ თვალსაზრისით, შეიქმნა სამი კანონი, რომელიც ზოგადად უკავშირდება მოცულობას ტემპერატურა და გაზების წნევა:
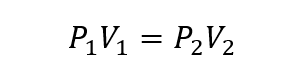
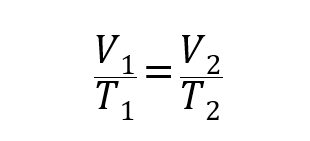
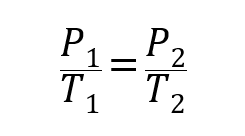
სად პ1, ვ1 ი თ1შესაბამისად არის გაზის საწყისი წნევა, მოცულობა და ტემპერატურა და პ2, ვ2 ი თ2 ფინალებია.
ამრიგად, სამ კანონსთან დაკავშირებით ვიღებთ გაზის ზოგადი კანონი,
PV / T = C სად გ არის მუდმივი, რომელიც დამოკიდებულია გაზის რაოდენობაზე.
იდეალური გაზის მაგალითები
იდეალური გაზი ეს არის თეორიული მოდელი, რომელიც წარმოადგენს გაზს, რომელიც სინამდვილეში არ არსებობს. ეს არის ინსტრუმენტი, რომელიც ხელს უწყობს მათემატიკური გამოთვლების დიდ რაოდენობას, რადგან იგი მნიშვნელოვნად ამარტივებს გაზის რთულ ქცევას. ეს გაზი ითვლება ნაწილაკებისგან, რომლებიც არც იზიდავს და არც მოგერიებს ერთმანეთს და რომელთა შეჯახება აბსოლუტურად ელასტიურია. ეს არის მოდელი, რომელიც ვერ ხერხდება, თუ გაზი განიცდის მაღალ წნევას და დაბალ ტემპერატურას.
ზოგადი განტოლება იდეალური გაზი წარმოიქმნება ბოილე-მარიოტის, ჩარლზისა და გეი ლუსაკის კანონების ავოგადროს კანონთან შერწყმით. ავოგადროს კანონში ნათქვამია, რომ თუ სხვადასხვა აირისებრი ნივთიერებები შეიცავს თანაბარი მოცულობით და ექვემდებარება ერთსა და იმავე წნევას და ტემპერატურას, მაშინ მათ აქვთ იგივე ნომერი ნაწილაკების. ამრიგად, მდგომარეობის იდეალური გაზის განტოლებაა: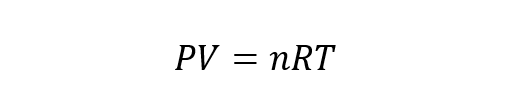
სად ნ არის გაზის მოლების რაოდენობა და რ გაზის მუდმივია ტოლი 8.314 J / Kmol.
შეუძლებელია იდეალური აირების სპეციფიკური ჩამონათვალის შედგენა, ვინაიდან ეს არის ა ჰიპოთეტური გაზი. ე. შეგიძლიათ ჩამოთვალოთ გაზების ნაკრები (კეთილშობილი გაზების ჩათვლით), რომელთა დამუშავება შეიძლება გაზების მკურნალობის მიახლოებით იდეალურია, რადგან მახასიათებლები მსგავსია, თუ წნევისა და ტემპერატურის პირობებია ნორმალური
- აზოტი (N2)
- ჟანგბადი (O2)
- წყალბადის (H2)
- ნახშირორჟანგი (CO2)
- ჰელიუმი (ის)
- ნეონი (ნე)
- არგონი (არ)
- კრიპტონი (კრ)
- ქსენონი (Xe)
- რადონი (Rn)
რეალური გაზების მაგალითები
რეალური გაზები ესენი არიან თერმოდინამიკური ქცევა და სწორედ ამიტომ არ მისდევენ მდგომარეობის იგივე განტოლებას, როგორც იდეალური გაზები. მაღალ წნევასა და დაბალ ტემპერატურაზე გაზები აუცილებლად უნდა ჩაითვალოს რეალობად, რადგან ამ შემთხვევაში მათ ნაწილაკებს შორის ურთიერთქმედება იზრდება.
არსებითი განსხვავება იდეალურ გაზსა და რეალურ გაზს შორის არის ის, რომ ამ უკანასკნელის შეკუმშვა შეუძლებელია განუსაზღვრელი ვადით, მაგრამ მისი შეკუმშვის სიმძლავრე შედარებით არის წნევისა და ტემპერატურის დონეზე.
შემუშავებულია სხვადასხვა განტოლებები რეალური გაზების ქცევის ასახსნელად. ერთ-ერთი ყველაზე მნიშვნელოვანია ვან დერ ვალსის მიერ 1873 წელს მოწოდებული, რომელიც უნდა იქნას გამოყენებული მაღალი წნევის პირობებში. ვან დერ ვაალის განტოლება წარმოდგენილია როგორც:
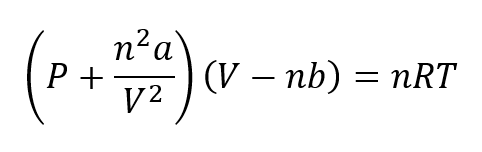
სად რომი ბისინი მუდმივები არიან, რომლებიც თითოეული გაზის ბუნებას ეხება.
შემდეგ ჩამონათვალში მოცემულია რეალური გაზების რამდენიმე მაგალითი, თუმცა შეგიძლიათ დაამატოთ ის უკვე ჩამოთვლილია როგორც იდეალური გაზები, მაგრამ ამჯერად მაღალი წნევის ან / და დაბალი კონტექსტში ტემპერატურა
- ამიაკი (NH)3)
- მეთანი (CH4)
- ეთანი (CH3CH3)
- ეთენი (CH2CH2)
- პროპანი (CH3CH2CH3)
- ბუტანი (CH3CH2CH2CH3)
მიჰყევით შემდეგს:



