Heterociklisko savienojumu piemērs
Ķīmija / / July 04, 2021
Ir cikliski ķīmiski savienojumi, kas sastāv tikai no oglekļa atomiem, un to valences papildina ūdeņraža atomi. Šādus savienojumus sauc homociklisks. A heterociklisks savienojums Tā ir organiska viela, kas satur gredzenu, ko veido vairāk nekā viena veida atomi; Bez oglekļa, visizplatītākie ir slāpeklis, skābeklis un sērs. Šie dažādie atomi tiek saukti heteroatomiem.
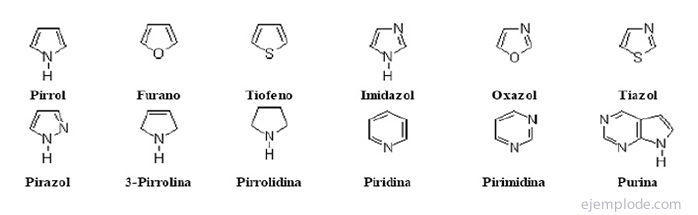
Iepriekš minētos savienojumus sauc par nieka nosaukumiem, tas ir, tirdzniecības nosaukumiem, kas nesniedz strukturālu informāciju par molekulu, bet kurus IUPAC ir akceptējusi un atzinusi.
Heterociklisko savienojumu klasifikācija
Heterocikliskos savienojumus klasificē pēc diviem galvenajiem kritērijiem: Saites veids kas satur (ja tie ir viens vai dubultā) un Gredzenu skaits tas bija.
Viņam Saites veids tie satur, ir klasificēti Alicikliskie savienojumi, kad tā saites ir vienas vai dubultas, bet ģeometrijā ir 5 vai mazāk atomu; Jā Aromātiski savienojumi, kad viņiem ir gredzens Benzols tā struktūrā vai uz kāda pamata heteroatoms pastāv.
Viņam Gredzenu skaits kas tai pieder, to var klasificēt kā Monociklisks, Biciklisks, Triciklisks, un vajadzības gadījumā tiek pievienots secīgs ciparu prefikss.
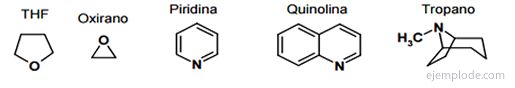
Trīs atomu heterocikliskie savienojumi
Ir trīs atomu heterocikliskie gredzeni, kas ir ļoti reaģējoši, jo tos viegli atver nukleofili, saukti par epoksīdiem un aziridīniem. Tie ir vērtīgi izejmateriāli organiskajā sintēzē.
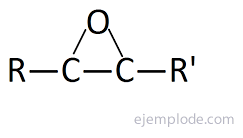
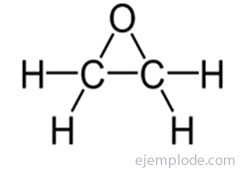
The Epoksīdi, ko sauc arī par oksirāniem, ir cikliski ēteri, kas sastāv no skābekļa atoma savienošanās ar diviem secīgiem oglekļa savienojumiem, kas savukārt veido daļu no kovalento saišu ķēdes. Tā ir trīsstūrveida struktūra, kuras pamats ir ogleklis un virsotne ir skābeklis. Tie ir bezkrāsaini šķidrumi, šķīst spirtos, ēteros un benzolā. Vienkāršākais termins ir Etilēna oksīds, ko sauc arī par Epoksietāns vai Oksirano. Tās sintēze notiek biežāk, pārtraucot dubulto saiti starp oglekļa atomiem ar skābēm, kas satur vairākus skābekļa atomus. Tie ir nosaukti, norādot skābekļa atoma piestiprināšanas vietas, kam seko prefikss "Epoxy-" un ogļūdeņraža nosaukums, kas to atbalsta.
Polimēros tie tiek izmantoti kā plastmasa konstrukcijām, pārklājumiem un līmēm. Turklāt viņiem ir svarīga līdzdalība abrazīvu, berzes materiālu ražošanā, tekstilrūpniecībā, čugunā, filtros un lakās. Arī minerālvatei, impregnēšanai, koksnes materiāliem, putām, formēšanas pulveriem. Pārtikas rūpniecībā epoksīdus izmanto kā ķīmiskos sterilizatorus pārtikas produktos ar zemu mitruma līmeni un aseptiskos iepakojuma materiālos.
The AziridīniTāpat kā epoksīdiem, tiem ir trīsstūrveida struktūra, tikai tas, ka heteroatoms ir slāpeklis. Tie ir bezkrāsaini šķidrumi, šķīst ūdenī, indīgi un ar amonjaka smaku. Viņiem ir īpaša fiziskā īpašība, kas tiek attiecināta uz gredzena ģeometriju; slāpekļa atomam ir ievērojami lielāka barjera piramīdas inversijai nekā citiem monocikliskajiem un acikliskajiem amīniem. Noderīga procedūra aziridīna sintēzei ir 1,2,3-triazolīnu pirolīze vai fotolīze. Šos savienojumus var viegli sagatavot, reaģējot azīdiem ar alkēniem 1,3-dipolārās cikliskās pievienošanās reakcijā.
Iztvaicējot, aziridīns var sasniegt kaitīgu koncentrāciju gaisā 20 ° C temperatūrā. Reaģē ar oksidētājiem un ir pakļauti degšanai, veidojot slāpekļa oksīdus.

Piecu atomu heterocikliskie savienojumi
Vienkāršākie no piecu atomu heterocikliskajiem savienojumiem ir: Pirole, ar slāpekļa heteroatomu, Furāns, Skābekļa heteroatoms un Tiofēns, Sēra heteroatoms.
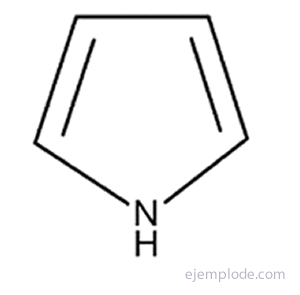
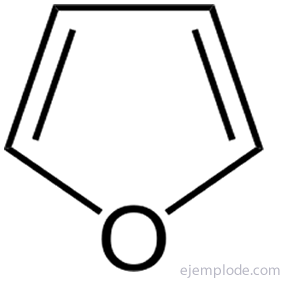
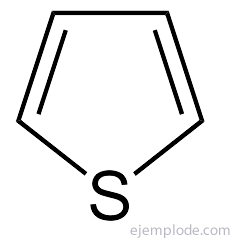
Pirola gredzens ir porfirīna sistēmas pamatvienība, kas atrodama, piemēram, hlorofilā un hemoglobīnā.
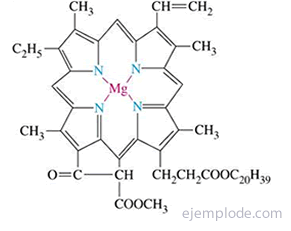
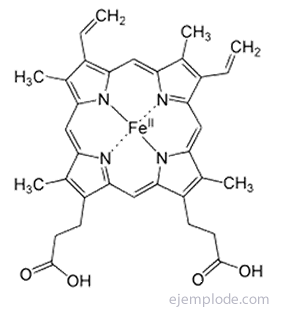
Pirols mazos daudzumos ir atrodams akmeņogļu darvā, tāpat kā tiofēns. Daļēji destilējot darvu, tiofēnu (viršanas temperatūra 84 ° C) savāc kopā ar benzolu (viršanas temperatūra 80 ° C).
Vieglākais veids furāna iegūšanai ir Furfural dekarbonilēšana (oglekļa monoksīda atdalīšana) (furfuraldehīds), ko savukārt iegūst, apstrādājot auzu vai rīsu sēnalas vai kukurūzas vālītes ar skābi verdoša sālsskābe.
Sešu atomu heterocikliskie savienojumi
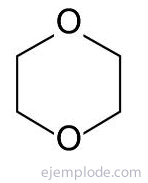
Starp piesātinātajiem terminiem viens no svarīgākajiem ir 1,4 dioksāns vai dioksāns, kas ir šķidrums bezkrāsains, ar raksturīgu smaku, kura tvaiki ir blīvāki par gaisu un var izplatīties pa ES parasti. Saskarē ar gaisu var veidot sprādzienbīstamus peroksīdus. Reaģē ar oksidētājiem un stiprām skābēm. Spēcīgi reaģē ar dažiem katalizatoriem.
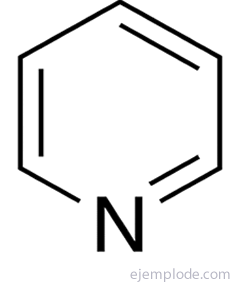
Starp nepiesātinātajiem heterocikliem viens no svarīgākajiem terminiem ir piridīns, kas sastāv no benzola gredzena struktūras ar slāpekļa heteroatomu. Tā ir daudzu vitāli svarīgu molekulu, piemēram, dezoksiribonukleīnskābes sastāvdaļu, priekšgājēja konfigurācija.
Heterociklisko savienojumu sistemātiskā nomenklatūra
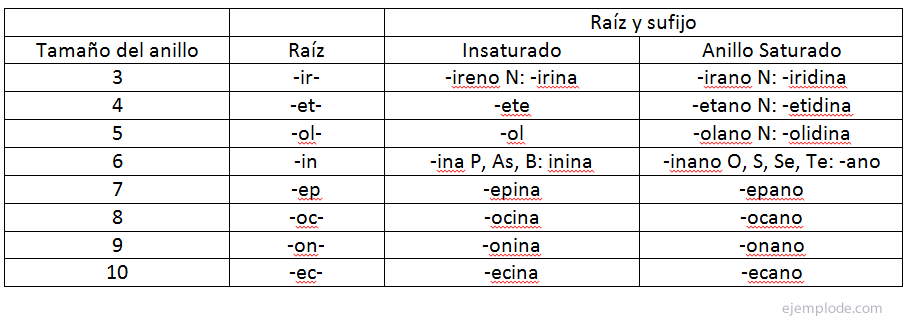
Heterocikliskiem gredzena (monocikliskā) savienojumiem atbilstošo nomenklatūru iegūst, apvienojot noteiktai saknei atbilstošu prefiksu un sufiksu saskaņā ar šādiem noteikumiem:
The priedēklis apzīmē heteroatomu, Sakne izskaidro gredzena izmēru un Sufikss nosaka nepiesātinājuma pakāpi. Nomenklatūrā jāievēro prefikss-sakne-sufikss.
The heteroatomu raksturs tiek apzīmēts ar prefikiem, piemēram, okso skābeklim, onkulis attiecībā uz Sēru vai aza slāpeklim.
The heteroatomu daudzveidība ir apzīmēts ar papildu prefiksu, piemēram, di, tri, tetra utt.
Ja ir divi vai vairāki dažādi heteroatomi, tos nosauc ar šādu prioritāti: O> S> N; piemēram Oksaso skābeklim un slāpeklim, Tiazo attiecībā uz sēru un slāpekli, Oxatio skābeklim un sēram.
The gredzena izmērs to apzīmē ar pareizu kātu.
The nepiesātinājumu pakāpe ir norādīts ar piedēkli. Ir ērti atzīmēt, ka sufikss ir nedaudz modificēts, ja heterocikliskajā gredzenā nav slāpekļa.
Gredzena numerācija sākas ar visaugstākās prioritātes heteroatomu un turpinās ap gredzenu, piešķirot pēc iespējas zemākus skaitļus pārējiem heteroatomiem vai aizvietotājiem.
Kad sistēmā, kurai ir maksimālais divkāršo saišu skaits, gredzenā joprojām ir piesātināts atoms, to norāda ar skaitli, kas norāda tās stāvokli un burtu. H- lielais kursīvs kā priedēklis.



